Общая характеристика
ЦИК — комплексы, состоящие из антигена, антител и связанных с ними компонентов комплемента С3, С4, С1q. В норме иммунные комплексы, образовавшиеся в кровотоке, фагоцитируются и разрушаются как фагоцитами, так и печенью. Однако при увеличении их размера (при избытке антигена и наличии в их структуре IgM, C1q-компонента комплемента) комплексы могут откладываться в периваскулярном пространстве и корковом слое почек, вызывая активацию комплемента и воспалительные процессы. Чаще иммунные комплексы откладываются в эндотелии кровеносных сосудов, почечных клубочках, суставах, что, соответственно, проявляется клиническими признаками васкулита, гломерулонефрита, артрита. Патогенез аутоиммунных заболеваний тесно связан с накоплением иммунных комплексов в тканях.
Клетки иммунной системы
Лейкоциты. Их назначение – распознавать чужеродных веществ и микроорганизмов, бороться с ними, а также запоминать информацию о них. Выделяют несколько видов лейкоцитов: — лимфоциты: В-лимфоциты получили свое название от латинского слова «bursa» — сумка (по названию сумки Фабрициуса – органа, в котором созревают В-лимфоциты у птиц. У человека этот процесс происходит в костном мозге). Эта разновидность лимфоцитов вырабатывает антитела (иммуноглобулины). Т-лимфоциты контролируют работу В-лимфоцитов, то есть продукцию антител. Свое название они получили от слова «тимус» — орган, в котором происходит их созревание. ٭Тимус – то же, что вилочковая железа. Т-хелперы — разновидность Т-лимфоцитов, помогающих синтезу антител (to help — англ. – «помогать»). Т-супрессоры — разновидность Т-лимфоцитов, подавляющих синтез антител (to supress — англ. – «подавлять, пресекать, сдерживать, запрещать»). — натуральные киллеры (НК) – это лимфоцитоподобные клетки, которые лишены признаков Т- и В-лимфоцитов. Они способны уничтожать опухолевые клетки и клетки, инфицированные вирусами; — нейтрофильные лейкоциты (палочкоядерные: ядро имеет вид изогнутых палочек; сегментоядерные: ядра сегментированы, имеют перетяжки); — эозинофильные лейкоциты; — базофильные лейкоциты. Нейтрофилы, эозинофилы и базофилы – это разновидности лейкоцитов, однако эти клетки не одинаково воспринимают красящие вещества, вследствие чего и различаются в названиях. Эозинофилы участвуют в уничтожении паразитов (выделяют специальные ферменты, оказывающие на них повреждающее действие), а также в аллергических реакциях (выделяют вещества, уничтожающие гистамин, предотвращающие выход ферментов из гранул тучных клеток). Нейтрофилы иногда называют «микрофагоцитами», указывая на их способность фагоцитировать микроорганизмы. Макрофаги, или фагоциты «поедают» живых и мертвых микробов, комплексы антиген-антитело (образуются в процессе борьбы с вирусами, бактериями и их токсинами), погибшие клетки самого организма. Без этих клеток невозможна деятельность лимфоцитов, поскольку именно они «помогают» последним распознавать антигены, выделяют медиаторы (вещества, которые стимулируют или угнетают деятельность других клеток иммунной системы). Среднее число микробов, поглощенных одной фагоцитирующей клеткой, называют фагоцитарным числом, а процент фагоцитирующих макрофагов – фагоцитарным показателем. На поверхности клеток находятся антигены – своеобразные маркеры (метки), по которым одни клетки отличаются от других. Их называют кластерами дифференцировки (CD). То, какие метки находятся на поверхности клетки, зависит от ее вида (Т-лимфоцит, В-лимфоцит и т.д.) и ее зрелости (способности выполнять свои функции). Метки нумеруются по очереди, в соответствии с тем, когда они были открыты: чем раньше был открыт кластер, тем меньше у него номер. В лабораториях кластеры дифференцировки выявляются с помощью моноклональных антител. ٭Клоном называют совокупность клеток, появившихся от одной общей клетки. Клетки клона идентичны на 100%. Одинаковые клетки синтезируют одинаковые антитела, которые и называют моноклональными.
Наиболее часто встречающиеся следующие виды кластеров: CD2 — кластер Т-лимфоцитов, NK-клеток; CD3 — кластер Т-лимфоцитов; CD4 — кластер Т-хелперов; CD8 – кластер Т-супрессоров; CD16 – кластер NK-клетки (натуральные киллеры); CD20 – кластер В-клеток. Обследование на иммуноглобулины дает информацию о состоянии гуморального звена иммунитета. Это используется в диагностике первичных и вторичных иммунодефицитов, аутоиммунных, инфекционных, гематологических и других заболеваний. Изменения иммунологических показателей могут быть проявлением нормальной реакции организма на воздействие физиологических или патологических факторов (с различной картиной сдвигов на разных стадиях заболевания), отражать чрезмерную активацию, истощение иммунной системы, характеризовать врожденный или приобретенный дефект отдельных звеньев иммунной системы.
Выделяют четыре разновидности иммуноглобулинов: IgM — этот вид антител появляется раньше всего при контакте с антигеном (микробом). Повышение их титра, или содержания в крови свидетельствует об остром воспалительном процессе. IgG — антитела этого класса появляются спустя какое-то время после контакта с антигеном. Они участвуют в борьбе с микробами: соединяются с антигенами на поверхности бактериальной клетки; затем к ним присоединяются другие белки плазмы (так называемый комплемент), в результате чего бактериальная клетка лизируется (ее оболочка разрывается). Кроме того, IgG участвует в возникновении некоторых аллергических реакций. IgA препятствуют проникновению микроорганизмов через слизистые оболочки. IgE — антитела этого класса взаимодействуют с рецепторами, расположенными на тучных клетках (٭клетки соединительной ткани, выделяющие физиологически активные вещества: гепарин, гистамин, серотонин и др. Они участвуют в процессах воспаления, свертывания крови и др.) и базофилах. В результате высвобождается гистамин и другие медиаторы аллергии. Развивается собственно аллергическая реакция. Один из самых важных показателей иммунного статуса – компоненты комплемента С3, С4. Комплементом называют набор иммунных белков, содержащихся в свежей сыворотке крови. Они участвуют в бактерицидном действии крови. С3 — центральный компонент системы комплемента, белок острой фазы воспаления. Это важнейшая часть защитной системы против инфекций. Он образуется в печени, макрофагах, фибробластах, лимфоидной ткани и коже. Поэтому нарушение их нормального состояния существенно влияет на этот компонент. С4 – гликопротеин, синтезируется в легких и в костной ткани. С4 поддерживает фагоцитоз, увеличивает проницаемость стенки сосудов, участвует в нейтрализации вирусов. Этот тест обычно назначают при подозрениях на аутоиммунные нарушения, повторные бактериальные инфекции; при динамическом наблюдении больных с системными аутоиммунными заболеваниями; при диагностике системной красной волчанки, ревматоидных васкулитов и других заболеваний. Еще один показатель иммунного статуса – криоглобулин – аномальный белок, который может присутствовать в крови при ряде заболеваний. При низкой температуре криоглобулины становятся нерастворимыми, приводя к закупорке небольших кровеносных сосудов, расположенных в пальцах рук и ног в холодную погоду, и вызывая появление характерной сыпи. Наличие криоглобулинов (криоглобулинемия) может являться симптомом различных заболеваний, в том числе макроглобулинемии, системной красной волчанки, а также ряда инфекционных заболеваний. Интерфероны – это особая группа белков, которые продуцируются клетками иммунной системы человека. Они представляют собой вид оружия, при помощи которого организм может противостоять болезнетворным бактериям, паразитам и даже раковым клеткам. Существует три основных класса интерферонов: интерферон альфа (α), интерферон бета (β), интерферон гамма (γ) и интерферон омега (ω). Все они не только обладают антивирусным и противоопухолевым действием, но и обладают свойством активировать – понуждать к действию другие факторы защиты – макрофаги и естественные киллеры. Все виды интерферона оказывают очень большое влияние на течение РНК-вирусных инфекций. В большинстве случаев продукция интерферона провоцируется проникновением в организм бактерий, вирусов или продуктов их жизнедеятельности.
Иммуноглобулины A, M, G, E
Общие иммуноглобулины – показатели гуморального иммунного ответа. Уровни IgM возрастают в острый период заболевания и при обострении хронической инфекции, IgG – в процессе выздоровления, IgA – в острый период заболевания, сохраняясь дольше IgM, отражают затяжное течение и поражение слизистых оболочек. Повышенные уровни IgE свидетельствуют об аллергическом воспалении.
Общие иммуноглобулины не объясняют причину инфекции, поэтому целесообразно смотреть специфические антитела к конкретным возбудителям. Основные показания для определения общих антител – это подозрение на врожденный иммунодефицит, связанный с гуморальным иммунитетом.
Исследуют Общий иммуноглобулин Е, иммуноглобулин G, иммуноглобулин M, иммуноглобулин A.
Клинический анализ крови с лейкоцитарной формулой
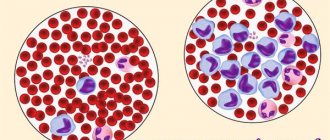
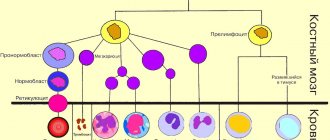
Клинический анализ крови с лейкоцитарной формулой позволяет выявить множество заболеваний. Он отражает состояние гемопоэза – созревания и роста клеток крови в костном мозге. О состоянии иммунной системы говорят уровни белых клеток крови – лейкоцитов и лейкоцитарная формула. Наблюдение за лейкоцитарной формулой в динамике заболевания позволит выявить осложнения, распространение инфекции по организму, реакцию на лечение.
При бактериальных инфекциях можно увидеть повышение лейкоцитов и нейтрофилов с появлением их молодых форм в крови.
При вирусных инфекциях, наоборот, лейкоциты снижаются, а в лейкоцитарной формуле преобладают лимфоциты.
Преобладание тех или иных популяций в лейкоцитарной формуле помогает в диагностике причины воспаления. Например, при определенных инфекциях (например, инфекционный мононуклеоз) нарастают измененные моноциты, а при аллергических и паразитарных заболеваниях – эозинофилы.
Наличие совсем юных клеток (бластов) в крови признак чрезмерной активации костного мозга, а низкий уровень лейкоцитов и нейтрофилов без воспаления – его угнетения.
Лимфоциты, иммунофенотипирование
Выделяют разные популяции лимфоцитов, которые играют ключевую роль в направлении иммунного ответа – клеточный или гуморальный. Определение иммунного фенотипа лимфоцита возможно в специальном исследовании методом проточной цитофлюориметрии. Фенотип лимфоцитов зависит от особых рецепторов на их поверхности – кластеров дифференцировки CD. Наличие того или иного рецептора свидетельствует о принадлежности клетки к определенной популяции лимфоцитов.
Определяют Клеточный иммунитет:
- В-лимфоциты (CD19+)
- Т-лимфоциты (CD3+) общие и их подтипы:
- Т-хелперы (CD3+CD4+)
- Т-цитотоксические (CD3+CD8+)
- Т- клетки-киллеры (CD3+CD16+CD56+)
- Естественные клетки-киллеры (CD3-CD16+CD56+)
- Лимфоциты с маркером HLA-DR+
- Иммунорегуляторный индекс (Т-хелперы/Т-цитотоксические)
Дополнительно исследуют другие CD маркеры лимфоцитов для определения их активности.
Оценка результата возможна только в совокупности с данными клинической картины и иммуномодулирующей терапии. Иммунофенотипирование лимфоцитов, как правило, проводят в динамике. Так, при ВИЧ-инфекции, поражающей Т-хелперы, снижение уровня CD3+CD4+ — клеток и иммунорегуляторного индекса (CD3+CD4+/CD3+CD8+) имеет плохой прогностический прогноз по течению заболевания.
Циркулирующие иммунные комплексы (ЦИК)
ЦИК – циркулирующие иммунные комплексы, уровень которых повышается при острых инфекциях, аутоиммунных заболеваниях. Циркулирующие иммунные комплексы (ЦИК) присутствуют у многих людей, страдающих системной красной волчанкой (СКВ) и ревматоидным артритом (РА), особенно в тех случаях, когда есть осложнения в виде васкулитов. Существует положительная корреляция (* систематическая и обусловленная связь) между активностью заболевания и уровнем ЦИК в крови. Формирование ЦИК представляет собой физиологический механизм защиты, приводящий к быстрому устранению либо эндогенных, либо экзогенных антигенов (например, микроорганизмы, вирусы, паразиты, растительные антигены, антигены грибов, пыльцы или пищевых продуктов) через ретикуло-эндотелиальную систему. Высокий уровень ЦИК в сыворотке и/или в других биологических жидкостях наблюдается при многих воспалительных и злокачественных заболеваниях, что может стать причиной развития патологии. Определение ЦИК в сыворотке — важный маркер для оценки активности заболевания, особенно при аутоиммунных заболеваниях.