Статья на конкурс «био/мол/текст»: Механизм остановки кровотечений необходим для выживания организма, однако, несмотря на историю исследования, насчитывающую десятилетия, многие детали этой системы остаются неясными. Восемь лет назад о свертывании крови «Биомолекуле» рассказал Михаил Пантелеев. С тех пор в этой области накопилось много новых данных. В этой статье мы расскажем, как молодой коллектив ученых из МГУ приоткрыл завесу тайны сразу над двумя загадочными явлениями в сложной системе формирования артериального тромба, показав, как в нем перемещаются умирающие клетки.
Основные функции тромбоцитов
По внешнему виду тромбоциты представляют собой круглые или овальные красные пластинки с гладкой поверхностью. Они образуются в костном мозге. Их созревание происходит в течение приблизительно 8 дней. Данные компоненты постоянно циркулируют в кровяном русле.
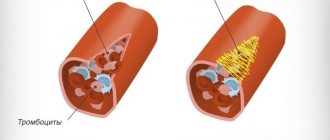
Главная функция тромбоцитов – обеспечение свертываемости крови. Кроме этого важной является способность данных компонентов крови – останавливать кровотечения. Это обеспечивается тем, что отдельные тромбоциты могут склеиваться между собой и прилипать к местам повреждения сосудов. Процесс автоматически запускается организмом человека при возникновении рисков кровотечения.
Важным является вопрос, сколько живут тромбоциты. Время их жизнеспособности длиться приблизительно 10 дней. В зависимости от возраста красных пластинок изменяется их размер: от 2 до 5 микрон в диаметре.
Процесс обновления тромбоцитов в крови происходит постоянно. Поэтому важным фактором для гарантии поддержания состояния крови является сбалансированность образования красных пластинок и их гибелью. В противном случае может наблюдаться склонность к тромбообразованию или повышенной кровоточивости.
Понятие о тромбоцитах
Пластинки бывают овальной или круглой формы. Когда они достигают поверхностей, на которых нет эпителиального слоя, то активизируется образование особенных отростков. Эти ветви предназначаются для остановки появляющегося кровотечения и закрытия ран, их длина больше размера тромбоцита в 5—9 раз.
Внутри гранул пластин содержатся тромбоцитарные ферменты, разрушающие оболочки бактерий и защищающие организм от вредных микроорганизмов. Отростки служат для ускорения перемещения в кровяном потоке путем прилипания к чужеродным телам, нити захватывают элементы, переваривают их. Защитный барьер создается при склеивании с другими тромбоцитами, то есть происходит свертывание крови.
Важной функцией тромбоцитов является поставка питательных микроэлементов к эндотелиальному слою. Продолжительность их жизни составляет от 7 до 12 суток, затем происходит разрушение в печени, легких и селезенке.
Формы тромбоцитов в крови:
- дегенеративные разновидности — содержатся в количестве до 0,2%;
- стереотипы раздражения — составляют от 0,8 до 2,3%;
- юные клетки — от 0 до 0,8%;
- зрелые формы — от 90,2 до 95%;
- старые пластинки — от 2,3 до 5,7%.
Инактивированные элементы представляют собой сплюснутые шаровидные формы, в которых полуоси находятся одна к другой в соотношении 2:8. Такая особенность применяется в случае распознавания оптических характеристик тромбоцитов и при регенерации параметров способом проточной цитометрии.
Строение клеток
Микроскопические исследования показывают, что перемена формы клетки при активации связывается с трансформацией кольца трубочек. Это явление вызывается преобразованием количества кальций-ионов.
Строение тромбоцитов неоднородное, присутствует гетерогенность, при этом конструкция содержит несколько слоев:
- наружная поверхность представлена трехслойной мембраной, в толще которой содержится фосфолипаза А, рецепторы сцепления с другими элементами и тканями;
- липидный слой является скоплением гликопротеинов и помогает пластинкам находиться в склеенном состоянии длительное время;
- микротрубочки в виде клеточного каркаса помогают сокращаться структуре для выброса содержимого тромбоцита за его пределы;
- область органелл представлена в строении разнообразными компонентами и факторами, которые способствуют заживлению ран.
В ранние периоды исследований отсутствовала фотографическая техника и не было однозначной терминологии, поэтому время начальных наблюдений за тромбоцитами точно не установлено. Есть информация, что первое изучение вел изобретатель микроскопа нидерландец ван Левенгук. В Англии сейчас клетки называются кровяными пластинками, термин ввел Биццоцеро в 181 году. Ему же приписывается открытие взаимосвязи элементов с гомеостазом и тромбоцитозом. В русском языке плоские кровяные клетки называются тромбоцитами, иногда используется название бляшка Боццоцеро.
Формирование и жизненный цикл
Их образование и созревание начинается в теле красного мозга в области тазовых костей и позвонков. Губчатая субстанция воспроизводит стволовые клетки, неспособные к процессу дифференциации и не разделяющиеся на определенные типы.
Тромбоциты проходят несколько степеней при формировании:
- стволовые клетки превращаются в элементы мегакариоцитарного ряда;
- начинается образование мегакариобласта — большого образования сетчатой структуры без гранул, с 2—3 круглыми ядрами;
- получившийся протромбоцит превращается в промегакариоцит и происходит формирование тромбоцита.
Преобразования происходят в результате воздействия генетических факторов. Недостаток клеток ведет к увеличению длительности кровотечения, повышенный объем элементов становится причиной формирования сгустков и закупорки сосудов. В результате перекрытия каналов может возникнуть инфаркт, инсульт, легочная эмболия или сосудистая пробка в других органах тела человека.
Неполноценность тромбоцитов или их недостаток носит наименование тромбоцитопатии. Низкий общий показатель количества пластинок при анализе вызывает последствие в виде тромботической пурпуры, при которой развивается ишемия разных органов или гемолитическая анемия, увеличивается число закупорок в сосудах после кровотечений.
Функции элементов
Тромбоциты формируют первичную пробку для затягивания раны поврежденного сосуда и ускоряют реакцию свертывания плазмы. Особенность пластинок в том, что они играют значимую роль в заживлении и восстановлении тканей, при этом выделяют полипептидные молекулы для роста и деления клеток. Тромбоциты быстро активируются при необходимости и переходят в новое необратимое состояние.
Пластины преобразовываются под действием возбудителей:
- основного белка соединительной ткани — коллагена;
- главного белка системы свертывания — тромбина;
- аденозинмонофосфата, продуцируемого поврежденными клетками — АДФ;
- активатора второго ряда, синтезируемого тромбоцитами для налаживания вазоконстрикции — тромбоксана А2.
Измененные плоские клетки крепятся к поврежденной поверхности, формируют пробку в результате прилипания к стенкам и друг другу. В результате обновляется форма пластинок, происходит экспрессия фосфатидилсерина и Р-селектина.
В обычном состоянии тромбоцитарная мембрана не поддерживает процедуру свертывания крови, при этом фосфолипиды находятся на ее внутреннем слое. Активация плоских элементов вызывает возбуждение белковых молекул скрамблазы, которые перебрасывают фосфолипиды на внешнюю оболочку. В итоге выравнивается концентрация фосфатидилсерина в обоих слоях. В процессе изменяются трансмембранные белки экзогенного слоя, которые ускоряют свертывание путем характерного сцепления факторов.
Анализ крови на тромбоциты
Определить количество тромбоцитов позволяет общий анализ крови. Основным показаниями для его проведения является следующее:
- Повышенная кровоточивость десен.
- Обильные менструации.
- Появление синяков при незначительных ударах.
- Частые носовые кровотечения.
- Трудности с остановкой крови при небольших повреждениях.
Количество тромбоцитов в крови измеряется в тысячах на 1 микролитр крови. Подсчет выполняется в специализированных лабораториях различными способами, которые гарантируют высокую точность.
Норма тромбоцитов в крови зависит от пола и возраста и составляет:
- У мужчин 200–400 тысяч.
- У женщин 180–320 тысяч, в период менструации количества может снизиться до 75–220 тысяч, а при беременности до 100–310 тысяч.
- У детей показатели зависят от возраста, и соответствующие значения приводятся в специальных таблицах.
Для проведения общего анализа крови выполняют забор крови из пальца. Особенной предварительной подготовки перед этим не требуется. Для гарантии получения точных результатов сдавать кровь лучше в утреннее время натощак. При этом за 12 часов до процедуры не рекомендуется употреблять жирные острые блюда, газированные напитки алкоголь.
Дополнительно для определения показателей свертываемости крови проводятся анализы по Сухареву и по Ли-Уайту. Они информативные и позволяют получить необходимые дополнительные данные о патологическом состоянии. Это позволит провести корректные лечебные мероприятия и избежать опасных последствий.
Что мы обнаружили и как нам это удалось
Биофизический подход
Как и любая сложная система, формирование тромба в артерии нуждается в управлении. Выявление механизмов, регулирующих биологические процессы, является одной из традиционных задач биофизики, поэтому проблема регуляции артериального тромбообразования уже давно привлекает внимание не только врачей и физиологов, но и биофизиков. На кафедре биофизики физического факультета МГУ на протяжении более двух десятилетий развивается направление, связанное с анализом принципов устройства и регуляции системы гемостаза: например, в ставших классическими работах профессора Ф.И. Атауллаханова и его учеников была продемонстрирована автоволновая природа распространения процесса свертывания плазмы крови в отсутствии потока [5], [6].
Установление механизмов, регулирующих тромбообразование в условиях артериального кровотока, — одна из главных задач нашего научного коллектива, участниками которого являются профессор кафедры медицинской физики М.А. Пантелеев, профессор кафедры биофизики Ф.И. Атауллаханов, с.н.с. кафедры биофизики Д.Ю. Нечипуренко, а также студенты и аспиранты физического факультета.
Исследование in vitro и in silico
Связать поверхностное распределение умирающих тромбоцитов с процессом сжатия тромба позволили недавние исследования, выполненные нами в сотрудничестве с коллегами из Франции и США [7]. При помощи конфокальной микроскопии в экспериментах по тромбообразованию in vitro мы показали, что прокоагулянтные тромбоциты формируются в различных частях растущего тромба, после чего перемещаются на его поверхность (рис. 1).
Рисунок 1. Динамика перемещения прокоагулянтных тромбоцитов в тромбе. а — Конфокальные микрофотографии тромбов в различные моменты времени. Зеленый цвет соответствует флуоресценции умирающих клеток (используется флуоресцентный маркер клеточной смерти). б — Тромбы в различные моменты времени. Зеленый цвет соответствует флуоресценции умирающих клеток, фиолетовый цвет — флуоресценции прикрепившихся к тромбу тромбоцитов (используется флуоресцентно-меченное антитело к поверхностным белкам тромбоцита). в — Основные величины, используемые для анализа перемещения тромбоцитов — вектор перемещения d, угол транслокации α между направлением перемещения и начальным радиус-вектором центра умирающей клетки, проведенным из центра тромба. г — Результаты анализа модулей средних скоростей перемещения и углов транслокации умирающих клеток (зеленый цвет) и «свежих» тромбоцитов, прикрепившихся к поверхности тромба (фиолетовый цвет). Масштаб — 10 микрометров.
[7]
Такое перераспределение сопровождается формированием фибрина на поверхности тромба. Так как умирающие (прокоагулянтные) тромбоциты достаточно слабо взаимодействуют с другими клетками и не участвуют в процессе контракции, было высказано предположение, что их перераспределение является результатом механического вытеснения в процессе активного сжатия тромба. Для проверки этой гипотезы была создана компьютерная модель сжатия тромбоцитарного агрегата, которая продемонстрировала работоспособность сформулированной гипотезы (рис. 2).
Рисунок 2. Моделирование контракции клеточного агрегата. а — Тромбоцитарный агрегат до и после сжатия. Зеленым цветом отмечены сферы, имитирующие прокоагулянтные клетки, которые не участвуют в процессе контракции и относительно слабо взаимодействуют с другими сферами. Контракция описывается как уменьшение равновесной длины парного потенциала (Морзе) взаимодействия между центрами сфер. б — Агрегат до и после контракции, в котором «прокоагулянтные» сферы, изначально расположенные внутри агрегата, имели различные радиусы. Фиолетовым цветом отмечены сферы, которые после контракции остались внутри агрегата, а зеленым — вне агрегата. в — Значение абсолютных величин перемещений прокоагулянтных тромбоцитов в экспериментах (ex vivo) и «прокоагулянтных» сфер в модели (in silico). г — Доля сфер, вытесненных в результате сжатия агрегата на его поверхность. Показаны результаты расчета для сфер различного радиуса.
[7]
Важной доказательной базой работы стали эксперименты с кровью уникальных генетически модифицированных мышей, тромбоциты которых лишены возможности проявлять механическую активность и, следовательно, обеспечивать контракцию тромба. В соответствии с предсказаниями модели и сформулированной гипотезы, умирающие клетки не перемещались к поверхности тромба в случае отсутствия контракции (рис. 3). Отсутствие поверхностного распределения умирающих тромбоцитов также сопровождалось отсутствием поверхностной локализации фибрина.
Рисунок 3. Сравнение распределения прокоагулянтных клеток и фибрина для нормальных и генетически модифицированных мышей. а — Распределение прокоагулянтных тромбоцитов (зеленый цвет) в нормальных мышах (верхняя панель) и модифицированных мышах (нижняя панель). Желтым цветом отмечен контур тромба, построенный по изображению в режиме дифференциально-интерференционного контраста. б — Анализ величин отношения суммарной флуоресценции поверхности умирающих клеток, находящихся вне плотной части тромба к флуоресценции таких же поверхностей внутри тромба для нормальных (WT) и генетических модифицированных мышей (MYH9). в — Распределение прокоагулянтных поверхностей (зеленый цвет) и фибрина (фиолетовый цвет) в тромбах мышей дикого типа (верхняя панель) и тромбах генетически модифицированных мышей (нижняя панель). Масштаб — 10 микрометров.
[7]
Повышение уровня тромбоцитов
Повышенные тромбоциты – это патологическое состояние. Его называют тромбоцитоз. Главная опасность патологии заключается в повышении рисков образования тромбов.
Причиной повышения уровня тромбоцитов в крови могут быть различные заболевания. Наиболее часто тромбоцитоз возникает на фоне:
- Злокачественных новообразований.
- Инфекционных болезней.
- Глистных инвазий.
- Хирургических операций.
- Аутоиммунных патологий.
- Почечной недостаточности.
Высокий уровень тромбоцитов в крови наблюдается у людей в пожилом возрасте. Временно показатели могут повышаться после тяжелых физических нагрузок, к примеру, после занятий спортом.
Симптоматика тромбоцитоза характерная, но при этом слабо выраженная. Следует обязательно провести общий анализ крови, если отмечаются следующие симптомы:
- Болевые ощущения в пальцах рук и ног.
- Зуд кожных поверхностей.
- Беспричинная слабость, которая приводит к снижению работоспособности.
- Отсутствие аппетита.
Конкурс «био/мол/текст»-2019
Эта работа опубликована в номинации «Своя работа» конкурса «био/мол/текст»-2019.
Генеральный спонсор конкурса и партнер номинации «Сколтех» — Центр наук о жизни Сколтеха.
Партнер номинации — Российский научный фонд.
Спонсор конкурса — : крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Спонсором приза зрительских симпатий выступила компания BioVitrum.
«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Специалистам и неспециалистам хорошо известно зловещее слово «тромбоз». Слово «тромб» традиционно воспринимается как что-то опасное. Однако не все тромбы представляют угрозу. При повреждении сосудистой стенки организм должен быстро сформировать что-то наподобие затычки, которая не даст крови вытекать из артерии или вены. Таким образом, формирование затычек, или, говоря научным языком, гемостатических тромбов, является ключевой задачей, которую решает система гемостаза человека (и, разумеется, не только человека). Однако иногда эта система дает сбой, и повреждение сосуда приводит к формированию массивного внутрисосудистого тромба, который практически полностью блокирует кровоток. Если этот процесс происходит в крупной артерии, питающей кровью жизненно-важный орган, такой тромб может стать причиной серьезных осложнений и даже смерти. Инфаркт миокарда и ишемический инсульт являются, пожалуй, самыми известными и распространенными осложнениями, вызванными артериальным тромбозом, которые сегодня являются наиболее частой причиной смерти и инвалидности людей в развитых странах [1].
Почему в некоторых случаях в ответ на повреждение система гемостаза срабатывает избыточно и формирует смертельно опасную пробку в сосуде? Несмотря на многие десятилетия исследований, данный вопрос остается без ответа. Отсутствие понимания механизмов, которые регулируют формирование тромба, приводит к тому, что сегодня не существует надежного способа предотвращения тромбоза: прием существующих антитромботических препаратов связан с достаточно высоким риском возникновения кровотечений — в том числе опасных для жизни.
Понижение уровня тромбоцитов
Пониженные тромбоциты, норма которых у мужчин и женщин разная, провоцируют развитие состояния, которое известно под названием тромбоцитопения. Очень часто она возникает на фоне неконтролируемого приема лекарственных препаратов: антидепрессантов и антибиотиков.
Причинами снижения уровня тромбоцитов в крови могут стать различные инфекционные болезни: ОРВИ, гепатит, герпес и пр. Наблюдаться тромбоцитопения может при включении в рацион большого количества продуктов разжижающих кровь. Это имбирь, вишня, чеснок, лук и др.
К неинфекционным факторам понижения уровня тромбоцитов в крови относя период беременности, авитаминоз, отравление алкоголем или тяжелыми металлами.
Заподозрить тромбоцитопению можно по следующим признакам:
- Обильным менструациям.
- Частым носовым кровотечениям.
- Появлением гематом.
При постоянном патологическом снижении уровня тромбоцитов в крови увеличиваются риски развития сильных кровотечений и инсультных состояний, которые несут угрозу жизни.
Восстановления уровня тромбоцитов в крови
Нормализовать уровень тромбоцитов в крови можно сбалансированным питанием. Важно насытить рацион продуктами, с высоким количеством материалов и микроэлементов. Нужно отказаться от острой пищи, алкоголя, фаст-фуда и сладких газированных напитков, вести здоровый образ жизни и соблюдать питьевой режим.
Если не удалось нормализовать показатели естественными способами, то нужно пройти полное обследование у гематолога. При повышенном уровне тромбоцитов могут быть назначены специальные медикаментозные средства – антикоагулянты или антиаггреганты. Они разжижают кровь и минимизируют риски образования тромбов. Но при этом принимать их нужно только по назначению врача. Следует понимать, что стабилизация состояния возможна только после устранения базовых причин, которые провоцируют отклонения от нормы.
Последствия низкого количества тромбоцитов
При состоянии пониженного количества тромбоцитов впоследствии развиваются нарушения, к которым относятся частые кровотечения (менструальные и носовые), при этом время кровотечения значительно увеличивается и его становится тяжело остановить. Может развиваться внезапная кровоточивость десен (не у всех). В моче или кале можно обнаружить кровяные сгустки. Появляются петехии (красные точки, являющиеся следствием повреждения стенки капилляров) на коже нижних конечностей, чаще голеней. Даже минимальные повреждения ведут к образованию экхимозов (синяков), когда в норме синяк бы не появился.
Сама тяжесть симптомов напрямую зависит от количества тромбоцитов. Чем меньше тромбоцитов, тем тяжелее клиника. При очень низком количестве тромбоцитов возможно возникновение внутреннего кровотечения в пищеварительный тракт или даже кровотечение в головной мозг.
Даже при наличии легкой клиники рекомендуется обращение к врачу-терапевту в целях профилактики данного состояния.