Диагностика
Выявляют безболевую ишемию миокарда теми же методами диагностики, что и другие формы ИБС. Наряду с изучением анамнеза заболевания и тщательным осмотром, которые проводит врач-кардиолог, используют следующие виды обследования:
- Холтеровское мониторирование. Его назначают при подозрении на безболевую форму ишемии миокарда.
- Стресс-тесты. Он обычно проводится на беговой дорожке или велотренажере, при этом осуществляется контроль сердечного ритма, артериального давления и дыхания. Если врач подозревает у вас наличие ишемии миокарда, но у вас отсутствуют какие-либо признаки или симптомы, назначают этот метод обследования сердечно-сосудистой системы.
- Электрокардиограмма (ЭКГ). Фиксирует нарушения электрической активности вашего сердца, которые свидетельствуют об субэпикардиальной или субэндокардиальной ишемии миокарда.
- Клинические анализы крови.
- Эхокардиограмма. Она поможет определить область повреждения сердца и нарушение его функции.
- Коронарография. При коронарографии рентгеновские изображения используют для изучения внутренней поверхности кровеносных сосудов вашего сердца. Во время коронарографии в кровеносные сосуды вашего сердца вводят контрастное вещество, которое видно на рентгеновских снимках. При этом рентгеновский аппарат выполняет ряд снимков (ангиограмм), что дает возможность изучить состояние кровеносных сосудов.
- КТ сердца. При проведении КТ выявляют наличие кальцификации сосудов сердца — основного симптома атеросклероза. Также состояние коронарных сосудов оценивается с помощью КТ коронарографии.
Классификация заболевания
Специалисты выделяют 2 основные формы безболевой ишемии:
Особенностью патологии является то, что пациент чувствует себя здоровым. Он может не знать о проблеме до тех пор, пока не начнут развиваться осложнения.
В некоторых случаях заболевание сопровождается:
- слабостью;
- быстрой утомляемостью;
- головокружениями.
Обычно пациенты не обращают внимания на симптом, который проявил себя однократно!
Между тем, патология прогрессирует! Она может перейти в новую форму и ярко проявить себя приступами боли.
К осложнениям заболевания относят:
- нарушения сердечного ритма;
- хроническую сердечную недостаточность;
- инфаркт миокарда.
В некоторых случаях ишемия становится причиной внезапной смерти. Медицинскими работниками прогноз патологии без адекватной терапии оценивается как неблагоприятный. Это обусловлено тем, что смертность достигает 35%.
Лечение
Лечение безболевой формы ишемии миокарда проводится теми же методами, что и лечение ишемической болезни сердца, протекающей с характерными симптомами. В зависимости от стадии заболевания и его особенностей, врач назначит:
- Медикаментозное лечение. Остановить развитие ИБС помогают некоторые лекарства для сердца. К необходимым препаратам относятся медикаменты, нормализующие артериальное давление и улучшающие качество работы сердечной мышцы. Также пациенты принимают препараты, снижающие уровень холестерина в крови и уменьшающие ее вязкость.
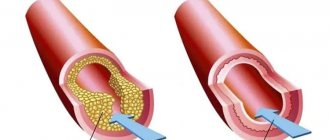
- Реваскуляризация миокарда. Для лечения ИБС используют аорто-коронарное шунтирование или внутрисосудистую операцию. При наличии показаний оптимальным вариантом считается эндоваскулярная операция по восстановлению пораженных сосудов — стентирование. Такой вид хирургической помощи безболезненный, поскольку он не требует общей анестезии и выполнения разрезов. В ходе операции в сосудистый просвет изнутри устанавливается эндопротез — стент, который удерживает стенки сосуда и обеспечивает нормальный кровоток.
- Нормализация образа жизни и вторичная профилактика. Рекомендуется исключить факторы, вызывающие рост холестериновых бляшек: жирная пища, малоподвижный образ жизни, курение. Подробнее о профилактике ишемической болезни мы поговорим в следующей публикации.
Бессимптомная ишемия миокарда
Ишемия миокарда — надежный показатель физиологически значимой ишемической болезни сердца (ИБС). В течение последних двух десятилетий, по данным эпидемиологических исследований и проспективного наблюдения, было установлено, что бессимптомная ишемия миокарда (БИМ), обнаруживаемая на ЭКГ, является неблагоприятным прогностическим фактором, так же как и у пациентов с доказанной ИБС. Результаты этих работ выявили настолько высокую прогностическую значимость ишемии миокарда у бессимптомных пациентов, что Американская ассоциация сердца и Американская коллегия спортивной медицины рекомендовали до начала программ интенсивных физических тренировок у мужчин с 45 лет и у женщин с 55 лет без явных заболеваний сердца и даже без факторов риска их развития проводить максимальный тест с физической нагрузкой на тредмиле.
Несмотря на эти рекомендации, вопрос о целесообразности проведения рутинных скрининговых исследований у практически здоровых лиц с целью выявления ишемии миокарда остается дискуссионным. Это связано с тем, что у практически здоровых лиц ишемию миокарда нередко диагностируют во время нагрузочного теста только по изменению сегмента ST, но без сопутствующих болей в грудной клетке. Отсутствие симптоматики явилось основанием для предположения о том, что изменения сегмента ST во время теста с физической нагрузкой, не сопровождающиеся болями в грудной клетке, не всегда отражают ишемические изменения миокарда и могут быть источником ложноположительных данных. Подобные сомнения возникли вследствие неправильного отбора пациентов для стресс-теста, при котором большинство обследованных исходно имели низкую вероятность диагноза ИБС. В то же время при правильном отборе на исследование (лица с высокой вероятностью ИБС) безболевая депрессия сегмента ST при нагрузке позволяет выделить группу пациентов с высоким риском развития сердечно-сосудистых событий и кардиальной смерти.
Диагностика
Преходящая ишемия миокарда наиболее часто бывает субэндокардиальной. Эпизоды субэндокардиальной ишемии обычно диагностируют с помощью ЭКГ-мониторирования по горизонтальной или косонисходящей депрессии сегмента ST >1 мм на расстоянии 0,06-0,08 с от точки J продолжительностью не менее 1 минуты.
Преодолев первоначальные технические трудности правильного воспроизведения низкочастотных ЭКГ-сигналов, современная технология позволяет достоверно воспроизводить положение сегмента ST с помощью устройств для ЭКГ-мониторирования. Возможность выявления ишемии миокарда с помощью ЭКГ-мониторирования увеличилась за счет использования двухполюсных грудных отведений. При этом одним из отведений обязательно должно быть модифицированное отведение V5 — CM-V5, так как оно обладает наибольшей чувствительностью для выявления депрессии сегмента ST независимо от локализации ишемии. В настоящее время появились ЭКГ-мониторы, позволяющие делать запись от 3 и даже 12 отведений. Однако вопрос о целесообразности использования более 2 отведений для улучшения диагностики субэндокардиальной ишемии пока не решен.
Отсутствие стенокардии во время ишемии миокарда в некоторых случаях можно объяснить незначительной продолжительностью и/или небольшой выраженностью ишемии. При значительной выраженности и продолжительности ишемии отсутствие болевого синдрома могут обусловливать несколько механизмов. Вероятно, причины отсутствия стенокардии различны: у пациентов с сочетанием болевых и безболевых приступов, у пациентов с преимущественно безболевыми приступами и у больных сахарным диабетом.
Сочетание эпизодов болевой и безболевой ишемии миокарда. Импульсы, проводимые по кардиальным афферентным нервным волокнам, модулируются в ганглиях сердца, ганглиях средостения и грудной клетки (афферентные волокна сердца, проходящие в симпатических нервах) или в ядрах tractus solitarius (афферентные волокна сердца, проходящие в парасимпатических нервах). Затем модуляция импульсов осуществляется в сером веществе головного мозга, расположенном около сильвиева водопровода, в гипоталамусе и таламусе. После этого импульсы билатерально подходят к различным участкам коры головного мозга, где и могут трансформироваться в болевые ощущения.
Реакция внутренних ганглиев сердца изменяется в возбуждающих и тормозящих синапсах. Местное воздействие на внутренние кардиальные нейроны ряда факторов (субстанция Р, брадикинин, окситоцин, ацетилхолин, никотин, аденозин и АТФ) приводит к изменению активности внутренних нейронов сердца. Установлено, что аппликация этих факторов на эпикардиальную поверхность сердца изменяет активность нейронов узловых ганглиев продолжительностью до 45 минут. Инфузия очень низких доз аденозина может уменьшить выраженность стенокардии, вызванной физической нагрузкой. Эти данные свидетельствуют о том, что восприятие ишемических болей в грудной клетке зависит не только от выработки сигналов, инициируемых ишемией миокарда, но и от модуляции их во внутренних ганглиях сердца, ганглиях средостения и грудной клетки.
Дальнейшее изменение импульсов, вызванных ишемией, может происходить в ЦНС на спинальном или супраспинальном уровне. Однако после достижения ЦНС афферентные импульсы проводятся в спиноталамическом тракте совместно с другими висцеральными и соматическими афферентными нервными импульсами. Маловероятно, что на этом уровне возможно избирательное подавление ишемических болей в грудной клетке, имеющих одинаковую продолжительность и выраженность. Таким образом, точный механизм отсутствия болевого синдрома у пациентов с сочетанием болевых и безболевых приступов ишемии остается неизвестным.
Отсутствие стенокардии у пациентов с БИМ. У лиц, которые никогда не испытывали ангинозных болей даже при развитии выраженной, продолжительной ишемии или у которых возникают преимущественно безболевые эпизоды, отсутствие болей может быть обусловлено психологическими факторами, стойко подавляющими восприятие боли. Это предположение подтверждается генерализованным нарушением восприятия боли. Действительно, пациенты с БИМ имеют более высокий порог и толерантность к болевым стимулам по сравнению с лицами с болевой ишемией. Эти данные подтверждаются при использовании следующих типов стимуляции: ишемия предплечья, холодовое воздействие, внутривенное введение аденозина, раздражение зубной пульпы и т.д. Изучение личностных особенностей пациентов с бессимптомной ишемией также выявляет более низкие показатели нервозности и возбудимости и более высокие показатели мужественности и меньшую предрасположенность к жалобам.
Существует предположение о роли эндогенных опиоидов в патогенезе БИМ. Известно три группы эндогенных опиоидов, происходящих от трех разных молекул-предшественников: 1) эндорфины, которые секретируются в основном гипофизом; 2) энкефалины, секретируемые надпочечниками; 3) динорфины, источник которых пока не известен. Эндогенные опиоиды действуют центрально, вызывая селективное подавление ноцицептивных нейронов. Вместе с тем, по данным позитронной эмиссионной томографии, у пациентов с БИМ по сравнению с пациентами со стенокардией оказалась значительно меньшей активация коры головного мозга во время ишемии миокарда.
Клиническая и прогностическая значимость БИМ при стабильном течении ИБС. Оценка суточного ритма эпизодов ишемии миокарда при стабильном течении ИБС выявляет пик их возникновения в утренние часы, особенно в течение первых часов после пробуждения и начала трудовой активности, то есть в период, которому соответствует максимальная симпатическая активация с соответствующим повышением потребности миокарда в кислороде и тонуса коронарных артерий. По данным амбулаторного ЭКГ-мониторирования (АЭКГМ), у пациентов со стабильным течением ИБС наличие бессимптомных эпизодов ишемии миокарда во время обычной повседневной активности может указывать на неблагоприятный прогноз. Так, при 24-часовом ЭКГ-мониторировании D.Tzivoni и соавт. среди 224 больных со стабильным течением ИБС после инфаркта миокарда у 33% выявили эпизоды безболевой ишемии миокарда. В течение 28-месячного наблюдения частота сердечно-сосудистых событий (смерть, повторный инфаркт, госпитализация по поводу стенокардии, баллонная ангиопластика или АКШ) составила 51% среди больных с эпизодами ишемии по сравнению с 12% среди пациентов без подобных изменений (p<0,0001). По данным мониторирования, ишемия миокарда оказалась более значимым неблагоприятным прогностическим фактором по сравнению с ишемией, выявляемой при тесте с физической нагрузкой (P<0,001).
Данные о более высокой прогностической значимости выявления ишемии миокарда при АЭКГМ по сравнению с тестом толерантности к физической нагрузке (ТТФН) подтверждены и в исследовании Asymptomatic Cardiac Ischemia Pilot (ACIP) Study. Были установлены достоверные прямые корреляции между индексами ишемии по данным ТТФН (число отведений ЭКГ с депрессией сегмента ST, время нагрузки до развития депрессии сегмента ST, сохранение депрессии сегмента ST в восстановительном периоде, максимальная глубина депрессии сегмента ST) и наличием и частотой бессимптомной ишемии по данным АЭКГМ. Несмотря на наличие корреляций между ТТФН и АЭКГМ в установлении факта ишемии, корреляции между индексами выраженности ишемии во время ТТФН и АЭКГМ оказались низкими.
В исследовании Angina and Silent Ischemia Study Group (ASIS) не было получено достоверных корреляций между числом эпизодов ишемии миокарда при АЭКГМ и продолжительностью нагрузки до появления депрессии сегмента ST. Таким образом, хотя ТТФН оказался полезен для выявления больных с высокой вероятностью ишемии миокарда при АЭКГМ, частота ишемических эпизодов, выявляемых при АЭКГМ, не отражала выраженность ишемии по данным ТТФН. Поскольку прогноз больных со стабильной стенокардией может определяться не только тяжестью ишемии миокарда при ТТФН, но и наличием и частотой бессимптомных эпизодов ишемии при АЭКГМ, мониторирование представляет дополнительную и независимую прогностическую информацию.
Амбулаторное ЭКГ-мониторирование оказывает существенную диагностическую помощь в оценке больных с так называемым кардиологическим синдромом Х (ангинозные боли, положительный ТТФН, нормальные коронарные артерии при коронароангиографии), который считают проявлением микрососудистой коронарной болезни. Анализ эпизодов депрессии сегмента ST при этом выявил их сходство с таковыми у больных со стабильным течением ИБС. Было также показано, что АЭКГМ выявляет эпизоды депрессии сегмента ST у части больных (до 50%) со стенокардией и нормальными коронарными артериями, но отрицательным ТТФН, что может свидетельствовать о вазомоторных микроциркуляторных нарушениях в генезе болевого синдрома и у этой категории больных, так же как и при классическом синдроме Х.
У больных ИБС, которые перенесли операцию (не на сердце), наличие эпизодов ишемии миокарда в послеоперационном периоде (97% из них безболевые) высоко коррелирует с неблагоприятным исходом вследствие кардиальных осложнений.
Клиническая и прогностическая значимость БИМ при острых коронарных синдромах. Острый коронарный синдром, включающий нестабильную стенокардию и инфаркт миокарда без зубца Q, характеризуется очень высоким риском развития инфаркта миокарда с зубцом Q или смерти. Важным прогностическим признаком при острых коронарных синдромах считается преходящая ишемия миокарда, определяемая по изменению сегмента ST при длительном мониторировании ЭКГ.
Еще в 1986 г. S.O.Gottlieb и соавт. на основании анализа 24-часового ЭКГ-мониторирования у больных, госпитализированных с нестабильной стенокардией, установили, что инфаркт миокарда развивается у 16% пациентов с эпизодами преходящей ишемии, но только у 3% — без них (p=0,005). При этом увеличение времени ишемии >60 минут за 24 часа повышало прогностическую ценность развития коронарных событий, включая процедуры реваскуляризации. A.Rebuzzi и соавт. при обследовании 102 больных с нестабильной стенокардией выявили, что при мультивариационном анализе преходящая ишемия миокарда по данным 24-часового ЭКГ-мониторирования оказалась наиболее сильным предиктором неблагоприятных кардиальных событий. Прогностическая ценность выявляемой при суточном мониторировании ЭКГ депрессии сегмента ST у больных с нестабильной стенокардией увеличивается при одновременном изучении частотных показателей вариабельности ритма сердца.
Подробный анализ особенностей ишемии миокарда у пациентов с острым коронарным синдромом был проведен в исследовании D.J.Patel и соавт. У 256 больных с нестабильной стенокардией или инфарктом миокарда без зубца Q проводилось 48-часовое ЭКГ-мониторирование на фоне максимальной медикаментозной терапии. В течение 10 629 часов мониторирования у 44 пациентов (17,2%) развилось 176 эпизодов преходящей ишемии. Средняя ЧСС в момент развития ишемии составляла 68 ударов в минуту, причем она во время бессимптомной ишемии миокарда достоверно не отличалась от пульса во время болевой ишемии. Более половины эпизодов ишемии миокарда развивалось без предшествующего повышения ЧСС.
Большая часть эпизодов ишемии (64%) развивалась в период с 22 часов до 8 часов. Время возникновения и характер эпизодов ишемии не различались у больных с инфарктом миокарда без зубца Q и нестабильной стенокардией, но при инфаркте миокарда эпизоды ишемии возникали чаще по сравнению с нестабильной стенокардией (27,3% и 15,1% соответственно) и были более длительными (в среднем 20 минут и 13,5 минуты соответственно, p<0,01). Таким образом, при острых коронарных синдромах имеется низкий порог возникновения преходящей ишемии, которая возникает без повышения потребности миокарда в кислороде, чаще в ночной период, а не в утренние часы. Это отличает ишемию миокарда при острых коронарных синдромах от ишемии, возникающей при стабильном течении ИБС.
Прогностическая значимость БИМ при остром инфаркте миокарда и после него. В нескольких исследованиях было показано прогностическое значение БИМ во время ЭКГ-мониторирования перед выпиской из стационара больных, перенесших острый инфаркт миокарда. J.B.Gill и соавт. на основании исследования 406 пациентов установили, что одногодичная летальность составляет 11,6% среди пациентов с признаками преходящей ишемии при 48-часовом ЭКГ-мониторировании и только 3,9% среди пациентов без ишемических эпизодов (p=0,009). Такая же тенденция отмечена и в отношении комбинированной конечной точки смерти или повторного инфаркта: 23,2% и 9,6% соответственно в группе больных с эпизодами ишемии и без них (p=0,001).
При наблюдении более 2 лет за 239 пациентами, перенесшими инфаркт миокарда, было установлено, что среди больных с ишемией миокарда при ЭКГ-мониторировании перед выпиской у 29% отмечены смерть или повторный инфаркт, а среди пациентов без ишемии эти события произошли лишь у 8% (p<0,01). При мультивариационном анализе безболевая ишемия оказалась единственным независимым предиктором повторного инфаркта.
Считается, что безболевая ишемия миокарда как прогностический фактор приобретает дополнительную ценность в подгруппе пациентов высокого риска, включая тех, у кого проведение ТТФН противопоказано, и у больных с низкой сократимостью левого желудочка.
По-видимому, прогностическое значение БИМ снижается по мере увеличения срока после перенесенного инфаркта. A.J.Moss и соавт. изучали роль ТТФН и стресс-теста с оценкой перфузии миокарда с помощью АЭКГМ у 966 больных через 1-6 месяцев после острого инфаркта миокарда и не выявили прогностического значения БИМ по данным АЭКГМ в отношении повторных ишемических событий, а стресс-тест имел только пограничную статистическую значимость в отношении прогноза этих событий.
В исследовании G.Casella и соавт., включавшем 766 больных пациентов со стабильным течением ИБС после инфаркта миокарда (средний срок после инфаркта составлял 2,8+0,75 года), было установлено, что безболевая ишемия во время ТТФН указывала на менее выраженную ишемию миокарда. Так, у пациентов с безболевой ишемией была больше продолжительность выполнения нагрузки, выше ишемический порог и короче период до нормализации сегмента ST по сравнению с пациентами, имеющими болевую ишемию миокарда (p<0,001 для всех показателей). На основании полученных данных авторы приходят к заключению о том, что пациенты со стабильным течением ИБС после перенесенного инфаркта миокарда представляют собой категорию низкого риска, а бессимптомный характер ишемии миокарда у этих больных не является неблагоприятным прогностическим фактором.
Безболевая ишемия миокарда у больных сахарным диабетом. Больные сахарным диабетом имеют достоверно повышенный риск развития коронарного атеросклероза и могут переносить бессимптомный инфаркт миокарда, не сопровождающийся болями в грудной клетке. Исходя из этих предпосылок, можно было бы ожидать более высокую частоту выявления бессимптомной ишемии миокарда у пациентов с ИБС на фоне сахарного диабета по сравнению с больными ИБС, но без диабета.
Бессимптомное течение ИБС у больных сахарным диабетом некоторые авторы объясняют наличием автономной нейропатии с вовлечением афферентных нервов сердца. I.Fearman и соавт. при исследовании сердца 5 больных с сахарным диабетом, умерших от БИМ, установили, что интрамиокардиальные нервы имеют морфологические изменения, характерные для диабетической нейропатии (четкообразное утолщение нервных волокон, их веретенообразное изменение, фрагментация волокон, снижение количества нейронов).
Niakan и соавт. изучали зависимость между наличием периферической нейропатии и частотой развития безболевого инфаркта миокарда у 73 пациентов. Установлено, что у больных с признаками нейропатии БИМ развился в 20% случаев, у больных без признаков автономной дисфункции — только в 4% случаев.
Однако данные о распространенности безболевой ишемии миокарда (по данным ТТФН и АЭКГМ) среди больных с сахарным диабетом и ИБС по сравнению с больными ИБС, но без диабета, неоднозначны. Одни авторы указывают на большую частоту БИМ у больных сахарным диабетом, другие не отмечают достоверных различий в распространенности бессимптомной ишемии миокарда во время ТТФН в зависимости от наличия или отсутствия сахарного диабета.
Попытки ответить на вопрос о распространенности безболевой ишемии миокарда были предприняты с помощью анализа данных уже упоминавшегося выше исследования ACIP. Сравнивали частоту возникновения и характеристики ишемии миокарда во время ТТФН и 48-часового ЭКГ-мониторирования у 77 пациентов с ИБС и сахарным диабетом, контролируемым гипогликемическими препаратами или инсулином, и у 481 пациента с ИБС, но без диабета. Многососудистое поражение коронарных артерий чаще встречалось у больных с сахарным диабетом по сравнению с пациентами без диабета (87% и 74% соответственно, p=0,01). Процент больных без стенокардии во время ТТФН был почти одинаков в группе пациентов с диабетом и без диабета (36% и 39% соответственно). Время до появления депрессии сегмента ST (1 мм) и время до развития приступа стенокардии достоверно не различалось между группами. Доля пациентов, которые имели только бессимптомные депрессии сегмента ST при 48-часовом АЭКГМ, также была почти одинакова в группе пациентов с диабетом и без диабета (94% и 88% соответственно). В то же время в группе больных с диабетом по сравнению с пациентами без диабета отмечены меньшая общая продолжительность ишемии за 24 часа, меньшая средняя продолжительность одного эпизода ишемии, а также меньшая глубина депрессии сегмента ST. Таким образом, исследование ACIP позволило установить одинаковую частоту возникновения бессимптомной ишемии миокарда по данным ТТФН и 48-часовом АЭКГМ у больных с ИБС на фоне сахарного диабета и пациентов с ИБС без диабета, несмотря на более выраженное и диффузное поражение коронарных артерий у первой группы больных.
Некоторые авторы оспаривают правомочность выводов исследования ACIP об отсутствии достоверных различий в распространенности безболевой ишемии миокарда у больных ИБС на фоне сахарного диабета и у больных ИБС без диабета, подчеркивая отсутствие данных о частоте автономной дисфункции среди обследованных пациентов с сахарным диабетом.
Несмотря на теоретические предпосылки, данные о том, что диабетическая автономная нейропатия является основной причиной бессимптомного течения ИБС у многих пациентов с сахарным диабетом, пока не нашли строгих доказательств в клинических или эпидемиологических исследованиях. Большую частоту бессимптомного течения ИБС у пациентов с сахарным диабетом чаще объясняют более высокой распространенностью ИБС среди этих больных и более выраженным коронарным атеросклерозом, при котором возрастает частота выявления ишемии миокарда, включая и бессимптомную.
Лечение
Общей терапевтической стратегией у пациентов с установленным диагнозом ИБС являются изменение факторов риска и использование дезагрегантов. Этот подход рекомендуется применять у всех пациентов, независимо от наличия или отсутствия бессимптомной ишемии.
Получены данные о том, что снижение уровня холестерина плазмы может уменьшить выраженность безболевой ишемии миокарда у больных с доказанной ИБС. В небольшом рандомизированном исследовании, включавшем 40 пациентов с доказанной ИБС и эпизодами депрессии сегмента ST при АЭКГМ, на фоне диеты и терапии ловастатином через 4-6 месяцев отмечено полное исчезновение эпизодов ишемии миокарда у 65% больных, в то время как в контрольной группе только у 10%. Снижение выраженности ишемии в группе лечения по сравнению с контрольной оказалось статистически достоверным (p<0,001). Уменьшение частоты БИМ на фоне терапии статинами связывают с улучшением функции эндотелия.
Методы лечения, непосредственно направленные на уменьшение ишемии миокарда, включают фармакологические (терапия бета-адреноблокаторами, антагонистами кальция и нитратами) и инвазивные методы (ангиопластика коронарных артерий и аортокоронарное шунтирование).
Atenolol Silent Ischemia Study Trial (ASIST) — первое рандомизированное плацебоконтролируемое исследование, в котором была доказана способность бета-адреноблокаторов уменьшать частоту возникновения эпизодов бессимптомной ишемии миокарда и улучшать клинические исходы пациентов. В этом исследовании 306 больных с доказанной ИБС и признаками ишемии миокарда при АЭКГМ рандомизированы в группу лечения атенололом в дозе 100 мг/сут или плацебо. После 4 недель терапии атенололом уменьшились количество эпизодов ишемии (в среднем с 3,6+4,4 до 1,7+4,6; p<0,001) и их продолжительность (с 30+3,3 до 16,4+6,7 минут) по данным 48-часового ЭКГ-мониторирования. Выживаемость без кардиальных событий в группе атенолола оказалась выше по сравнению с группой плацебо (p <0,0066). Наиболее сильным предиктором выживаемости без кардиальных событий оказалось отсутствие ишемии при АЭКГМ через 4 недели от начала лечения.
В исследовании Circadian Anti-ischemia Program in Europe (CAPE) 315 больных со стабильным течением ИБС и наличием более 4 эпизодов ишемии миокарда при 48-часовом ЭКГ-мониторировании рандомизировали в группы приема амлодипина или плацебо. Две трети больных в каждой группе получали бета-адреноблокаторы. По сравнению с плацебо амлодипин достоверно снижал частоту возникновения и продолжительность эпизодов ишемии (p=0,025).
В исследовании Canadian Amlodipine/Atenolol in Silent Ischemia Study (CASIS) у 100 пациентов со стабильным течением ИБС и ишемией миокарда при ТТФН на тредмиле и АЭКГМ сравнивали терапию амлодипином с плацебо, атенололом с плацебо, а также оценивали комбинированную терапию атенололом и амлодипином. Амлодипин был более эффективен для уменьшения ишемии, вызванной физической нагрузкой, в то время как атенолол оказался эффективнее для предупреждения ишемии, выявляемой при АЭКГМ. Комбинированная терапия амлодипином и атенололом оказывала более выраженное антиишемическое действие по сравнению с монотерапией каждым из препаратов.
Исследование Total Ischemic Burden Bisoprolol Study (TIBBS) включало 330 больных со стабильной стенокардией, положительным ТТФН и при наличии более 2 эпизодов ишемии миокарда при суточном ЭКГ-мониторировании. В группу лечения бисопрололом был включен 161 пациент, в группу лечения длительно действующей формой нифедипина — 169 больных. Бисопролол и нифедипин достоверно уменьшали среднее количество эпизодов ишемии. Однако бисопролол оказался эффективнее нифедипина в отношении уменьшения частоты и продолжительности ишемии.
В исследовании Total Ischemic Burden European Trial (TIBET) 682 больных со стабильной стенокардией рандомизированы в группы лечения атенололом, нифедипином или их комбинацией. До рандомизации и на фоне лечения больным проводили ТТФН и АЭКГМ. Уменьшение ишемии было отмечено во всех трех группах. В группе комбинированной терапии степень уменьшения ишемии была выражена больше, чем в каждой их групп монотерапии. Ежегодная частота возникновения первичной конечной точки (смерть или нефатальное сердечно-сосудистое событие) не различалась между двумя группами.
Одним из наиболее значимых исследований бессимптомной ишемии миокарда является Asymptomatic Cardiac Ischemia Pilot (ACIP) study, в котором сравнивали различные стратегии лечения больных с ИБС и БИМ. В исследование были включены 558 больных с ангиографически доказанной ИБС и коронарной анатомией, допускающей реваскуляризацию. Рандомизацию осуществляли в одной из трех групп: 1) лечение стенокардии с титрованием доз антиангинальных препаратов до ее исчезновения (n=183); 2) лечение стенокардии и ишемии под контролем АЭКГМ (n=183); 3) реваскуляризация с помощью ангиопластики или аортокоронарного шунтирования (n=192; из них 49% проведена ангиопластика, 41% — аортокоронарное шунтирование и 10% — без вмешательств). Медикаментозную терапию в первых двух группах проводили атенололом, комбинацией атенолола с нифедипином, дилтиаземом или комбинацией дилтиазема с изосорбидом динитратом. Ишемия миокарда при АЭКГМ через 12 недель от начала лечения не регистрировалась у 39% группы лечения стенокардии, у 41% больных группы лечения стенокардии и ишемии и у 55% группы реваскуляризации. Все три стратегии лечения приводили к уменьшению среднего количества эпизодов ишемии и общей продолжительности периодов депрессии сегмента ST при АЭКГМ. Однако самым важным результатом исследования ACIP считают более благоприятный показатель выживаемости без кардиальных событий в группе реваскуляризации по сравнению с группами медикаментозной терапии через 1 год наблюдения. При этом 65% больных в группе реваскуляризации не нуждались в медикаментозной терапии. Сравнение медикаментозной терапии выявило более эффективное подавление ишемии миокарда в подгруппе лечения атенололом и/или нифедипином по сравнению с подгруппой лечения дилтиаземом и/или изосорбидом динитратом.
Нитраты в виде пероральных или чрескожных форм часто применяют для лечения больных со стабильным течением ИБС. Быстрое развитие толерантности ограничивает эффективность применения длительно действующих нитратов. Для уменьшения толерантности рекомендуется делать 8-12-часовые перерывы в приеме нитратов, но в течение этого периода пациенты остаются без медикаментозной защиты.
S.B.Freeman и соавт. в плацеборандомизированном контролируемом перекрестном исследовании у 52 больных со стабильной стенокардией сравнивали эффективность бета-адреноблокаторов, антагонистов кальция и пластырей с нитроглицерином. Для оценки ишемии миокарда использовали АЭКГМ. В течение одной недели пластыри с нитроглицерином или плацебо накладывали в 8 часов и снимали в 22 часа (период, свободный от нитратов, составлял 10 часов в сутки). В течение последних 48 часов каждого периода проводили ЭКГ-мониторирование для оценки ишемии. Средняя продолжительность ишемии в этот период оказалась одинаковой на фоне активного лечения и плацебо. 88% ишемических эпизодов были бессимптомными. В период, свободный от применения пластыря с нитроглицерином, продолжительность ишемии по сравнению со временем ишемии при применении пластыря без активного препарата увеличивалась соответственно до 46,9+17,9 мин и до 22,5+ 9,2 мин за сутки. Обратная закономерность выявлена в период воздействия пластыря с нитроглицерином или плацебо: эпизоды ишемии продолжались соответственно 27,5+14 мин в сутки и 34,5+11 мин в сутки. Хотя различия в продолжительности ишемии на фоне отмены нитроглицерина или плацебо не достигали статистической значимости, выявленные тенденции указывают на развитие синдрома отмены в виде увеличения периодов ишемии при интермиттирующей терапии трансдермальными формами нитроглицерина.
Увеличение эпизодов ишемии по данным АЭКГМ в период отмены пластырей с нитроглицерином по сравнению с отменой плацебо-пластырей были подтверждены в многоцентровом рандомизированном двойном слепом плацебоконтролируемом перекрестном исследовании Second Transdermal Intermittent Dosing Evaluation Study (TIDES-II), включавшем 72 пациента со стабильной стенокардией. Исследование проводили на фоне терапии бета-блокаторами, антагонистами кальция или их комбинацией. Частота возникновения эпизодов ишемии была ниже после отмены плацебо-пластырей по сравнению с периодом после отмены пластырей с нитроглицерином соответственно, в то время как в период аппликации пластырей частота ишемии была ниже в группе нитроглицерина по сравнению с плацебо соответственно. Действительно, синдром отмены ограничивает эффективность использования длительно действующих нитратов для лечения пациентов с БИМ.
Несмотря на официальную регистрацию метаболического цитопротективного препарата триметазидина для лечения ИБС, до настоящего времени нет доказательств его эффективности при лечении бессимптомной ишемии миокарда. В частности, M.S.Ulgen и соавт., оценивавшие эффективность триметазидина у 64 пациентов, перенесших инфаркт миокарда, не выявили его достоверного влияния на БИМ по данным ЭКГ-мониторирования.
Результаты рандомизированных клинических исследований указывают на важность лечения бессимптомной ишемии миокарда, хотя единая стратегия терапии не выработана. Опубликованные данные основаны на исследованиях относительно небольшого числа больных с доказанной ИБС. Их результаты не могут быть применены у пациентов без четких доказательств поражения коронарных артерий. Лишь небольшую часть пациентов, включенных в исследование, составляли женщины. Также малое число пациентов с ИБС на фоне сахарного диабета. Нет данных о пороговом уменьшении БИМ, при котором возможно улучшение прогноза. В исследовании ACIP даже на фоне реваскуляризации удавалось полностью подавить ишемию только у 55% больных, но прогноз после реваскуляризации через 12 месяцев оказался существенно лучше по сравнению с медикаментозной терапией.
В работах, посвященных оценке лечения пациентов с БИМ, отсутствуют данные об экономической эффективности вмешательств. Хотя общепризнана целесообразность ЭКГ-мониторирования для выявления БИМ и нестабильной стенокардии, вопрос о роли скринингового ЭКГ-мониторирования у больных со стабильным течением ИБС или после процедур реваскуляризации пока не решен.
Появились сообщения о том, что скрининговое исследование с помощью электронно-лучевой компьютерной томографии (ЭЛКТ) среди лиц без клинических проявлений ИБС позволяет выявлять пациентов с высоким риском бессимптомной ишемии миокарда. Преимуществом ЭЛКТ является высокая чувствительность, достигаемая за счет выявления коронарного атеросклероза и выраженности кальциноза коронарных артерий. Эти данные коррелируют с результатами коронароангиографии.
Zuo-Xiang He и соавт. в течение 2,5 года проспективно обследовали 3895 лиц, не имеющих клинических проявлений ИБС. У всех исследуемых проводили ЭЛКТ, а у 411 выполняли стресс-тест с перфузионной томографией миокарда (stress myocardial perfusion tomography) и тредмил стресс-тест. Полученные данные совпадали с показателями шкалы кальциноза коронарных артерий, основанной на результатах ЭЛКТ. Бессимптомная ишемия миокарда выявлена у 22% исследуемых с признаками патологии коронарных артерий по данным ЭЛКТ. Среди лиц со значением шкалы кальциноза коронарных артерий <10 ишемия миокарда не выявлялась, со значением шкалы от 11 до 100 выявлена в 2,6%, от 101 до 399 — в 11,3%, а при значении шкалы около 400 — в 46% случаев (p<0,0001). Показатели шкалы кальциноза коронарных артерий предсказывали риск выявления БИМ независимо от возраста и пола пациентов. Считается, что скрининговое исследование с помощью ЭЛКТ среди бессимптомных лиц с высоким риском ИБС является экономически эффективным.
Итак, бессимптомная ишемия миокарда — распространенный феномен, причины которого изучены недостаточно. Установлено ее высокое прогностическое значение у больных с острым коронарным синдромом и острым крупноочаговым инфарктом миокарда. Во всех других клинических ситуациях данные о роли БИМ в стратификации риска пациентов с ИБС противоречивы и нуждаются в уточнении.
Владимир ОРЛОВ,
заведующий кафедрой клинической
фармакологии и терапии, профессор.
Сергей ГИЛЯРЕВСКИЙ,
Профессор кафедры.
Российская медицинская академия последипломного образования.