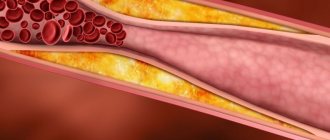
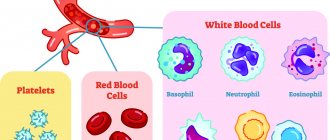
Среди лабораторных приемов, предназначенных для оценки характеристик красных кровяных телец (эритроцитов – Er), не последняя роль принадлежит окраске мазка и его морфологическому исследованию. Хотя до того, пока препарат попадет под объектив микроскопа человек или машина (автоматический гематологический анализатор) произведет подсчет эритроцитов и определит уровень красного пигмента крови – гемоглобина (Hb). Заметив некоторое несоответствие, а именно, снижение уровня гемоглобина в крови при нормальном содержании эритроцитов, врач на основании полученных данных может рассчитать цветовой показатель (ЦП) и в случае его пониженного значения (ниже 0,8), не дожидаясь просмотра мазка, дать однозначный ответ – гипохромия
. Разумеется, для установления диагноза этот ответ не может быть окончательным, зато он станет дополнительным ориентиром при микроскопическом исследовании.
Гипохромия в общем анализе крови (ОАК) указывает на развитие гипохромной (в основном, микроцитарной) анемии.
Однако при подозрении на развитие анемического синдрома в обязательном порядке должны учитываться не только количественные, но и качественные (морфологические) изменения красной крови.
До морфологического исследования
Цветовой показатель (ЦП), характеризующий общее состояние эритроцитов, можно рассчитать по простой и надежной формуле:
ЦП = (Hb, г/л • 3) / три первых значения общего содержания эритроцитов
Возможные результаты и их интерпретация:
- ЦП находится в диапазоне 0,85-1,05 – норма содержания эритроцитов, содержащих достаточное количество гемоглобина.
- ЦП менее 0,8 – гипохромная анемия (гипохромазия), когда количество эритроцитов в норме, но гемоглобина недостаточно.
- ЦП выше 1,1 – гиперхромия (гиперхромазия), свыше 1,4 – имеется дефицит фолиевой кислоты (витамина B12), или пернициозная анемия.
Цветовой показатель – это отношение содержания гемоглобина к эритроцитам, выраженное в цифрах. Дефицит гемоглобина и низкий уровень цветового показателя – признак дефицита железа или сидероахрестической анемии, образующейся из-за нарушения синтеза гемоглобина в эритробластах. Эти состояния относятся к классу гипохромных анемий.
От точности определения уровня Hb и подсчета числа эритроцитов зависит правильный подсчет цветового показателя. Эти критерии определяют наличие или отсутствие анемического синдрома.
Первоисточники повышения значений
Изменения физиологической природы провоцируются:
- сильным эмоциональным стрессом;
- выраженным обезвоживанием;
- длительными спортивными нагрузками;
- проживанием в высокогорных районах.
Патологическая форма эритроцитоза связана:
- с эритремией – опухолевым поражением кроветворных органов;
- пороками сердца – при смешивании артериальной и венозной крови наблюдается недостаточное поступление кислорода к тканям, для компенсации отклонения костный мозг начинает вырабатывать большее число эритроцитов;
- новообразованиями в почках, гипофизе, надпочечниках или печени – органы отвечают за утилизацию старых элементов в крови, формирование болезни приводит к остановке указанной функции, в анализах отмечается преобладание зрелых форм;
- болезнями дыхательных путей и сердца, инфекционными патологиями – наблюдается большое количество молодых или ретикулярных видов элементов;
- первичной легочной гипертензией;
- синдромом Пиквика, вызванного ожирением, легочной недостаточностью, повышенным АД.
К менее опасным источникам развития увеличенного числа эритроцитов относят:
- недостаток пищеварительных ферментов;
- обезвоживание на фоне жары или продолжительных физических нагрузок;
- некачественную воду: с хлором, загрязненную, сильно газированную;
- дефицит витаминов или их недостаток из-за дисфункции печени;
- курение.
На фоне большого количества причин, вызывающих изменение в анализах, только врач может правильно определить первоисточник отклонения.
Качественный и количественный анализ
Подсчет количества эритроцитов, выполненный при помощи гематологического анализатора, малоинформативен. Для получения полной информации используется морфологический или качественный анализ.
Что позволяет сделать это исследование:
- Изучить мазок;
- Определить размер эритроцитов;
- Визуально увидеть степень насыщения эритроцитов гемоглобином.
Морфологические признаки гипохромной анемии:
- Гипохромия;
- Гипохромия и микроцитоз;
- Появление шизоцитов (фрагментов красных кровяных клеток) и нормобластов (молодых клеток);
- Полихроматофилия – состояние, когда в мазке имеются эритроциты, поддающиеся окраске кислыми и щелочными красителями;
- Колебания или отсутствие реакции со стороны белой крови.
Размер клеток, как важный показатель
При отклонении значений ЦП от нормы гематолог анализирует размер красных кровяных клеток:
- Эритроциты нормального размера (нормоциты), имеющие размер 7-8 микрон могут быть при некоторых видах анемий;
- Макроциты (эритроциты с диаметром более 8 мм) – признак анизоцитоза с преобладанием макроцитов;
- Микроциты (эритроциты с диаметром менее 8 мм) – признак микроцитарной анемии.
При появлении отклонений от нормы гематолог изучает материал при помощи кривой Прайс-Джонса.
Интенсивность окрашивания эритроцитов
Важный критерий оценки эритроцитов – интенсивность их окрашивания:
- Нормохромия (нормохромазия), когда эритроциты, насыщенные Hb, выглядят, как нормальные клетки с небольшим светлым пятном посередине клетки, ЦП при этом находится в диапазоне 0,85-1,0. Это состояние не всегда соответствует норме, может наблюдаться при нормохромной анемии.
- Гиперхромия (гиперхромазия), когда срединное просветление не отличается от остальной части эритроцита из-за чрезмерного насыщения пигментами. ЦП при этом более 1,1.
- Гипохромия (гипохромазия), когда срединное просветление чрезмерно велико, а ободок клетки очень узок из-за слабого насыщения красным пигментом. Состояние характеризуется некачественным выполнением эритроцитами своих функций.
Врач, оценив характеристики эритроцитов при проведении морфологического исследования, выявит анемию и отразит диагноз, оформляя заключение.
…их окрашивание
{banner_banstat3}
Между тем, помимо размеров эритроцитов, существует еще один, не менее важный критерий, который дает визуальная оценка – интенсивность окрашивания эритроцитов:
- Красные клетки крови, полноценно (но не чрезмерно!) насыщенные гемоглобином, под микроскопом просматриваются как нормоциты с маленьким просветлением в середине клетки – это нормохромия или нормохромазия
, соответствующая цветовому показателю в пределах 0,85 – 1,0. И опять-таки, нормохромия – не значит отсутствие патологии, пропорциональное уменьшение красных клеток и пигмента крови тоже обозначается как нормохромия, а на самом деле имеет место нормохромная анемия; - Чрезмерное насыщение эритроцитов красным пигментом крови дает излишне интенсивную окраску, стирающую срединное просветление (ЦП – больше 1,1) – гиперхромия или гиперхромазия
; - Большое срединное просветление и узкий ободок (кольцо), очерчивающий клетку, указывает на гипохромию эритроцитов или гипохромазию
(чем больше просветление, тем значительнее степень анемии). Это значит, что эритроциты (их называют анулоцитами) слабо насыщены красным пигментом крови, стало быть, и свои основные функциональные обязанности (доставлять тканям и органам кислород) они будут выполнять некачественно.
Врач лабораторной диагностики, проведя морфологическое исследование эритроцитов и увидев изменения со стороны красных кровяных телец (а это случится наверняка, если большинство клеток по каким-либо причинам изменило свои характеристики – размер и окраску), заподозрит развитие анемического состояния, что отразит в своем заключении. Однако тема данной работы – гипохромия,вот к ней и вернемся…
Степени гипохромии
Градация гипохромной анемии:
- 1 степень – ободок клеток окрашен, зона просветления больше, чем обычно;
- 2 степень – центральное просветление шире, чем обычно, приближается к мембране, окрашенная зона четкая;
- 3 степень – окрашена лишь зона у мембраны, эритроцит похож визуально на бледное кольцо. Проявляется при тяжелой анемии, в очень запущенных стадиях.
Очень часто гипохромию сопровождает микроцитоз, эти симптомы – признаки гипохромных анемий. Они приобретают еще большее значение, если требуется различить микроцитарные анемии друг от друга или дифференцировать их от других патологий крови.
Достоверный признак гипохромных анемий
Различают следующие формы анемических состояний, входящие в группу гипохромных анемий:
- Железодефицитная анемия.
Самая распространенная форма гипохромных анемий.
Характерные признаки:
- Микроцитоз в сочетании с гипохромией;
- Цветовой показатель ниже нормы;
- Сниженный уровень сывороточного железа;
- Положительная динамика лечения.
- Железонасыщенная анемия (сидероахрестическая).
Уровень Hb при этой патологии неуклонно снижается из-за неэффективного всасывания железа к месту синтеза гемоглобина. Возникает по причине интоксикации промышленными ядами, химикатами, побочного действия лекарственных препаратов, влияющих на образование красных кровяных телец.
Характерные признаки:
- Низкий Hb;
- Гипохромия;
- Нормальный уровень железа;
- Отсутствие эффекта от использования препаратов с повышенным содержанием железа.
- Железоперераспределительная анемия.
В основе этиологии этой формы анемии лежит чрезмерный гемолиз эритроцитов, туберкулез, гнойные процессы, сердечные патологии. Относится к гипохромным микроцитарным анемиям.
Характерные признаки:
- Низкий Уровень Hb;
- Гипохромия;
- Уровень сывороточного железа в норме;
- Отсутствие эффекта от терапии препаратами железа.
При сочетании признаков разных видов диагностируют смешанную форму гемохроматоза.
Особенности классификации
Выделяется два типа эритроцитоза:
- Первичный наследственный – относится к генетическим патологиям, встречается редко. Источником развития болезни является низкая восприимчивость кислородных рецепторов в почках, повышенные значения эритропоэтина. Признаком заболевания считается выраженный упадок сил, приступы головокружения, изменение стандартного оттенка кожного и слизистого покрова в багровые оттенки, сниженную свертываемость крови.
- Вторичный или приобретенный – провоцируется кислородным голоданием клеток, возникает на фоне новообразований в печени, почках, дыхательных органах.
При игнорировании первичной формы патологии существует риск формирования сосудистых осложнений, включая тромбообразование. Проблема связана с изменениями скорости свертывания крови.
Причины гипохромии
В основе этиологии гипохромии лежит гипохромная анемия.
Факторы риска, способствующие развитию гипохромии и анемии:
- Длительные или хронические кровопотери (ЖКТ, матка);
- Хронические воспалительные процессы (энтерит, резекция органов), приводящие к нарушению всасыванию железа в желудочно-кишечном тракте;
- Злокачественные опухоли ЖКТ (рак желудка);
- Повышенная потребность в железе, витаминах и микроэлементах во время беременности, лактации, усиленного роста детей и подростков;
- Нехватка железа и витаминов, помогающих его усваивать из-за резкого уменьшения поступления продуктов питания в организм (при вегетарианстве или соблюдении диеты).
Клинические признаки анемии в зависимости от степени тяжести и уровня гемоглобина:
- 1 степень (легкая) – уровень Hb ниже нормы, но не опускается менее 90 г/л;
- 2 степень (умеренная) — уровень Hb в диапазоне 70-90 г/л, ЦП ниже 0,8, при визуальной оценке мазка отмечается умеренная гипохромия;
- 3 степень (тяжелая) — уровень Hb ниже 70 г/л, ЦП снижен, при визуальной оценке мазка отмечается выраженная гипохромия.
Чем меньше степень анемии, тем слабее выражены ее проявления.
Железодефицитная анемия у детей
Почему при ЖДА необходимы препараты железа? В чем преимущества препаратов последнего поколения? Почему прием препаратов железа должен быть длительным?
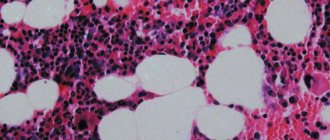
| Картина крови при хронической железодефицитной анемии. Выраженные гипохромия эритроцитов, анизоцитоз, пойкилозитоз, шизоцилы, присутствие полихроматофилов |
Анемия — это патологическое состояние, характеризующееся снижением массы эритроцитов, часто в сочетании с уменьшением количества эритроцитов в единице объема крови. Причин возникновения анемий очень много; для детского же возраста наиболее типична железодефицитная анемия (ЖДА). ЖДА характеризуется наличием небольших гипохромных эритроцитов и истощением запасов железа в организме.
Распространенность дефицита железа у детей в раннем возрасте, по данным ВОЗ, составляет от 17,5 до 30%.
Можно выделить следующие причины развития дефицита железа у детей.
- Недостаточные запасы железа при рождении. Недоношенные дети, а также дети от матерей, страдавших во время беременности анемией, относятся к группе риска по развитию ЖДА. Состояние плаценты также имеет огромное значение, поскольку положительный баланс железа у плода обусловлен совершенными транспортными механизмами плаценты.
- Недостаточное поступление железа с пищей и нарушение всасывания в желудочно-кишечном тракте. Имеет значение не cтолько содержание железа в продукте, сколько эффективность его всасывания и усвоения. Железо всасывается в двенадцатиперстной и тощей кишках, поэтому при различных заболеваниях пищеварительного тракта (хронический энтерит, синдром мальабсорбции) также может развиваться дефицит железа в силу нарушения его всасывания.
- Повышенная потребность в железе в связи с ростом, интенсивными процессами дифференцировки тканей, созревания различных органов и систем, увеличением объема циркулирующей крови. Особенно высока потребность в железе в период вытяжения, пубертатный период и во время становления менструальной функции у девочек-подростков.
- Избыточная потеря железа организмом. Это прежде всего кровопотеря: кровотечения различной локализации (при заболеваниях пищеварительного тракта — язвенные процессы, полипы, сосудистые аномалии, носовые), глистная инвазия, менструации у девочек-подростков. Избыточная потеря железа может быть при выраженных аллергических проявлениях на коже за счет потери микроэлемента со слущивающимся эпителием, при частых ОРВИ у детей, поскольку вирусы и бактерии используют железо ребенка для своих метаболических процессов.
Важно отметить, что у детей раннего возраста причинами дефицита железа, как правило, являются недостаточное депо железа и нерациональное питание, а у детей старшего возраста — кровопотеря и резкое вытяжение.
Патофизиологические аспекты
Поскольку всасывание железа ограничено, у большинства людей его поступление с пищей едва покрывает текущую потребность организма, в результате заболеваний или неправильного питания довольно легко развивается дефицит железа. Этот процесс состоит из нескольких стадий.
Стадия 1. Потеря железа превышает его поступление. На фоне отрицательного баланса железа его запасы в костном мозге постепенно истощаются. Хотя уровень железа в сыворотке и количество гемоглобина остаются нормальными, содержание ферритина в сыворотке уменьшается (ниже 20 нг/мл). По мере истощения запасов железа происходит компенсаторное повышение концентрации трансферрина (о чем свидетельствует увеличение железосвязывающей способности).
Стадия 2. Истощенные запасы железа уже не обеспечивают эритропоэтическую функцию костного мозга. В то время как уровень трансферрина в плазме растет, содержание железа в сыворотке снижается, что приводит к его всевозрастающей нехватке при образовании эритроцитов. Эритропоэз нарушается, когда уровень железа ниже 50 мкг%, а насыщение трансферрина — ниже 16%. Возрастает концентрация рецепторов ферритина в сыворотке (более 8,5 мг/л).
Стадия 3. Анемия при внешне нормальных эритроцитах и эритроцитарных индексах.
Стадия 4. Развитие микроцитоза и затем гипохромии.
Стадия 5. Дефицит железа сопровождается симптомами тканевых нарушений.
Клинические проявления
Представление о клиническом статусе больного с анемией зависит от основного заболевания и формы анемии (острой или хронической). ЖДА — состояние хроническое. Проявление анемии per se объясняют с помощью патофизиологических механизмов. Большинство симптомов ЖДА являются отражением сердечно-сосудистых и газообменных изменений, компенсирующих уменьшение массы эритроцитов. Степень выраженности симптомов зависит от скорости развития анемии (при медленном развитии анемии, характерном для железодефицитных состояний, времени для полного развития компенсаторных механизмов достаточно) и ее длительности. Даже анемия средней тяжести нередко протекает бессимптомно. Ребенок может жаловаться на усталость, одышку и сердцебиение, особенно после физической нагрузки. При тяжелой анемии симптоматика сохраняется и в состоянии покоя, больной не может переносить физические нагрузки. Если уровень гемоглобина менее 75 г/л, то минутный сердечный выброс в покое заметно повышается по мере увеличения как частоты сердечных сокращений, так и ударного объема. Симптомы сердечной недостаточности развиваются, когда резерв миокарда исчерпан. Следовательно, тяжесть состояния больного определяется прежде всего степенью выраженности сердечно-сосудистых нарушений.
Симптоматика при анемии средней и тяжелой степени распространяется и на другие системы органов. Больной часто жалуется на головокружение и головные боли, шум в ушах, возможен даже обморок. Человек становится раздражительным, нарушается сон, снижается концентрация внимания. Поскольку кровоток в коже снижен, может развиваться гиперчувствительность к холоду. Возникает симптоматика и со стороны желудочно-кишечного тракта — резкое снижение аппетита, диспепсические расстройства (тошнота, изменение характера и частоты стула), прежде всего это происходит за счет шунтирования крови, минующей сосудистое русло внутренних органов. У девочек-подростков нарушается менструальный цикл, что проявляется в виде аменореи или обильного кровотечения.
Основной признак анемии — бледность кожных покровов. Однако его информативность ограничена другими факторами, определяющими цвет кожи.
Поэтому наиболее информативным признаком анемии является бледность видимых слизистых — слизистой оболочки полости рта, ногтевого ложа и конъюнктивы век. Информативным также считается цвет кожи на сгибах ладонной поверхности — если по цвету они не отличаются от окружающей кожи, то уровень гемоглобина у больного, как правило, менее 80 г/л.
Развитие бледности кожных покровов при анемии объясняется двумя факторами: первый — это, несомненно, уменьшение уровня гемоглобина в крови, второй — шунтирование крови в обход сосудов кожи и других периферических тканей, способствующее усиленному кровоснабжению жизненно важных органов. Перераспределение кровотока представляет собой один из важных механизмов компенсации анемии.
Из других клинических симптомов анемии следует отметить уже упоминавшиеся выше тахикардию, значительные колебания пульсового давления, систолический шум изгнания над предсердиями, снижение умственной и физической активности, дети становятся раздражительными, быстро утомляются, их сон беспокойный, аппетит снижен.
При ЖДА к обычным симптомам анемии присоединяются признаки, специфичные для недостаточности железа. При длительном дефиците железа появляются извращенные аппетит (поедание мела, грязи, красок) и обоняние (нравятся резкие запахи бензина, красок, лаков, поедание льда (пагофагия), развиваются глосситы, хейлит, койлонихия (истонченные, исчерченные, ломкие ногти). При дефиците железа падает активность иммунной системы за счет снижения синтеза ИЛ-2, Т-киллеров; дети чаще болеют ОРВИ, что, в свою очередь, усугубляет имеющийся дефицит железа.
Диагноз подтверждается лабораторными данными. Критерием диагностики ЖДА является анемия микроцитарная, гипохромная, норморегенераторная. Для ЖДА характерны анизоцитоз, тромбоцитоз, снижение уровня сывороточного железа (менее 13 ммоль/л), общая железосвязывающая способность сыворотки не изменена или повышена, уровень сывороточного ферритина менее 15 нг/мл, насыщение трансферрина меньше 16%, уровень протопорфирина эритроцитов повышен, уровень Hb A2 снижен, в костном мозге отмечается раздражение красного ростка (эритроциты : гранулоциты = 1:1 — 1:2), типично отсутствие в костном мозге запасов железа и кольцевидных сидеробластов.
В дифференциально-диагностический поиск включаются талассемия, отравление свинцом, анемия при хронических заболеваниях, врожденные нарушения обмена железа (дефицит трансферрина, нарушение утилизации железа, нарушение реутилизации железа), гемосидероз, в том числе синдром Гудпасчера, дефицит меди.
Принципы лечения ЖДА у детей
- Устранение причин, лежащих в основе развития дефицита железа.
- Терапия ЖДА должна проводиться препаратами железа, поскольку возместить дефицит железа при этом состоянии только диетотерапией невозможно, истинный дефицит железа не сопровождается дефицитом витаминов В12, В6, фолиевой кислоты.
- Цель терапии препаратами железа — устранение дефицита железа в организме, а не просто нормализация уровня гемоглобина, поэтому срок лечения длительный (не менее 3 месяцев).
- Терапия ЖДА проводится преимущественно пероральными препаратами железа.
- Гемотрансфузии при ЖДА проводятся только по жизненным показаниям.
Диетотерапия при ЖДА у детей
В настоящее время общепризнано, что устранить дефицит железа в организме только с помощью диетотерапии невозможно. Это связано с тем, что всасывание железа из пищевых продуктов ограничено — 1,8-2 мг (не более 2,5 мг) железа в сутки — даже при рациональном питании, соответствующем возрасту, и при потреблении достаточного количества продуктов с высоким содержанием железа. (Для сравнения: здоровый ребенок в зависимости от возраста теряет за сутки от 0,15 до 0,6 мг железа, девочка во время месячных — 15-50 мг) При приеме современных препаратов железа оно усваивается в 20 раз лучше. Диетотерапия должна быть одной из составляющих терапии ЖДА у детей.
С другой стороны, очень важно ориентироваться не на содержание железа в продуктах питания, а на его форму. Именно форма железа определяет процент его всасывания и усвоения и, следовательно, эффективность терапии. Из различных форм железа легче всего усваивается гемовое железо — сложное органическое соединение, в котором железо находится в составе гемоглобина; неорганические соединения — соли железа — усваиваются организмом значительно хуже. Железо в составе гема активно захватывается клетками слизистой кишечника и всасывается в неизмененном виде. Процессы всасывания гема в кишечнике не зависят от кислотности среды и активности пищевых ферментов. Железо из злаков, овощей, фруктов всасывается значительно хуже из-за присутствия в них ингибиторов ферроабсорбции, таких, как оксалаты, фосфаты, танин и другие. Сравните: коэффициент усвояемости железа из говядины (гемовое железо) составляет 17-22%, из фруктов — не более 3%. Степень усвояемости железа из продуктов животного происхождения также зависит от формы железосодержащих соединений. Так, из печени, где соединения железа представлены в виде ферритина и трансферрина, железо усваивается в значительно меньшем количестве, чем из мясных продуктов, хотя общее содержание железа в печени в 3 раза больше, чем в мясе. Поэтому включение печени в рацион питания для устранения дефицита железа или с профилактической целью не имеет никакого смысла. Таким образом, рацион питания должен быть максимально богат продуктами, в которых железо содержится в виде гема (язык говяжий, мясо кролика, говядина).
Необходимо отметить также, что мясо, печень и рыба улучшают всасывание железа из фруктов и овощей при одновременном их употреблении.
Всасываемость железа из злаковых, бобовых, клубневых, овощей, фруктов значительно ниже, поскольку железо в них содержится в негемовой форме, и во многом зависит от содержания в рационе веществ, ингибирующих или потенцирующих всасывание железа. Усиливают всасывание негемового железа аскорбиновая кислота, продукты из мяса, птицы, рыбы, а также вещества, понижающие кислотность пищи (например, молочная кислота). Снижают усвоение негемового железа соевый протеин, полифенолы, входящие в состав чая, кофе, орехов и бобовых. Несмотря на высокое содержание железа в некоторых продуктах растительного происхождения, они не могут обеспечить высокую потребность в железе, характерную для растущего организма, поскольку железо из них всасывается значительно хуже, чем из продуктов животного происхождения. Рекомендации употреблять в больших количествах фруктовые соки, яблоки, гранаты, гречневую крупу и другие продукты в целях восполнения депо железа при ЖДА также нельзя считать обоснованными. Сбалансированная по основным ингредиентам диета позволяет «покрыть» только физиологическую потребность организма ребенка в железе, но никак не устраняет дефицита железа и должна использоваться в комплексе с препаратами железа при лечении ЖДА. Однако полноценная и сбалансированная диета занимает важное место в профилактике развития дефицита железа в организме ребенка во все периоды детства.
Медикаментозная терапия при ЖДА
Основной задачей терапии ЖДА является устранение дефицита железа в организме ребенка. Это достигается благодаря приему железосодержащих лекарственных препаратов. Основные требования, предъявляемые к препаратам железа, — это достаточное содержание в них элементарного железа и отсутствие побочных эффектов и осложнений. В настоящее время на фармацевтическом рынке России достаточный выбор препаратов железа, что расширяет возможности врача и позволяет учитывать индивидуальные особенности пациентов при назначении лечения (табл. 1). В частности, появились удобные формы для детей младшего возраста — капли и сироп (феррум лек, мальтофер, актиферрин, гемофер).
Все препараты зарегистрированы и разрешены к применению в Российской Федерации.
Современные препараты железа разделяют на две группы:
- ионные железосодержащие препараты (солевые, полисахаридные соединения железа);
- неионные соединения, т. е. препараты, представленные гидроксид-полимальтозным комплексом трехвалентного железа (феррум лек, мальтофер).
Усвояемость железа из лекарственного препарата зависит от содержания в нем элементарного (активного) железа. Наибольшее количество элементарного железа содержится в препаратах, в которых железо представлено в виде фумарата (ферретаб, ферронат) или сульфата двухвалентного железа (актиферрин, ферро-фольгамма, гемофер пролангатум, ферро-градумет). В настоящее время появились препараты железа нового поколения, к которым относятся лекарственные средства, представленные гидроксид-полимальтозным комплексом трехвалентного железа (мальтофер, феррум лек). Особенностью этих препаратов является то, что поступление железа из кишечника в кровь происходит путем активного всасывания в отличие от солевых соединений железа, всасывание которых происходит по градиенту концентрации. Это важно, поскольку исключается возможность передозировки препаратов железа, содержащих гидроксид-полимальтозный комплекс трехвалентного железа.
Солевые препараты железа в просвете кишечника взаимодействуют с компонентами пищи и с другими лекарствами, что затрудняет абсорбцию железа. Поэтому эта группа препаратов железа назначается за час до еды. Однако на фоне выраженного свободнорадикального стресса, возникающего при взаимодействии железа со слизистой кишечника во время его диффузии, усиливается повреждающее действие на слизистую кишечника соединений железа, что проявляется диспепсическими расстройствами, вплоть до некроза слизистой. При плохой переносимости солевых препаратов железа их можно принимать и во время еды, что уменьшит побочные проявления, но и всасывание железа в свою очередь будет ухудшаться. Солевые препараты железа нельзя запивать чаем, молоком и сочетать их с приемом некоторых медикаментов (тетрациклинов, левомицетина, препаратов кальция, антацидов, пеницилламина), поскольку при этом снижается усвояемость железа.
Препараты неионного железа, как показывают проведенные исследования, не взаимодействуют с компонентами пищи и лекарствами, что позволяет использовать эти препараты, не нарушая режима питания детей (препараты можно добавлять в пищу, соки) и схемы терапии сопутствующей патологии (если есть необходимость в проведении такого лечения).
Суточная терапевтическая доза препаратов железа должна быть достаточной для нормализации уровня гемоглобина и восполнения запасов железа в костном мозге, что составляет для солевых препаратов железа 3-6 мг/кг/сут элементарного железа в два-три приема. Гидроксид-полимальтозный комплекс железа (феррум лек) назначается в дозе 3-6 мг/кг/сут в один или несколько (по желанию пациента) приемов.
Побочные реакции при приеме препаратов железа
Наиболее часто при лечении ферропрепаратами наблюдаются следующие побочные явления (табл. 2): металлический привкус во рту, потемнение эмали зубов, аллергические высыпания на коже, диспепсические нарушения в результате раздражающего действия на слизистую пищеварительного тракта, прежде всего кишечника (жидкий стул, тошнота, рвота). Поэтому начальные дозы препаратов должны составлять 1/2-1/3 терапевтической с последующим увеличением их до полной дозы в течение нескольких дней во избежание возникновения выраженных побочных действий. При непереносимости солевого препарата его можно заменить гидроксид-полимальтозным комплексом железа, в результате применения которого не возникает вышеописанных эффектов. Гидроксид-полимальтозный комплекс железа можно сразу применять в полной дозе. Неионные препараты железа не вызывают перечисленных выше побочных эффектов, чувство переполнения желудка также отмечается редко.
Парентеральное введение препаратов железа
Парентеральное введение препаратов железа проводится только по строгим показаниям из-за развития выраженных местных и системных побочных эффектов. Показания таковы: патология пищеварительного тракта (синдром нарушенного кишечного всасывания, неспецифический язвенный колит, хронический энтероколит, желудочно-кишечное кровотечение) и непереносимость железосодержащих препаратов при пероральном приеме.
Противопоказаниями к назначению препаратов железа являются анемии, не обусловленные дефицитом железа (гемолитические, апластические), гемосидероз, гемохроматоз.
Продолжительность курса лечения
Клинический и терапевтический эффекты при пероральной ферротерапии развиваются постепенно. Через некоторое время появляется клиническое улучшение: уменьшается слабость, исчезает головокружение, ребенок становится более активным, повышается аппетит, постепенно розовеют кожные покровы и видимые слизистые. На 8-10-й день терапии отмечается ретикулоцитарный криз — до 5%, что подтверждает эффективность лечения. Позже наблюдается повышение уровня гемоглобина, чаще всего нормализация гемоглобина происходит на 3-6-й неделе от начала терапии и зависит от степени тяжести анемии. В среднем уровень Hb повышается на 10 г/л за 10 дней. Однако нормализация уровня гемоглобина не является признаком устранения дефицита железа. Для полного восполнения депо железа в организме курс ферротерапии должен составлять не менее 3 месяцев.
Причины неэффективности ферротерапии
Неэффективность терапии на фоне приема препаратов железа при их хорошей переносимости может быть обусловлена следующими факторами:
- неправильный диагноз,
- продолжающаяся кровопотеря,
- интеркуррентные заболевания (ОРВИ, обострение хронических очагов инфекции).
ЖДА — это заболевание, при правильной терапии которого наступает полное выздоровление!