Анатомические данные о сердце как органе
Уже более 30-ти лет существует так называемый аппарат искусственного кровообращения, который кратковременно, но может заменить насосную функцию сердца, хотя, конечно, в полной мере его заменить никак не получается. И этот факт заставляет нас беспокоиться за мотор организма, ибо без него жить не получится.
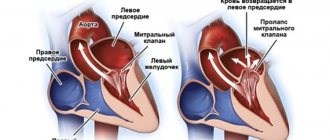
Для млекопитающих отряда приматов, к коим относится человек, характерно 4-х камерное сердце, т.е. оно состоит из 4 камер — 2 желудочка (левый и правый), и 2 предсердия (также левый и правый). Правые отделы сердца отвечают за перекачку крови по так называемому «малому» кругу кровообращения, т.е. сердце — легкие (в которых кровь обогащается кислородом); а из левых отделов кровь поступает в «большой круг», т.е. левое предсердие — левый желудочек — организм.
Правое предсердие сообщается с правым желудочком с помощью трикуспидального (трехстворчатого) клапана, а левое предсердие с левым желудочком сообщается через митральный (двухстворчатый) клапан, о поражении которого и пойдет речь в данной статье.
Структурных изменений:
- Гипертрофическая кардиомиопатия.
- Разрыв сухожильных хорд (вторичный в следствии митрального пролапса, инфаркта миокарда, травим или эндокардита или спонтанный).
- Дилатация фиброзного кольца клапана и полости левого желудочка (аневризматическая дилатация левого желудочка или при кардиомиопатии).
- Дисфункция или разрыв папиллярных мышц (в результате инфаркта миокарда или ИБС (ишемическая болезнь сердца)).
- Парапротезная фистула, возникшая в результате прорезывания швов.
Причины заболевания
Миксоматозная дегенерация митрального клапана
Точная причина миксоматозной дегенерации митрального клапана не известна, часто данную патологию связывают с наследственной предрасположенностью. Наиболее часто данному заболеванию подвержены люди, у которых нарушено образование хрящевой ткани, имеются врожденные дефекты и заболевания суставов.
Дегенерация митрального клапана (миксоматоз митрального клапана) в последние годы ученые связывают с гормональными нарушениями различного генеза. Также есть определенная связь между данной патологией и различными вирусными заболеваниями, которые оказывают повреждающее действие на створки сердца, а также стрептококковой инфекцией, которая вызывает прямое повреждение не только клапанного аппарата, но и эндокарда сердца.
Повреждения кольца митрального клапана:
- В результате образования абсцесса в следствии инфекционного эндокардита.
- Травм, чаще при оперативном вмешательстве на клапане.
- Инфекционного эндокардита или в результате прорезывания швов образование парапротезной фистулы.
- Повреждение створок клапана:
- Разрушение или перфорация створок в следствии инфекционного эндокардита.
- Мискома предсердия.
- Травмы.
- Либмана-Сакса повреждение при системной красной волчанке.
Патогенез развития болезни
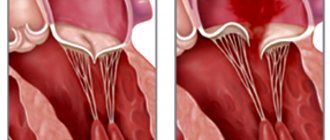
Утолщение створок митрального клапана
Растяжение и утолщение створок митрального клапана вызывает нарушение смыкания последних, что способствует (из-за более высокого давления в левом желудочке, чем в левом предсердии) обратному забросу крови в полость левого предсердия. Это в свою очередь вызывает гиперфункцию с последующей гипертрофией левого предсердия и относительной недостаточностью клапанов легочных вен, а в последующем и гипертензией в малом круге кровообращения, что и обуславливает большинство симптомов данного заболевания.
В зависимости от толщины створок клапана выделяют следующие стадии заболевания:
I степень — створки утолщены до 3-5 миллиметров, при этом смыкание клапана не нарушено, поэтому клинических проявлений у пациента нет, из-за этого выявить заболевание на данной стадии возможно только при обследовании заболеваний других систем или на профилактических осмотрах.
Какое-либо специальное лечение миксоматоз митрального клапана I степени не требует, даже ограничений по физической нагрузке не дается, главное вести здоровый образ жизни, стараться не болеть различными вирусными и стрептококковой инфекциями и периодически проводить профилактические осмотры (чаще всего рекомендуют 2 раза в год).
Дегенеративное заболевание митрального клапана
II степень — утолщение створок достигает 5-8 миллиметров, смыкание клапана нарушено, наблюдается обратный заброс крови. Также при обследовании обнаруживаются единичные отрывы хорды и деформация контура митрального клапана. При данной стадии, врач расписывает образ жизни, питание и частоту профилактических осмотров.
III степень — утолщение створок превышает 8 миллиметров, смыкание клапана не происходит, наблюдаются полные отрывы хорды. При этом состояние пациента резко ухудшается, возникают симптомы острой левожелудочковой недостаточности, поэтому нужно экстренное специализированное лечение данного пациента и в эту стадию очень важно раннее обращение за медицинской помощью.
Пролапс митрального клапана — норма или патология?
П
од термином пролапс митрального клапана (ПМК) понимают
провисание одной или обеих створок митрального клапана в полость левого предсердия в систолу
. Данный феномен описан относительно недавно – только во второй половине 60–х годов, когда появился метод эхокардиографии. Тогда было замечено, что у лиц со среднесистолическим щелчком и систолическим шумом в I точке аускультации при эхокардиографии створка(–и) митрального клапана в систолу провисает в полость левого предсердия.
В настоящее время различают первичный (идиопатический) и вторичный ПМК. Причинами вторичного ПМК
являются ревматизм, травма грудной клетки, острый инфаркт миокарда и некоторые другие заболевания. Во всех данных случаях происходит отрыв хорд митрального клапана, вследствие чего створка начинает провисать в полость предсердия. У больных с ревматизмом из–за воспалительных изменений, затрагивающих не только створки, но и прикрепляющиеся к ним хорды, чаще всего отмечен отрыв мелких хорд 2 и 3–го порядка. Согласно современным воззрениям, для того чтобы убедительно подтвердить ревматическую этиологию ПМК, необходимо показать, что у больного данный феномен отсутствовал до дебюта ревматизма и возник в процессе болезни. Однако в клинической практике сделать это весьма затруднительно. В то же время у больных с недостаточностью митрального клапана, направленных на кардиохирургическое лечение, даже без четкого указания на ревматизм в анамнезе, примерно в половине случаев при морфологическом исследовании створок митрального клапана находят воспалительные изменения как самих створок, так и хорд.
Травма грудной клетки
является причиной острого отрыва хорд и развития тяжелой митральной недостаточности с клинической картиной острой левожелудочковой недостаточности. Нередко это является причиной смерти таких пациентов.
Острый задний инфаркт миокарда
, затрагивающий заднюю папиллярную мышцу, также приводит к отрыву хорд и развитию пролапса задней створки митрального клапана.
Популяционная частота ПМК, по данным разных авторов (от 1,8 до 38%), существенно колеблется в зависимости от используемых критериев диагностики, однако большинство авторов считают, что она составляет 10–15%. При этом на долю вторичного ПМК приходится не более 5% всех случаев. Распространенность ПМК существенно колеблется с возрастом – после 40 лет число лиц с данным феноменом резко уменьшается и в возрастной популяции старше 50 лет составляет всего 1–3%. Поэтому ПМК – это патология лиц молодого трудоспособного возраста
.
У лиц с ПМК по результатам многих исследователей установлена повышенная частота развития серьезных осложнений:
внезапная смерть, жизненно опасные нарушения ритма, бактериальный эндокардит, инсульт, тяжелая недостаточность митрального клапана. Их частота невелика – до 5%, однако учитывая, что эти пациенты работоспособного, призывного и детородного возраста, проблема выделения среди огромного числа лиц с ПМК подгруппы больных с повышенным риском развития осложнений становится крайне актуальной.
Идиопатический (первичный) ПМК
в настоящее время является самой распространенной патологией клапанного аппарата сердца. По мнению абсолютного большинства авторов, основой патогенеза идиопатического ПМК являются генетически детерминированные нарушения различных компонентов соединительной ткани, что приводит к «слабости» соединительной ткани створок митрального клапана и поэтому их пролабированию в полость предсердия под давлением крови в систолу. Поскольку центральным патогенетическим звеном в развитии ПМК считают дисплазию соединительной ткани, то у этих пациентов должны быть признаки поражения соединительной ткани и со стороны других систем, а не только сердца. Действительно, многие авторы описали комплекс изменений соединительной ткани разных систем органов у лиц с ПМК. По нашим данным, у этих пациентов достоверно чаще по сравнению с лицами без ПМК выявляются астенический тип конституции, повышенная растяжимость кожи (более 3 см над наружными концами ключиц), воронкообразная деформация грудной клетки, сколиоз, плоскостопие (продольное и поперечное), миопия, повышенная гипермобильность суставов (3 и более суставов), варикозное расширение вен (в том числе варикоцеле у мужчин), положительные признаки большого пальца (возможность вывести дистальную фалангу большого пальца за ульнарный край ладони) и запястья (первый и пятый пальцы перекрещиваются при обхвате запястья противоположной руки). Поскольку эти признаки выявляются при общем осмотре, их называют фенотипическими признаками дисплазии соединительной ткани. При этом у лиц с ПМК одновременно выявляется не менее 3–х из перечисленных признаков (чаше 5–6 и даже более). Поэтому для выявления ПМК мы рекомендуем направлять на эхокардиографию лиц с одновременным наличием 3–х и более фенотипических признаков дисплазии соединительной ткани.
Нами проводилось морфологическое исследование биоптатов кожи у лиц с ПМК при помощи светооптического исследования (гистологические и гистохимические методы). Выделен комплекс морфологических признаков патологии кожи – дистрофия эпидермиса, истончение и сглаженность сосочкового слоя, деструкция и дезорганизация коллагеновых и эластических волокон, изменение биосинтетической активности фибробластов и патология сосудов микроциркуляторного русла и некоторые другие. При этом в биоптатах кожи лиц контрольной группы (без ПМК) подобных изменений обнаружено не было. Выявленные признаки свидетельствуют о наличии у лиц с ПМК дисплазии соединительной ткани кожи, а следовательно, о генерализации процесса «слабости» соединительной ткани.
Клиническая картина
Клиническая картина при ПМК весьма многообразна и может быть условно поделена на 4 больших синдрома
– вегетативной дистонии, сосудистых нарушений, геморрагический и психопатологический.
Синдром вегетативной дистонии
(СВД) включает в себя боли в левой половине грудной клетки (колющие, ноющие, без связи с физической нагрузкой, длительностью либо несколько секунд для колющих болей, либо часами для ноющих), гипервентиляционный синдром (центральный симптом – чувство нехватки воздуха, желание сделать глубокий, полноценный вдох), нарушение вегетативной регуляции деятельности сердца (жалобы на сердцебиение, чувство редкого биения сердца, ощущение неровного биения, «замирания» сердца), нарушения терморегуляции (ощущение «познабливания», длительно сохраняющийся субфебрилитет после инфекций), расстройства со стороны желудочно–кишечного тракта (синдром «раздраженного кишечника», функциональные желудочные диспепсии и др.), психогенную дизурию (частое или, напротив, редкое мочеиспускание в ответ на психоэмоциональную нагрузку), повышенную потливость. Естественно, в такой ситуации должны быть исключены все возможные органические причины, которые могут вызывать сходную симптоматику.
Синдром сосудистых нарушений
включает синкопальные состояния – вазовагальные (обмороки в душных помещениях, при длительном стоянии и др.), ортостатические, а также предобморочные состояния в тех же условиях, мигрени, ощущение ползанья мурашек в ногах, холодные на ощупь дистальные отделы конечностей, утренние и ночные головные боли (в основе которых лежит венозный застой), головокружения, идиопатические пастозность или отечность. В настоящее время гипотеза об аритмогенной природе синкоп при ПМК не нашла подтверждений, и их рассматривают, как вазовагальные (т.е. нарушение вегетативной регуляции сосудистого тонуса).
Геморрагический синдром
объединяет жалобы на легкое образование синяков, частые носовые кровотечения и кровотечения из десен, обильные и/или длительные менструации у женщин. Патогенез этих изменений сложен и включает нарушение коллаген–индуцированной агрегации тромбоцитов (вследствие патологии коллагена у этих пациентов) и/или тромбоцитопатий, а также патологию сосудов по типу васкулита. У лиц с ПМК и геморрагическим синдромом часто обнаруживают тромбоцитоз и повышение АДФ–агрегации тромбоцитов, которые расценивают, как реактивные изменения системы гемостаза по типу гиперкоагуляции, как компенсаторную реакцию данной системы на хронический геморрагический синдром.
Синдром психопатологических расстройств
включает неврастению, тревожно–фобические расстройства, расстройства настроения (чаще всего в виде его неустойчивости). Интересен тот факт, что выраженность клинической симптоматики напрямую коррелирует с количеством фенотипических признаков «слабости» соединительной ткани со стороны других систем органов и с выраженностью морфологических изменений кожи (см. выше).
Изменения ЭКГ при ПМК чаще всего выявляются при холтеровском мониторировании. Достоверно чаще у этих пациентов отмечены отрицательные зубцы Т в отведениях V1,2, эпизоды пароксизмальной наджелудочковой тахикардии, дисфункция синусового узла, удлинение интервала QT, суправентрикулярные и желудочковые экстрасистолы в количестве более 240 за сутки, горизонтальная депрессия сегмента ST (продолжительностью более 30 минут за сутки). Поскольку депрессия сегмента ST имеется у лиц с болями в левой половине грудной клетки, отличными от стенокардии, учитывая также молодой возраст этих пациентов, отсутствие дислипидемии и других факторов риска ИБС, данные изменения не трактуются, как ишемические. В их основе лежат неравномерность кровоснабжения миокарда и/или симпатикотония. Экстрасистолы, особенно желудочковые, в большей степени были выявлены в положении больных лежа. При этом во время пробы с физической нагрузкой экстрасистолы исчезали, что свидетельствует об их функциональном характере и о роли гиперпарасимпатикотонии в их генезе. При специальном исследовании мы отметили преобладание парасимпатического тонуса и/или снижение симпатических влияний у лиц с ПМК и экстрасистолией.
При проведении пробы с максимальной физической нагрузкой мы установили высокую или очень высокую физическую работоспособность пациетов с ПМК, которая не отличалась от таковой у лиц контрольной группы. Однако у этих лиц выявлены нарушения гемодинамического обеспечения физической нагрузки в виде более низких пороговых значений частоты сердечных сокращений (ЧСС), систолического артериального давления (АД), двойного произведения и их более низкого прироста на пороговую нагрузку, что напрямую коррелировало с тяжестью СВД и фенотипической выраженностью дисплазии соединительной ткани.
Обычно в клинической практике ПМК ассоциируется с наличием артериальной гипотонии. По нашим данным, частота артериальной гипотонии достоверно не отличалась у лиц с наличием или отсутствием ПМК, однако частота артериальной гипертонии (1 степени по ВОЗ–ВНОК) была достоверно выше, чем в контрольной группе. Артериальная гипертония выявлена нами примерно у 1/3 обследованных молодых (18–40) лиц с ПМК, тогда как в контрольной группе (без ПМК) – лишь у 5%.
Функционирование вегетативной нервной системы при ПМК имеет важное клиническое значение, поскольку до последнего времени считали, что у этих пациентов преобладают симпатические влияния, поэтому препаратами выбора для лечения были b-блокаторы. Однако в настоящее время точка зрения на этот аспект существенно изменилась: среди этих людей имеются лица как с преобладанием тонуса симпатического, так и с преобладанием тонуса парасимпатического звена вегетативной нервной системы. При этом последние даже преобладают. По нашим данным, повышение тонуса того или иного звена больше коррелирует с клиническими симптомами. Так, симпатикотония отмечена при наличии мигрени, артериальной гипертонии, болях в левой половине грудной клетки, пароксизмальной наджелудочковой тахикардии, ваготония – при синкопальных состояниях, экстрасистолии.
Наличие СВД и тип вегетативной регуляции у лиц с ПМК напрямую связан с четвертым синдромом клинической картины – психопатологическими расстройствами. При наличии этих расстройств увеличивается частота выявления и тяжесть СВД, а также частота обнаружения гиперсимпатикотонии. По мнению многих авторов, именно психопатологические расстройства у этих лиц являются первичными, а симптомы СВД – вторичные, возникающие в ответ на эти психопатологические особенности. Косвенно в пользу данной теории свидетельствуют и результаты лечения лиц с ПМК. Так, применение b-блокаторов, хотя и позволяет ликвидировать объективные признаки гиперсимпатикотонии (например, ЧСС достоверно снижается), но все другие жалобы сохраняются. С другой стороны, лечение лиц с ПМК противотревожными препаратами приводило не только к коррекции психопатологических расстройств, значительному улучшению самочувствия пациентов, но и к исчезновению гиперсимпатикотонии (снижались ЧСС и уровень АД, уменьшались или исчезали суправентрикулярные экстрасистолы и пароксизмы наджелудочковой тахикардии).
Диагностика
Основным методом диагностики ПМК по–прежнему является эхокардиография
. В настоящее время считают, что необходимо использовать только В–режим, в противном случае можно получить большое количество ложноположительных результатов. В нашей стране принято делить ПМК на 3 степени в зависимости от глубины пролабирования (1–я – до 5 мм ниже клапанного кольца, 2–я – 6–10 мм и 3–я – более 10 мм), хотя многими отечественным авторами установлено, что ПМК глубиной до 1 см прогностически благоприятен. При этом лица с 1–й и 2–й степенью пролабирования практически не отличаются друг от друга по клинической симптоматике и частоте осложнений. В других странах принято делить ПМК на органический (при наличии миксоматозной дегенерации) и функциональный (в отсутствие ЭхоКГ–критериев миксоматозной дегенерации). На наш взгляд, такое деление более оптимально, поскольку от наличия миксоматозной дегенерации (независимо от глубины ПМК) зависит вероятность развития осложнений.
Под миксоматозной дегенерацией
понимают комплекс морфологических изменений створок митрального клапана, соответствующих «слабости» соединительной ткани (см. выше описание морфологических изменений кожи) и описанных морфологами в результате изучения материалов, полученных при проведении кардиохирургических операций (у лиц с ПМК и тяжелой, гемодинамически значимой, митральной регургитацией). В начале 90–х годов японские авторы создали эхокардиографические критерии миксоматозной дегенерации – их чувствительность и специфичность составляет около 75%. Они включают утолщение створки более 4 мм и ее пониженную эхогенность. Выявление лиц с миксоматозной дегенерацией створок представляется очень важным, поскольку все осложнения ПМК (внезапная смерть, тяжелая недостаточность митрального клапана, требующая хирургического лечения, бактериальный эндокардит и инсульты) в 95–100% случаев отмечены только при наличии миксоматозной дегенерации створок. По мнению ряда авторов, таким больным необходимо проводить антибиотикопрофилактику бактериального эндокардита (например, при удалении зубов). ПМК с миксоматозной дегенерацией считают также одной из причин инсульта у молодых людей с отсутствием общепринятых факторов риска развития инсульта (прежде всего артериальной гипертонии). Мы изучали частоту ишемических инсультов и транзиторных ишемических атак у больных в возрасте до 40 лет по архивным данным 4 клинических больниц Москвы за 5–летний период. Доля этих состояний у лиц до 40 лет составляла в среднем 1,4%. Из причин инсультов у молодых следует отметить гипертоническую болезнь – 20% случаев, однако у 2/3 молодых лиц отсутствовали какие–либо общепринятые факторы риска развития ишемического поражения головного мозга. Части из этих пациентов (кто дал согласие на участие в исследовании) выполнена эхокардиография, и в 93% случаев обнаружен ПМК с миксоматозной дегенерацией пролабирующих створок. Миксоматозно измененные створки митрального клапана могут являться основой для формирования микро– и макротромбов, поскольку потеря слоя эндотелия с появлением мелких ульцераций вследствие увеличения механического напряжения сопровождается отложением на них фибрина и тромбоцитов. Следовательно, инсульты у этих пациентов имеют тромбоэмболический генез, и поэтому лицам с ПМК и миксоматозной дегенерацией ряд авторов рекомендуют ежедневный прием малых доз ацетилсалициловой кислоты. Другой причиной для развития острых нарушений мозгового кровообращения при ПМК является бактериальный эндокардит и бактериальные эмболы.
Лечение
Вопросы лечения этих пациентов практически не разработаны. В последние годы все большее количество исследований посвящено изучению эффективности пероральных препаратов магния
. Это обусловлено тем, что ионы магния необходимы для укладки волокон коллагена в четвертичную структуру, поэтому дефицит магния в тканях обусловливает хаотичность расположения волокон коллагена – основной морфологический признак дисплазии соединительной ткани. Известно также, что биосинтез всех компонентов матрикса в соединительной ткани, а также поддержание их структурной стабильности является функцией фибробластов. С этой точки зрения представляется важным выявленное нами и другими авторами уменьшение содержания РНК в цитоплазме фибробластов дермы, что свидетельствует о снижении биосинтетической активности последних. Учитывая сведения о роли дефицита магния в нарушении функции фибробластов, можно предположить, что описанные изменения биосинтетической функции фибробластов и нарушение структуры экстрацеллюлярного матрикса связаны с дефицитом магния у больных с ПМК.
Ряд исследователей сообщали о дефиците магния в тканях у лиц с ПМК. Нами установлено достоверное снижение уровня магния в волосах у 3/4 пациентов с ПМК (в среднем 60 и менее мкг/г при норме 70–180 мкг/г).
Мы провели лечение 43 пациентов с ПМК в возрасте от 18 до 36 лет в течение 6 месяцев препаратом Магнерот
, содержащим 500 мг оротата магния (32,5 мг элементарного магния) в дозе 3000 мг/сут (196,8 мг элементарного магния), на 3 приема.
После применения Магнерота у больных с ПМК выявлено достоверное уменьшение частоты всех симптомов СВД
. Так, частота нарушений вегетативной регуляции ритма сердца уменьшилась с 74,4 до 13,9%, нарушений терморегуляции – с 55,8 до 18,6%, болей в левой половине грудной клетки – с 95,3 до 13,9%, расстройств желудочно–кишечного тракта – с 69,8 до 27,9%. До лечения легкая степень СВД диагностирована в 11,6%, средняя – в 37,2%, тяжелая в 51,2% случаев, т.е. преобладали больные с тяжелой и средне–тяжелой выраженностью синдрома вегетативной дистонии. После лечения отмечено достоверное уменьшения тяжести СВД: появились лица (7%) с полным отсутствием данных нарушений, в 5 раз увеличилось количество больных с легкой степенью СВД, при этом тяжелой степени СВД не обнаружено ни у одного больного.
После терапии у больных с ПМК также достоверно уменьшились частота и выраженность сосудистых нарушений:
утренней головной боли с 72,1 до 23,3%, синкопов с 27,9 до 4,6%, предобморочных состояний с 62,8 до 13,9%, мигрени с 27,9 до 7%, сосудистых нарушений в конечностях с 88,4 до 44,2%, головокружений с 74,4 до 44,2%. Если до лечения легкая, средняя и тяжелая степени были диагностированы у 30,2, 55,9 и 13,9% лиц соответственно, то после лечения в 16,3% случаев сосудистые нарушения отсутствовали, в 2,5 раза увеличилось число больных с легкой степенью сосудистых расстройств, тяжелая же степень не выявлена ни у одного из обследованных после лечения Магнеротом.
Установлено и достоверное уменьшение частоты и тяжести геморрагических нарушений:
обильных и/или длительных менструаций у женщин с 20,9 до 2,3%, носовых кровотечений – с 30,2 до 13,9%, исчезала кровоточивость десен. Число лиц без геморрагических нарушений увеличилось с 7 до 51,2%, со средней степенью выраженности геморрагического синдрома – уменьшилось с 27,9 до 2,3%, а тяжелая степень не выявлена.
Наконец, после лечения у больных с ПМК достоверно уменьшилась частота неврастении
(с 65,1 до 16,3%) и расстройств настроения (с 46,5 до 13,9%), хотя частота тревожно–фобических расстройств не изменилась.
Выраженность клинической картины в целом после лечения также достоверно уменьшилась. Поэтому неудивительно, что было отмечено высокодостоверное повышение качества жизни этих больных
. Под этим понятием подразумевают субъективное мнение больного об уровне своего благополучия в физическом, психологическом и социальном плане. До лечения по шкале самооценки общего самочувстия лица с ПМК оценили его хуже, чем контрольная группа (лица без ПМК) – примерно на 30%. После лечения больные с ПМК отметили достоверно улучшение качества жизни по этой шкале – в среднем на 40%. При этом оценка качества жизни по шкалам «работа», «социальная жизнь» и «личная жизнь» до лечения у лиц с ПМК также отличалась от контроля: при наличии ПМК больные расценили имеющиеся у них нарушения по этим трем шкалам, как начальные или умеренные – примерно в равной степени, тогда как здоровые люди отмечали отсутствие нарушений. После лечения у больных с ПМК выявлено высокодостоверно улучшение качества жизни – на 40–50% по сравнению с исходным.
По данным холтеровского мониторирования ЭКГ после терапии Магнеротом по сравнению с исходным уровнем установлено достоверное уменьшение средней ЧСС (на 7,2%), количества эпизодов тахикардии (на 44,4%), продолжительности интервала QT и количества желудочковых экстрасистол (на 40%). Особенно важным представляется положительный эффект Магнерота в лечении желудочковой экстрасистолии
у этой категории пациентов.
По данным суточного мониторирования АД выявлены достоверное снижение до нормальных значений среднего систолического и диастолического АД, гипертонической нагрузки. Данные результаты подтверждают ранее установленный факт, что между уровнем магния в тканях и уровнем АД существует обратная зависимость, а также тот факт, что дефицит магния является одним из патогенетических звеньев развития артериальной гипертонии.
После лечения выявлено уменьшение глубины пролабирования митрального клапана, достоверное уменьшение числа пациентов с гиперсимпатикотонией, при этом увеличилось количество лиц с равным тонусом обоих отделов вегетативной нервной системы. Подобные сведения содержатся и в работах других авторов, посвященных лечению лиц с ПМК пероральными препаратами магния.
Наконец, по данным морфологического исследования биоптатов кожи после терапии Магнеротом в 2 раза уменьшилась выраженность морфологических изменений.
Таким образом, после 6–ти месячного курса терапии препаратом Магнерот у пациентов с идиопатическим ПМК установлено значительное улучшение объективной и субъективной симптоматики с полной или почти полной редукцией проявлений болезни более чем у половины больных. На фоне лечения отмечено уменьшение тяжести синдрома вегетативной дистонии, сосудистых, геморрагических и психопатологических расстройств, нарушений ритма сердца, уровня АД, а также улучшение качества жизни пациентов. Кроме того, на фоне лечения достоверно уменьшилась выраженность морфологических маркеров дисплазии соединительной ткани по данным биопсии кожи.
Литература:
1. Мартынов А.И., Степура О.Б., Остроумова О.Д. и соавт. Пролапс митрального клапана. Часть I. Фенотипические особенности и клинические проявления. // Кардиология. – 1998,№1 – С.72–80.
2. Мартынов А.И., Степура О.Б., Остроумова О.Д. и соавт. Пролапс митрального клапана. Часть II. Нарушения ритма и психологический статус. // Кардиология. – 1998,№2 – С.74–81.
3. Степура О.Б., Остроумова О.Д. и соавт. Роль магния в патогенезе и развитии клинической симптоматики у лиц с идиопатическим пролапсом митрального клапана. // Российский кардиологический журнал – 1998, №3 – С.45–47.
4. Степура О.Б., Мельник О.О., Шехтер А.Б. и соавт. Результаты применения магниевой соли оротовой кислоты «Магнерот» при лечении больных с идиопатическим пролапсом митрального клапана. // Российские медицинские вести – 1999 – №2 – С.12–16.
Дегенерация МК — клинические проявления
Одышка при физической нагрузке
Клиническая картина данного заболевания напрямую зависит от стадии заболевания и степени компенсации организма.
Первая степень в подавляющем большинстве случаев клинических проявлений не имеет, так как регургитации (обратного заброса крови) нет и в целом гемодинамика организма не нарушена. Могут, конечно, встречаться общие симптомы — головокружение, повышенная усталость, уменьшение переносимости физической нагрузки, но эти симптомы встречаются при огромном множестве других заболеваний и даже у полностью здоровых людей.
При второй степени уже присутствуют небольшие отрывы хорды, а также имеется регургитация, хотя уровень ее и не критичный, но физиологически и клинически пациент ощущать ее будет. Отмечается снижение работоспособности, общая слабость, беспокоит одышка при физической нагрузке, причем при такой нагрузке, при которой раньше никаких подобных симптомов не было (например, подъем на третий этаж).
Также таких пациентов может беспокоить покалывание в области сердца, нарушение ритма, которое также начинается после непродолжительной физической нагрузки.
Но всех этих симптомов может и не быть, если вы заметили хотя бы несколько подобных из них, то стоит незамедлительно обратиться к врачу, ведь раннее обращение увеличивает шансы на полное выздоровление в несколько раз.
Пенистый кашель с прожилками крови
Для третьей степени из-за истощения компенсационной способности организма характерны все вышеперечисленные симптомы, но поскольку из-за полного отрыва хорды смыкание створок сильно нарушено или вообще отсутствует, то симптомы будут очень выраженны. Пациент жалуется на тяжелую одышку даже при малейшей физической нагрузке, также иногда беспокоит кашель, часто пенистый, с прожилками крови.
Беспокоит головокружение, которое часто приводит к обморокам. Иногда пациентов беспокоят стенокардитичесие боли в области сердца, которые не ослабевают даже после приема нитратных препаратов типа нитроглицерина. В данную стадию любое промедление по оказанию квалифицированной медицинской помощи может привести к летальному исходу.
Лечение недостаточности митрального клапана в Израиле
Никакая консервативная терапия не способна устранить причину недостаточности клапана. При недостаточности 1 степени необходимо избегать повышенных физических и эмоциональных нагрузок, вести здоровый образ жизни. Крайне нежелательно злоупотребление алкоголем и курение.
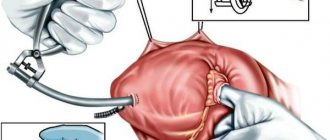
- Хирургическое лечение показано при недостаточности со струей регургитации 2-3 степени. Целью операции является восстановление запирательной функции митрального клапана.
- Коррекция осуществляется при выключенном из кровообращения сердце. Его функцию в это время выполняет аппарат искусственного кровообращения. В подавляющем большинстве случаев производится протезирование клапана. Могут использоваться как искусственные клапаны, так и биологические протезы (достаточно успешно производится протезирование клапанами свиней). Пораженный клапан при этом удаляется.
- Если клапан изменен не сильно, то возможно проведение клапаносохраняющих операций: пластика кольца клапана;
- сужение кольца клапана;
- пластика створок;
- замещение отдельных створок.
Никогда не следует затягивать с проведением операции, поскольку при пороках с большим объемом регургитации наступают необратимые изменения со стороны полостей сердца и его стенок.
Опыт медиков и современные технологии позволяют производить операции без разреза грудины, как это делается обычно. В некоторых случаях может быть использован доступ со стороны ребер, что значительно снижает наносимую травму.
Внимание! Все поля формы обязательны. Иначе мы не получим Вашу информацию. Альтернативно пользуйтесь
Диагностический алгоритм при подозрении на МД МК
Общеклинические анализы
Дегенерация митрального клапана диагностируется на основании жалоб пациента, о которых мы говорили выше (в разделе «Дегенерация МК — клинические проявления»), но даже при их отсутствии следует обследовать пациента специальными методами, о которых мы поговорим ниже.
Далее доктор назначает пациенту общеклинические анализы, такие как общий анализ крови, общий анализ мочи и биохимический анализ крови. Чаще всего изменения в них отсутствуют, но при третьей степени недостаточности в общем анализе крови может выявляться анемия или наоборот признаки сгущения крови (увеличение уровня эритроцитов, тромбоцитов, гемоглобина и уменьшение уровня СОЭ), связано это с выходом жидкой части крови в третье пространство (легкие).
УЗИ исследование сердца с допплерометрией
«Золотым» стандартом при выявлении недостаточности клапана и разрыва хорды является УЗИ-исследование сердца с допплерометрией. Этот метод и позволяет выявить стадию и степень декомпенсации заболевания, причем это можно сделать еще до того как ребенок родился, а значит рано выявить и назначит раннее лечение.
Не высокоспецифичными методами, но нужными для ранней диагностики заболевания является ЭКГ исследование и рентген-исследование органов грудной клетки. В первом случае мы выявим признаки гипертрофии левых отделов сердца, а в третью стадию присоединится и гипертрофия правых отделов сердца, также выявляются различные суправентрикулярные тахиаритмии типа фибриляции или трепетания предсердий, суправентрикулярные экстрасистолий.
А при рентген-исследовании будут признаки легочной гипертензии, выбухание дуги левого предсердия, а также расширение границ сердца (в третьей стадии развитие «бычьего» сердца).
Для уточнения диагноза могут применяться специальные методы исследования — катетеризация левого и правого желудочков, а также левая вентрикулография, которые помогут уточнить наличие заболевания и его степень.
Диагностика недостаточности митрального клапана в Израиле
Диагностика недостаточности митрального клапана начинается с традиционных методов, которые знакомы врачам уже на протяжении сотен лет.
- Объективное обследование – отмечается цианоз периферических частей тела и видимых слизистых, могут отмечаться отеки стоп.
- При пальпации можно отметить смещение верхушечного толчка влево. Перкуссия позволяет выявить смещение границы сердечной тупости влево, поскольку происходит гипертрофия левого желудочка.
- Аускультация – отмечается ослабление 1 тона, при выслушивании его на верхушке сердца. Также выслушивается акцент 2 тона на легочном стволе. Также выслушивается систолический шум.
- Рентгенологическое исследование позволяет судить о форме сердца. Оно приобретает митральную конфигурацию из-за гипертрофии левого желудочка.
- Имеются изменения и в результатах ЭКГ, позволяющие судить о клапанном пороке.
- На ЭХО-КГ видно утолщение створок митрального клапана, усиление амплитуды колебаний его створок.
- Доплерография позволяет выявить струю регургитации в левое предсердие. Выделяют 4 степени регургитации: 1 степень – струя регургитации достигает 4 мм;
- 2 степень – струя от 4 до 6 мм;
- 3 степень – 6-9 мм;
- 4 степень – более 9 мм.