Транзиторная ишемическая атака головного мозга является временным острым расстройством центральной нервной системы. В медицинской практике такую патологию могут еще называть микроинсультом. Единственное отличие заключается в продолжительности проявления симптоматики. В случае с транзиторной ишемией признаки исчезают в течение часа, они не несут необратимых последствий. Чаще всего такого рода нарушения обнаруживаются у лиц пожилого возраста.
Диагностика осуществляется на основании совокупности всех сведений, получаемых путем медицинских исследований: компьютерной, магнитно-резонансной томографии, результатов УЗДГ, ПЭТ отделов головного мозга. Дополнительно могут назначать лабораторные процедуры. Обследование желательно проходить в специализированных неврологических центрах.
Лечение транзиторной ишемической атаки головного мозга может быть консервативным, симптоматическим и оперативным. Все зависит от возраста пациента, наличия сопутствующих заболеваний и общего состояния. Терапия необходима для того, чтобы исключить риск развития инсульта. По статистике, у больного по истечении 2 дней после приступа риск инсульта составляет 4 %, через 30 дней — 8 %, в течение 5 лет — 29 %.
Общие сведения
Понятие транзиторной ишемической атаки (сокр. ТИА) достаточно широкое и представляет собой преходящее нарушение кровообращения головного мозга. Присвоенный код транзиторной ишемической атаки по мкб-10: G45.9.
Патология развивается по ишемическому типу – возникает в результате местного снижения кровообращения и приводит к эпизодам неврологических нарушений (парезам и различным нарушениям чувствительности). ТИА также сопровождается ишемией сетчатки глаза, но при этом не происходит развития инфаркта мозга. Если выявляются необратимые ишемические повреждения участков головного мозга, то говорят об инсульте.
Ишемическая атака, что это такое? Ранее считалось, что атака — это заболевание быстро развивающейся симптоматики с очаговыми и диффузными поражениями функций мозга, которое возникает без воздействия явных внесосудистых факторов и длится менее 1 суток. Однако, в дальнейшем ученые изменили определение, так как зачастую симптомы сохранявшиеся в течение суток на МРТ головного мозга в условиях диффузно-взвешенного режима приводили к инфаркту. Поэтому на данный момент установлено, что в среднем длительность транзиторных атак обычно не превышает 1 часа.
На сегодняшний день достаточно важно своевременно выявить ТИА и оценить распространенность поражений, но, к сожалению, больные не обращают внимания на периодически преходящие симптомы и не консультируются у врача. И это очень плохая тенденция, ведь в 30-50% случаев у особ, перенесших транзиторную ишемическую атаку или так называемый микроинсульт в течение 5 лет диагностируется инсульт.
Нейровизуализация и антитромбоцитарная терапия
Результаты нейровизуализации могут оказать существенное влияние на выбор методов лечения. Агрессивное ведение больных с применением ДАТ увеличивает риск внутричерепных кровоизлияний (ВЧК). И это существенно ограничивает лечение больных с ТИА в отличие от больных с ОКС. И хотя действующие клинические рекомендации позволяют назначать ДАТ всем больным с ТИА и малыми ИИ, безопаснее начать лечение с приема нагрузочной дозы ацетилсалициловой кислоты (300–325 мг), а клопидогрел (как второй компонент ДАТ) в нагрузочной дозе 300 мг включить в схему лечения после проведения МРТ (КТ) [3, 4, 11]. Необходимо отметить, что российские клинические рекомендации 2021 г. демонстрируют более осторожный подход к ДАТ, предписывая назначение двух антитромбоцитарных препаратов только пациентам, имеющим, наряду с картиной острой церебральной ишемии, и кардиологические показания для более агрессивной терапии [12]. Если по результатам нейровизуализации у больного обнаруживаются биомаркеры высокого риска ВЧК, врач в связи с этим может ограничить агрессивность лечения (табл. 1).
Если при МРТ (КТ) не обнаруживаются биомаркеры высокого риска ВЧК, то ДАТ в течение 2–3 нед. заметно снижает вероятность всех сосудистых событий и ИИ. Нагрузочные дозы (300–325 мг для ацетилсалициловой кислоты и до 300 мг для клопидогрела) были использованы в клинических исследованиях, результаты которых показали снижение вероятности инсульта в течение 90 дней после ТИА на 32% [13–16]. В работах [14, 17–19] установлено, что преимущества от назначения ДАТ получают больные с ТИА и малыми ИИ без признаков амилоидной церебральной ангиопатии. Клинические рекомендации AHA/ASA 2021 г. разрешают применение ДАТ при ТИА и ИИ, допуская возможность продления такой терапии до 3 мес. [11]. Последние европейские руководства демонстрируют более осторожный подход к агрессивной антитромботической терапии, ограничивая продолжительность ДАТ 10–21 сут [17]. Таким образом, активная антитромбоцитарная терапия для пациентов с ТИА не только возможна, но и в высшей степени целесообразна [10, 17, 18]. Очевидной представляется тенденция последних лет к увеличению активности антитромботической терапии при ТИА. Антитромбоцитарные препараты назначают как можно раньше в комбинациях и дозах, которые в максимальной степени предупреждают повторные сосудистые события. Относительно новое понятие «ранняя вторичная профилактика» предполагает активное или даже агрессивное ведение больных в первые часы и дни после появления симптомов декомпенсации кровообращения в церебральном сосудистом бассейне. Антиагреганты назначают независимо от предполагаемого подтипа ОНМК. Однако через несколько дней после кардионеврологического обследования больные с фибрилляцией предсердий должны получать антикоагулянты вместо антиагрегантов. Принципиальный подход к активному ведению больных с ТИА не ограничивается антитромботической терапией. Антигипертензивная и гиполипидемическая терапия для пациентов с признаками ТИА отличается от стратегии, которая применяется при крупноочаговых инсультах.
Патогенез
Ишемия тканей мозга является преходящим нарушением мозгового кровоснабжения, которое еще принято называть микроинсультом. При этом неврологические симптомы исчезают самопроизвольно в течение часа после окончания атаки, не вызывая необратимых органических повреждений в структурах головного мозга.
Транзиторные ишемические атаки обычно развиваются в условиях атеросклеротической окклюзии магистральных сосудов приносящих кровь к голове. К ним относят систему сонных артерий – особенно в местах бифуркации, а также вертебральные артерии. Чаще всего патогенезу способствует компрессия и ангиоспазм, вызванные остеохондрозом.
Механизм развития ТИА
Ишемия церебральных тканей включает в себя 4 этапа:
- Авторегуляция – возникающая благодаря компенсаторному расширению церебральных сосудов как ответ на пониженное перфузионное давление мозгового кровообращения, вызывает увеличение объемов крови, которой заполняются сосуды головного мозга.
- Олигемия – дальнейшее нарастание падения показателей перфузионного давления вызывает уменьшение церебрального тока крови, когда не может быть компенсировано авторегуляторными механизмами, на этом этапе процессы кислородного обмена еще не нарушены.
- Обратимая ишемия — развитие «ишемической полутени», вызванной нарастанием снижения перфузионнного давления и снижением уровня кислородного обмена, что приводит к гипоксии и нарушению работы нейронов.
- Необратимая ишемия — представляет собой необратимую клеточную смерть или апоплексическую деполяризацию нейронов.
Таким образом, микроинсульт вызывает нарушения церебральной гемодинамики, внезапные и кратковременные дисциркуляторные расстройства в структурах головного мозга, проявляющиеся очаговыми и общемозговыми симптомами, сохраняющимися в течение суток.
Контроль АД и гиполипидемическая терапия
Агрессивная терапия ТИА, кроме ДАТ, предполагает назначение гиполипидемической и антигипертензивной терапии с достижением целевых значений АД (130/80 мм рт. ст.) так скоро, как это только возможно. Такая лечебная стратегия существенно отличается от принятого в действующих рекомендациях порядка оказания помощи больным с ОНМК, в которых не упоминаются статины, а артериальная гипертензия до 180 мм рт. ст. считается допустимой в первые часы заболевания [12]. Артериальная гипертония является важнейшим фактором риска ИИ и частым спутником острого периода сосудистой катастрофы. Причины артериальной гипертонии в остром периоде ИИ связывают с активацией нейроэндокринных и нейрогенных механизмов регуляции АД, ишемией стволовых структур мозга, госпитальным стрессом, срывом ауторегуляции мозгового кровообращения [20]. Оптимальные значения систолического и диастолического АД в острой фазе ИИ не установлены, и у клиницистов нет на этот счет единого мнения. Крупные исследования, которые должны решить этот вопрос, в настоящее время еще не закончены [20–22]. Единственный аргумент, оправдывающий высокий уровень АД в остром периоде ИИ, — это предполагаемая возможность наилучшей перфузии ткани мозга в области ишемического очага при высоком системном давлении в условиях срыва ауторегуляции [23, 24]. Однако результаты последних исследований не поддерживают эту идею [24]. Предположение о благоприятном влиянии высокого систолического АД на поврежденный мозг представляется неубедительным и в отношении периваскулярного отека, так как у больных с высокими значениями АД и формирующимся инфарктом мозга отек в зоне повреждения более выражен [24, 25]. Еще менее обоснованным представляется сохранение «лечебной» артериальной гипертензии у больных с ТИА. Преходящая фокальная церебральная ишемия очень часто ассоциируется с гипертоническим кризом, церебральным вазоспазмом и тромбоэмболией. Во всех случаях ТИА условия для восстановления церебрального кровотока будут лучше при показателях АД, близких к нормальным. Гиполипидемическая терапия статинами не упоминается в руководствах по ведению больных в остром периоде инсульта, но активно используется у больных с ТИА [2, 3, 25]. Плейотропные эффекты статинов, обеспечивающие уменьшение отека, стабилизацию атеросклеротических бляшек и восстановление микроциркуляции, могут оказаться полезными не только для предупреждения повторного сосудистого события. Исследования, в которых для верификации результатов интенсивной гиполипидемической терапии у больных с атеротромботическим ИИ были использованы биомаркеры воспаления и деструкции тканей (высокочувствительный С-реактивный белок и матриксная металлопротеаза 9), показали эффективность аторвастатина в суточной дозе 60 мг [25].
Классификация
Транзиторная ишемическая атака может отличаться по длительности и тяжести течения, поэтому приступы ТИА бывают:
- легкие – их длительность обычно не превышает 10 мин;
- средне тяжелые – длятся от 10 мин до нескольких часов и не вызывают органических симптомов после полного восстановления функций;
- тяжелые – могут длиться до 24 часов и в результате дают легкую органическую симптоматику после полного восстановления функций.
Клиническая картина ТИА отличается в зависимости от того в каком отделе кровоснабжения возникла окклюзия – в вертебробазилярном или каротидном бассейне.
Транзиторная ишемическая атака в вертебро-базилярном бассейне
По данным Верещагина Н.В. (1980 г.) ТИА возникающая в вертебро-базилярном бассейне является самым распространенным типом транзиторной ишемии, на нее приходится примерно 70% всех случаев. Клинические проявления состоят из ряда симптомов и синдромов:
- системные случаи головокружения с приступами головной боли в области затылка и другими стволовыми симптомами;
- различные нарушения работы зрительного анализатора: нистагм, диплопия, гемианопсия (двусторонняя слепота, возникающая в половине поля зрения), фотопсия (появление в поле зрения движущихся образов);
- тошнота и рвота, которая может быть неукротимой;
- альтернирующие синдромы и разные варианты проявлений синдрома Валенберга и Захарченко;
- дроп-атаки (внезапное падение человека без потери сознания);
- атаки дезориентировки;
- временная утрата памяти и другие признаки транзиторного глобального амнестического синдрома;
- синдром недостаточности кровотока в артериях вертебробазилярного бассейна, наиболее часто возникающий в виде дисциркуляторынх обмороков — синкопального вертебрального синдрома Унтерхарншайдта.
Причина транзиторной ишемической атаки в вертебро базилярном бассейне
Транзиторная ишемическая атака в каротидной системе
Окклюзия артерий каротидной системы приводит:
- к преходящим геми- и монопарезам;
- гипестезии по гемитипу в одной из конечностей и пальцах;
- различным нарушениям речи, наиболее часто проявляющимся в виде частичной моторной афазии;
- развитию оптико-пирамидного синдрома.
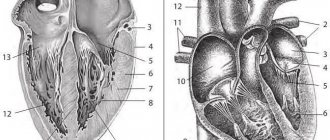
Артерии каротидного бассейна
Нарушение кровообращения головного мозга при шейном остеохондрозе
Шейный остеохондроз – современный недуг, который поражает 60-80% населения среднего возраста индустриальных развитых стран. Он ведет к стенозу – сдавливанию сосудов вдоль спинного мозга в результате образования грыж, остеофитов, а также разрастания и утолщения других позвоночных тканей. Изначально человек испытывает только скованность, болевой синдром в пораженном отделе позвоночника, но в дальнейшем присоединяется корешковый синдром. Он проявляется в виде головной боли, парестезиях, нарушениях речи и обоняния.
Самым опасным при шейном остеохондрозе становится компрессия – сдавливание позвоночной артерии каротидной системы. Оно вызывает развитие синдрома позвоночной артерии, который выражается в виде постоянной или приступообразной жгучей головной боли, больше всего охватывающей затылок, виски и шею. Может привести к ишемии церебральных тканей и развитию различных общемозговых и очаговых симптомов как при микроинсульте.
Поражения сонной артерии
Появление типичной симптоматики наблюдается через 2-5-минутный промежуток. При дисфункции обращения кровеносной системы в области сонной артерии больной чувствует слабость, внезапно теряет зрение, полностью или частично перестаёт говорить.
Часто наблюдается двигательная дисфункция конечностей на одной из сторон, а также пациент теряет чувствительность.
Пульс стремительно падает, в сонной артерии слышится шум. На болезнь может указывать очаговая симптоматика поражения мозговых структур головы: лицо становится асимметричным, давление колеблется, сетчатка меняется.
В области грудины ощущается тяжесть, сердце работает с перебоями, не хватает воздуха для дыхания, появляются судороги, хочется плакать.
Причины
Главные причины развития транзиторной ишемической атаки артериальная гипертензия, тромбоэмболия и атеросклеротические поражения крупных сосудов, приносящих кровь к головному мозгу, например, позвоночные и сонные артерии. Кроме того, в патогенезе значительную роль играют нарушения нервной регуляции состояния сосудов и обменных процессов в мозгу, наличие таких морфологических изменений как стенозы, а также изменения физико-химических и биохимических свойств крови. К ним относят увеличение вязкости, адгезию и агрегацию форменных элементов крови.
Наиболее всего подвержены риску развития ТИА особы:
- старческого и пожилого возраста;
- страдающие от артериальной гипертензии или от сердечных заболеваний, включая мерцательную аритмию, аневризму левого желудочка, кардиомиопатию, бактериальный эндокардит, перенесенный инфаркт миокарда или наличие искусственного клапана сердца;
- больные сахарным диабетом;
- при сдавливании позвоночной артерии остеофитами, образованными в результате шейного остеохондроза либо анкилозирующего спондилоартрита (болезнь Бехтерева);
- подверженные стрессам и занимающие ответственные должности;
- чрезмерно большие нагрузки и тяжелые условия труда;
- с большим стажем табакокурения;
- с реактивными изменениями тканей миокарда и эндотелия, вызванными болезнью Фабри;
- имеющие отложения глобозидов в тканях и органах сердечно-сосудистой системы.
Симптомы транзиторной ишемической атаки
Симптомы ишемической атаки головного мозга могут значительно отличаться в зависимости от того, какой участок головного мозга был затронут, но есть ряд клинических нарушений являющихся общемозговыми симптомами, к ним относится:
- головокружение;
- головная боль;
- кратковременная потеря сознания.
Очаговые симптомы нарушения кровообращения головного мозга проявляются в виде:
- временной потери речи и нарушений речи — афазии;
- утрате способности читать и/или писать;
- слабости в одной из половин тела – гемипарезе, вызывающем потерю равновесия и нарушение координации движений;
- косоглазия или обездвиженности глазных яблок, утрате зрения или резкого его ухудшения;
- непроизвольное мочеиспускание;
- онемения – гипестезии, нарушения чувствительности и покалывания – парестезии.
Осложнения и последствия ишемической атаки головного мозга
Транзиторная атака характеризуется приходящими симптомами в результате нарушения церебрального кровообращения. Они должны проходить в течение суток и не провоцировать тяжелые последствия. К симптомам сохраняющимся после перенесенного тяжелого микроинсульта относится:
- невнятная речь;
- амнезия;
- паралич;
- ухудшение остроты зрения.
Для реабилитации после микроинсульта и наиболее успешного прогноза — предупреждения ишемического инсульта необходима помощь многих специалистов:
- невролог – мониторит состояние церебральных сосудов, работу нейронов и уровень обменных процессов в головном мозге;
- кардиолог – подберет лучшую схему лечения для нормализации артериального давления и сердечного ритма;
- эндокринолог – поможет скорректировать уровень сахара в крови и нивелировать негативное влияние сахарного диабета;
- логопед – специалист, который поможет решить проблемы с речью;
- психолог – необходим для коррекции психических нарушений.
Диагностика ТИА
После возникновения любого симптома человек должен госпитализироваться в неврологическое отделение. Специалисты европейских клиник способны в экстренном порядке сделать пациенту МРТ головы и КТ для отслеживания изменений головного мозга, диагностики ишемии или дифференцировки нозологических форм.
Визуализировать повреждение сосудов мозга позволяет МР или КТ-ангиография – процедуры контрастного обследования артерий после введения контраста внутрь вены. Одновременно с оценкой проходимости артериальной сети оценивают состояние сердечнососудистой системы:
- Холтеровское мониторирование;
- Эхокардиография;
- Электрокардиография.
Лабораторные способы диагностики:
- Определение антикардиолипиновых антител, волчаночного антикоагулянта, антитромбина III, протеина S и C, Д-димера, фактора Виллебранда;
- Изучение коагулограммы;
- Биохимический анализ.
После появления первых неврологических признаков церебрального ишемического приступа обязательно требуется консультация нескольких специалистов – окулиста, кардиолога, терапевта.