Общие сведения
Homocysteine – это продукт обмена цистеина и метионина. Для его метаболизма требуется фолиевая кислота, B6 и B12. При их дефиците возможно повышение уровня Homocysteine. Переизбыток этого вещества приводит к развитию серьезных проблем со здоровьем. Возможно появление сгустков крови и повреждения стенок сосудов. Анализ крови на гомоцистеин
часто используется для определения вероятности появления патологий сердечно-сосудистой системы, но его ценность в этом плане сомнительна. В ходе исследований было установлено, что восполнение недостатка фолиевой кислоты и витаминов не снижает риск заболеваний.
Резкий рост показателей часто наблюдается при гомоцистеинурии. Это генетическое заболевание, при котором в ферменте имеется дефект, препятствующий расщеплению метионина. Происходит накопление аминокислот в организме. Новорожденный с таким заболеванием визуально не отличается от здоровых малышей. Нарушения проявляются только через несколько лет. Дети с таким заболеванием худые и высокие, у них тонкие пальцы. У них появляются аномалии скелета, развивается остеопороз, возможны ранние сердечно-сосудистые заболевания.
Введение
Гомоцистеин является продуктом превращения метионина, одной из восьми незаменимых аминокислот. Из гомоцистеина в дальнейшем может образовываться другая аминокислота, цистеин, не входящая в число незаменимых аминокислот.
Избыток накапливающегося в организме гомоцистеина может обратно превращаться в метионин. Кофакторами ферментов метаболических путей метионина в организме выступают витамины, самыми важными из которых являются фолиевая кислота, пиридоксин (витамин B6), цианокобаламин (витамин B12) и рибофлавин (витамин B1).
Гомоцистеин не является структурным элементом белков, а потому не поступает в организм с пищей. В физиологических условиях единственным источником гомоцистеина в организме является превращение метионина.
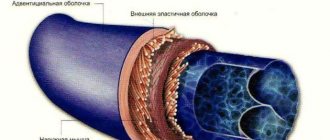
Гомоцистеин обладает выраженным токсическим действием на клетку. Для защиты клетки от повреждающего действия гомоцистеина существуют специальные механизмы выведения его из клетки в кровь. Поэтому, в случае появления избытка гомоцистеина в организме, он начинает накапливаться в крови, и основным местом повреждающего действия этого вещества становится внутренняя поверхность сосудов.
Для превращения избытка гомоцистеина в метионин нужны высокие концентрации активной формы фолиевой кислоты (5-метилтетрагидрофолата). Основным ферментом, обеспечивающим превращение фолиевой кислоты в ее активную форму, является 5,10 метилентетрагидрофолат-редуктаза (MTHFR). Снижение активности этого фермента — одна из важных причин накопления гомоцистеина в организме. (рис. 1)
Рис. 1
Обратите внимание на то, что гомоцистеин может образовываться только из метионина. Гомоцистеин может превращаться либо в цистатионин, который в дальнейшем используется для синтеза цистеина, либо в метионин. На всех ключевых этапах метаболизма метионина и гомоцистеина важную роль играют витамины. Красным цветом обозначен цикл превращения метионина, зеленым — цикл превращения фолиевой кислоты. MTHFR — 5,10 метилентетрагидрофолат-редуктаза. Метионин, гомоцистеин и фолиевая кислота являются аминокислотами. Аминокислоты являются важнейшими субстратами метаболизма азота в организме. От аминокислот берут начало белки, ферменты, пуриновые и пиримидиновые основания (и нуклеиновые кислоты), пиррольные производные (порфирины), биологически активные соединения пептидной природы (гормоны), а также ряд других соединений. При необходимости аминокислоты могут служить источником энергии, главным образом за счет окисления их углеродного скелета. В живых организмах аминокислоты образуют пул, величина которого во взрослом состоянии остается в физиологических условиях постоянной. Она соответствует разнице между поступлением аминокислот извне или иногда из эндогенных источников, и расходом аминокислот, служащих субстратами в анаболических и катаболических процессах. Живые организмы не запасают аминокислоты и белки впрок, поэтому необходимое количество азота (лучше в форме аминокислот) должно поступать с пищей. Во взрослом организме в физиологических условиях количество поступающего и выводящегося азота одинаково (азотное равновесие). Аминокислоты из экзогенных источников (из пищи) всасываются в пищеварительном тракте и переносятся кровью в печень и другие ткани и органы, где они далее используются. Кроме того, источником аминокислот (эндогенный источник) могут служить тканевые белки организма, которые постоянно подвергаются метаболизму с освобождением входящих в них аминокислот. Эти аминокислоты используются для синтеза новых белков лишь в малой степени, однако эндогенные источники очень важны, поскольку они обеспечивают около двух третей всего пула аминокислот, и только одна треть аминокислот поступает из пищи. Незаменимые аминокислоты — это те аминокислоты, которые не могут синтезироваться данным организмом. Для человека это валин, лейцин, изолейцин, лизин, метионин, треонин, фенилаланин, триптофан и, в определенных условиях, также аргинин и гистидин.
Интерпретация результатов
Референсные значения варьируются в зависимости от возраста. Для грамотной интерпретации результатов необходимо обращаться к врачу, самодиагностика недопустима. Повышенные показатели гомоцистеина могут указывать на дефицит витаминов группы B, почечную недостаточность, диабет, псориаз, старческое слабоумие, осложнения беременности. Также они могут быть повышены при недоедании. Значительно повышенные показатели у новорожденного указывают на гомоцистеинурию. Для подтверждения этого диагноза в обязательном порядке проводится дополнительное обследование. Недостаток аминокислоты наблюдается при синдроме Дауна и гипертиреозе.
На результаты теста может влиять длительный прием ряда лекарственных препаратов, поэтому о приеме любых лекарств необходимо поставить в известность врача.
Гипергомоцистеинемия и патология беременности
Гипергомоцистеинемия приводит к повреждению и активации эндотелиальных клеток (клеток выстилки кровеносных сосудов), что значительно повышает риск развития тромбозов. Не все детали механизма патологического действия гипергомоцистеинемии до конца изучены, но многое уже известно.
Тромбогенное действие гомоцистеина может быть связано с повреждением клеток эндотелия, неспецифическим ингибированием синтеза простациклина, активацией фактора V, торможением активации протеина C, даун-регуляцией экспрессии тромбомодулина, блокадой связывания тканевого активатора плазминогена эндотелиальными клетками. Кроме того, высокие уровни гомоцистеина усиливают агрегацию тромбоцитов вследствие снижения синтеза эндотелием релаксирующего фактора и NO, индукции тканевого фактора и стимуляции пролиферации гладкомышечных клеток.
Микротромбообразование и нарушения микроциркуляции приводят к целому ряду акушерских осложнений. Нарушение плацентации и фетоплацентарного кровообращения могут быть причиной репродуктивной недостаточности: невынашивания беременности и бесплодия в результате дефектов имплантации зародыша. На более поздних стадиях беременности гипергомоцистеинемия является причиной развития хронической фетоплацентарной недостаточности и хронической внутриутробной гипоксии плода. Это приводит к рождению детей с низкой массой тела и снижению функциональных резервов всех жизнеобеспечивающих систем новорожденного и развития целого ряда осложнений периода новорожденности.
Гипергомоцистеинемия может быть одной из причин развития генерализованной микроангиопатии во второй половине беременности, проявляющейся в виде позднего токсикоза (гестоза): нефропатии, преэкламсии и экламсии. Для гипергомоцистеинемии характерно развитие тяжелых, часто неуправляемых состояний, которые могут приводить к досрочному прерыванию беременности по медицинским показаниям. Рождение незрелого недоношенного ребенка в таких случаях сопровождается высокой детской летальностью и большим процентом неонатальных осложнений.
Гомоцистеин свободно переходит через плаценту и может оказывать тератогенное и фетотоксическое действие. Было доказано, что гипергомоцистеинемия является одной из причин анэнцефалии и незаращения костномозгового канала (spina bifida
). Аненцефалия приводит к стопроцентной летальности, а
spina bifida
— к развитию серьезных неврологических проблем у ребенка, включая моторный паралич, пожизненную инвалидность и преждевременную смерть. Нельзя исключить прямое токсическое действие избыточного уровня гомоцистеина на нервную систему плода.
Гипергомоцистеинемия может быть не только причиной, но и спутником акушерских осложнений. Предполагается, что в некоторых случаях проблемы могут быть связаны не только с высоким уровнем гомоцистеина, но и с теми состояниями, которые являются причиной развития гипергомоцистеинемии (витаминодефицитные состояния, сопутствующие заболевания и т. д.)
Следует помнить, что гипергомоцистеинемия может сопровождаться развитием вторичных аутоиммунных реакций и в настоящее время рассматривается как одна из причин антифосфолипидного синдрома. Аутоиммунные факторы могут мешать нормальному развитию беременности и после устранения высокого уровня гомоцистеина.
Использованная литература
1. Клинические аспекты гипергомоцистеинемии : монография / В.А. Снежицкий [и др.]; под общей ред. В.А. Снежицкого, В.М. Пы- рочкина. – Гродно : ГрГМУ, 2011. – 292 с. 2. Костюченко Г.И. Гипергомоцистеинемия: клиническое значение, возрастные особенности, диагностика и коррекция // Клиническая геронтология. 2007. №4. URL: https://cyberleninka.ru/article/n/gipergomotsisteinemiya-klinicheskoe-znachenie-vozrastnye-osobennosti-diagnostika-i-korrektsiya (дата обращения: 30.08.2020). 3. РЕКОМЕНДАЦИИ ЕОК/ЕОА ПО ДИАГНОСТИКЕ И ЛЕЧЕНИю ДИСЛИПИДЕМИЙ 2021 Оригинальная публикация European Heart Journal (2016), 37 (39): 2999- 3058, doi:10.1093/eurheartj/ehw272
Показания для анализа крови на гомоцистеин
Определение гомоцистеина проводят для оценки степени риска артериальных или венозных тромбозов, особенно в молодом возрасте. Одновременно определяют уровень витамина В12 и фолиевой кислоты для определения (исключения) гипергомоцистеинемии, возникшей вследствие дефицитов витаминов. Анализ крови на гомоцистеин делают при подозрении у пациента наследственного нарушения метаболизма метионина, включая недостаточность цистатионин-бета-синтазы (гомоцистинурию) и дефицит метилентетрагидрофолатредуктазы и её термолабильных вариантов – недостаточности метионин-синтазы, нарушения метаболизма кобаламина.
Диагностика гипергомоцистеинемии
Для диагностики гипергомоцистеинемии проводится определение уровня гомоцистеина в крови. Для дифференциальной диагностики различных форм гомоцистеинемии иногда используются нагрузочные пробы с метионином (определение уровня гомоцистеина натощак и после нагрузки метионином).
Для выяснения причин гипергомоцистеинемии проводится ДНК-диагностика наследственных дефектов ферментов, участвующих в обмене метионина и фолиевой кислоты, в частности, MTHFR, и определение уровня витаминов B6, B12, B1 и фолиевой кислоты в крови.
При обнаружении высокого уровня гомоцистеина в крови рекомендуется проведение тестов, позволяющих исключить дополнительные факторы риска развития сосудистых и акушерских осложнений. Мы рекомендуем проведение гемостазиограммы, анализа крови на волчаночный антикоагулянт, анализа на антифосфолипидные и анти-ДНК-антитела, антитела к щитовидной железе, антитела к фактору роста нервов и анализ крови на наследственные дефекты гемостаза (лейденскую мутацию и наследственные дефекты протромбина). По показаниям могут быть назначены и другие анализы.
Язва желудка, стеатоз, высокий гомоцистеин и ЛПНП, проблемы с кишечником
Михаил
30 августа 2020
Добрый день! Помогите разобраться в куче симптомов/анализов и что делать дальше. Симптомы: сильная усталость на протяжении нескольких месяцев, сильная дневная сонливость, раздражительность, ломота в мышцах, головокружения, эпизодические повышения давления (не более одного часа), панические атаки, ощущение нехватки кислорода в мозгу, иногда головокружения и затуманенность сознания, заторможенность, трудно сосредоточиться, иногда боль в ногах в области икр (как будто болит внутри ноги), тяжесть в правом боку, «воспаленность глаз», отечность лица, случаи бессонницы, спазмируются мышцы шеи и середины спины, красные пятна на лице под глазами и между глазами и на переднем крае волосяного покрова, метеоризм с запахом гнили, вздутие живота, стул периодически жидкий. Исследования/анализы: 12.08.2020 УЗИ органов брюшной полости: эхографические признаки диффузных изменений паренхимы печени, вероятно по типу жировой дистрофии, хронического панкреатита. Печень увеличена за счет обеих долей: правая доля ВР 177 мм, левая доля 0 толщина 80 мм, ВР 109 мм 13.08.2020 Эзофагогастродуоденоскопия: Диффузный неатрофический гастрит. Множественные острые эрозии и 2 острые язвы желудка. Рубцовая деформация луковицы двенадцатиперстной кишки (вылеченная язва в 2009 году). Бульбит. Экспресс-тест на HP положительный. 14.08.2020 Консультация гастроэнтеролога: Де-нол 120 мг, 2т-2р, до еды за 50 мин, 4 нед. Париет 20 мг, 1т-2р, за 30 мин. до еды, 4 нед. Дюспаталин 200 мг. 1т-2р, за 30 мин до еды, 14 дней Хелинорм 1к-1р, во время еды, 4 нед. Консультация кардиолога: Факторы риска ССЗ: повышен ХС и ЛПНП, снижен ЛПВП (дислипидемия 2А) Дуплексное сканирование брахиоцефальных артерий: Умеренные атеросклеротические изменения брахиоцефальных артерий без признаков их стенозирования. Умеренно выраженная непрямолинейность хода внутренней сонной артерии слева. Фиброэластометрия печени: Фиброза нет, стеатоз 1-й степени (251 dB/m) Анализы кал (привожу только те, где есть отклонения): Дрожжевые грибы – обнаружены Мышечные волокна с исчерненностью – немного Реакция на скрытую кровь – обнаружена (но гемоглобин и гаптоглобин – не обнаружены) Крахмал внутриклеточный – немного Крахмал внеклеточный – немного Лактозонегативная кишечная палочка 10*6 Гемолизирующая кишечная палочка 10*8 Клебсиелла 10*6 Стафилоккок золотистый 10*4 Клостридии 10*6 Анализы кровь (пишу только те, где есть отклонения): Гомоцистеин 13.9 Эстрадиол 45.89 Холестерин общий 5.60 АЛТ 53.2 Холестерин-ЛПНП 4.02 Холестерин-ЛПВП 0.82 Гамма-ГТ 79 Гематокрит 50.8 Тромбоциты 410 Средний объем тромбоцитов 11.3 Тромбокрит 0.47 Базофилы 0.11 Базофилы % 1.1 Лимфоциты 3.82 Лимфоциты% 39.6 Ретикулоциты 96.3 Гастроскопия, сделанная через 2 недели после начала лечения язвы, показала хорошую динамику, поэтому, исходя из анализов крови и кала, добавили к лечению следующие медикаменты: Тербинафин 250 мг. 1т-1р, 10 дней Альфа-нормикс, 2т-2р, 10 дней Гептрал 400 мг, 1т-2р, 14 дней Общее состояние улучшилось мало, остается сильная усталось, сонливость и все симптомы, указанные в самом начале. Язва стала заживать, печень (кажется) в целом в относительной норма, но зловонный метеоризм и вздутие живота никуда не исчезли, головокружения и затуманенность сознания остаются. Куда мне идти теперь? На что могут указывать мои анализы? Начитался про повышенный плохой холестерин и гомоцистеин – стало страшно)) Подскажите, что делать дальше? К какому врачу идти? Гематологу? P.S. Есть также МРТ всего позвоночника от октября 2021 года – остеохондроз, протрузии, спондилоартроз грудного и пояснично-крестцового отделов.
Вопрос закрыт
анализ
печени
анализы кала