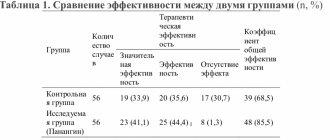
Экспресс-диагностика инфаркта миокарда
ИХА-исследования:
05.09.2018
Шибанов А.Н., Гервазиев Ю.В.
Инфаркт миокарда (ИМ) является одной из основных причин смертности в цивилизованных странах. По данным, представленным на Коллегии Министерства здравоохранения и социального развития в 2008 году, в структуре причин смертности в России ИМ составляет 20% и занимает второе место, лишь немного уступая болезням сосудов головного мозга.
За последние 20 лет мировая медицина достигла больших успехов в лечении сердечно-сосудистых заболеваний, и ИМ в том числе. Такие методы, как тромболитическая терапия, реперфузия сердечной мышцы, баллонная ангиопластика во многих случаях позволяют восстановить кровообращение в сердечной мышце и спасти жизнь больного. Эффективность этих методов решающим образом зависит от времени между моментом возникновения острой сердечной недостаточности и началом проведения лечебных мероприятий. Каждый час задержки значительно снижает вероятность положительного исхода. Поэтому большую роль в успешном лечении ИМ играет своевременная постановка диагноза.
Диагностика ИМ основывается на 3 группах критериев:
- анамнез и физикальное обследование;
- данные инструментальных исследований;
- определение в крови кардиомаркеров: белков, специфичных для инфарктного состояния.
Данные анамнеза заболевания и физикального обследования являются по существу субъективными и не могут служить критериями диагностики ИМ. Целью физикального обследования является в первую очередь исключение внесердечных причин боли в грудной клетке (плеврит, пневмоторакс, миозит, воспалительные заболевания костно–мышечного аппарата, травмы грудной клетки и др.). Кроме того, при физикальном обследовании выявляются заболевания сердца, не связанные с поражением коронарных артерий (перикардит, пороки сердца), а также оценивается стабильность гемодинамики и тяжесть недостаточности кровообращения [1].
Ключевым методом инструментальной диагностики является электрокардиография (ЭКГ). Наиболее надежными электрокардиографическими признаками ИМ являются динамика сегмента ST и изменения зубца Т. Однако до 25% всех ИМ не вызывают никаких изменений на ЭКГ, а от 20% до 30% всех случаев вообще протекают без болевого приступа, особенно у пожилых, а также у больных диабетом и гипертонической болезнью.
Следовательно, определение биохимических маркеров некроза миокарда – необходимый компонент комплексной диагностики ИМ [1].
Национальной академия клинической биохимии по лабораторной медицинской практике США предлагает схему дифференциальной диагностики острого коронарного синдрома, представленную на Рисунке 1 [2].
Рисунок 1. Схема дифференциальной диагностики острого коронарного синдрома.
Белки-маркеры ИМ
При некрозе миокарда содержимое погибшей клетки поступает в общий кровоток и может быть определено в пробах крови. При правильном выборе этих белков (маркеров или, точнее, кардиомаркеров) на основе информации об их концентрации в крови можно поставить правильный диагноз. Выбор маркеров некроза миокарда определяется, в первую очередь, их специфичностью для данного заболевания. Важны также и такие характеристики, как время появления в диагностически значимых концентрациях в крови и время, в течение которого их концентрация сохраняется повышенной. В число биомаркеров миокардиального некроза входят сердечные тропонины I и T (сТnI и сТnT), сердечная фракция креатинкиназы (CK-MB), миоглобин (Myo), изофермент лактатдегидрогеназа-1, трансаминазы и ряд других молекул [3].
Рисунок 2. Структура тропонина I.
Тропонин I — белок, локализованный в сердечной мышце и участвующий в ее сокращении. В мышечной клетке присутствуют три формы тропонинов — I, Т и С, в соотношении 1:1:1. Они входят в состав тропонинового комплекса, который связан с белком тропомиозином. Последний вместе с актином образует тонкие филаменты миоцитов – важнейший компонент сократительного аппарата клеток поперечно-полосатой мускулатуры. Все три тропонина участвуют в кальций-зависимой регуляции акта сокращения – расслабления.
- ТнI — является ингибирующей субъединицей этого комплекса, связывающей актин в период расслабления и тормозящей АТФ-азную активность актомиозина, таким образом предотвращая мышечное сокращение в отсутствие ионов кальция.
- ТнТ — является регуляторной субъединицей, прикрепляющей тропониновый комплекс к тонким филаментам и тем самым участвуя в кальций-регулируемом акте сокращения.
- ТнС – является кальций-связывающей субъединицей и содержит четыре кальций-рецепторных участка.
- ТнI и ТнТ существуют в трех изоформах, уникальных по структуре для каждого типа поперечно-полосатых мышц (быстрых, медленных и сердечных).
Кардиальная изоформа ТнI существенно отличается от изоформ ТнI , локализующихся в скелетной мускулатуре: ТнI содержит дополнительный N-терминальный полипептид, состоящий из тридцати одного аминокислотного остатка. Таким образом, ТнI – абсолютно специфичный миокардиальный протеин. Молекулярный вес ТнI – около 24 000 дальтон.
В диагностике ИМ используются кардиальные изоформы как ТнI, так и ТнТ. Они могут быть отдифференцированы от аналогичных белков скелетных мышц иммунологически, с помощью моноклональных антител, что и используется в методах их иммунотестирования.
Кардиальный ТнС в противоположность ТнI и ТнТ, совершенно идентичен по структуре мышечному ТнС и, следовательно, не является кардиоспецифичным протеином.
Рисунок 3. Структура креатинкиназы.
Креатинкиназа – фермент, осуществляющий превращение фосфокреатина с образованием креатина и АТФ (ресинтез АТФ в реакции трансфосфорилирования АДФ и креатинфосфата), который необходим для мышечного сокращения. Общая активность креатинкиназы складывается из активности изоформ фермента – CK-MM, CK-BB и CK-MB, где М- мышечная субъединица фермента (muscle) и В-мозговая (brain). Изоформа CK-BB в основном присутствует в ткани мозга, легких, в желудке. Изофермент CK-MM характерен для мышечной ткани, а изоформа CK-MB сконцентрирована в ткани сердца. При поражении сердечной мышцы именно эта изоформа выходит из клеток сердца в кровяное русло, что сопровождается увеличением активности изофермента в крови.
Рисунок 4. Структура миоглобина.
Миоглобин — железосодержащий белок мышечных клеток, который отвечает за транспорт кислорода в скелетных мышцах и в мышце сердца. Повышение уровня белка в крови наблюдается через 2 часа после появления боли при ИМ. Уровень миоглобина повышается самым первым из всех кардиомаркеров, степень повышения зависит от площади поражения миокарда. Это самый «короткоживущий» маркер ИМ — нормализация показателя происходит, как правило, за 24 часа. В этом и заключается его уникальная диагностическая ценность. Если уровень миоглобина остается повышенным после острого приступа ИМ – это свидетельство расширение зоны инфаркта. Повторные повышения уровня миоглобина в крови на фоне уже начавшейся нормализации говорит об образовании новых некротических очагов. Таким образом, миоглобин – очень важен для диагностики повторного ИМ. Существенным недостатком этого маркера является его низкая специфичность — он появляется в крови также и при повреждении скелетных мышц.
Другие потенциальные кардиомаркеры (изофермент лактатдегидрогеназа-1, трансаминазы, белок, связывающий жирные кислоты) по разным причинам практически не используются для диагностики ИМ.
Свойства кардиомаркеров можно резюмировать следующим образом:
| Маркер | Молеку-лярный вес | Кардио-специ-фичность | Преимущества | Недостатки | Первое повышение концентрации | Длительность сохранения повышенного уровня |
| CTnT | 37000 | ++++ | Высокая специфичность в отношении ткани сердца. Выявление ИМ в срок до двух недель. | Не является ранним маркером некроза миокарда. Двухфазная кинетика выделения в кровоток затрудняет диагностику повторного ИМ | 3-4 часа | 10-14 дней |
| CTnI | 23500 | ++++ | Высокая специфичность в отношении ткани сердца. Выявление ИМ в срок до 7 дней. | Не является ранним маркером некроза миокарда. | 4-6 часов | 4-7 дней |
| CK-MB | 85000 | +++ | Большой опыт применения в клинике. Прежний «золотой стандарт» для выявления ИМ. | Сниженная специфичность при повреждении скелетных мышц. | 3-4 часа | 24-36 часов |
| Myo | 18000 | Отсут-ствует | Возможность исключения ИМ на ранних этапах. Возможность диагностики повторных инфарктов. | Низкая специфичность при наличии повреждения скелетных мышц и почечной недостаточности. Быстрое выведение из организма. | 1-3 часа | 12-24 часа |
Пациентам с подозрением на острый инфаркт миокарда следует проводить одновременное определение трех кардиомаркеров — тропонина, CK-MB и миоглобина.
В ургентных ситуациях, в частности, в условиях скорой помощи, определять кардиомаркеры предпочтительно экспресс-методом, поскольку, фактор времени на постановку диагноза имеет критическое значение.
В настоящее время единственным методом, позволяющим провести экспресс-определение тропонина, креатинкиназы и миглобина является метод иммунохроматографии (ИХА). Он позволяет вне лабораторных условий и в течение 15 минут выявить маркеры заболеваний.
Принцип иммунохроматографического анализа
Устройство иммунохроматографического теста показано на Рисунке 5.
Рисунок 5. Схематическое изображение иммунохроматографического теста.
Он состоит из следующих элементов: фильтра, мембраны с коньюгатом, хроматографической мембраны, содержащей одну или несколько зон захвата иммунных комплексов и контрольную зону захвата, мембраны абсорбции. Все это устройство помещено в пластиковый корпус, в котором имеется приемное окно. Внешний вид иммунохроматографического теста в разобранном виде показан на Рисунке 6.
Рисунок 6. Вид иммунохроматографического теста со снятым корпусом. Видны предварительный фильтр, мембрана с коньюгатом, хроматографическая мембрана, мембрана абсорбции.
В основе метода лежит технология тонкослойной хроматографии (Рисунок 7). Кровь в объеме 100 мкл (5-6 капель) наносится через специальное приемное окно на подложку для образца. Плазма крови, пройдя через фильтр, под действием капиллярных сил пропитывает полосу, где присутствующие в плазме крови белки-маркеры вступают в реакцию с моноклональнми антителами, меченными коллоидным золотом, образуя комплексы антиген-антитело. Коллоидное золото – специальный краситель, видимый даже в сверхнизких концентрациях.
Рисунок 7. Принцип иммунохроматографического метода.
Далее под действием капиллярных сил эти комплексы двигаются по хроматографической мембране и вступают в реакцию с иммобилизованными антителами в соответствующих зонах против тех же белков. При этом, если целевой белок-маркер присутствует в достаточном количестве, окрашенный коньюгат, связанный с белком, накапливается в зоне иммобилизации антител протв этого белка. Образуется как бы «сэндвич» (рисунок). Свободный коньюгат продвигается по хроматографической мембране и захватывается в контрольной полосе иммобилизованными вторичными антителами. Если в зонах захвата накопится достаточное количество иммунных комплексов, то полосы благодаря частицам коллоидного золота приобретают характерный бордовый оттенок. Контрольная зона окрашивается всегда.
Если в контрольной зоне не появилось чёткой цветной полосы, то результат теста неправилен, и в этом случае образец должен быть повторно протестирован. При этом необходимо использовать новое тестовое устройство.
Если в зонах захвата не содержится ни одной яркой цветной полосы, а контрольная зона показывает такую полосу, то результат теста является отрицательным.
Тест является положительным, если в зонах захвата иммунных комплексов в течение 15 минут появились цветные полосы. Диагностикумы сконструированы таким образом, что едва видимое присутствие окрашенной полосы уже свидетельствует о превышении концентрации белка-маркера над пороговым уровнем.
На Рисунке 8 показано несколько клинических случаев. Исследования проводились в лаборатории «СклифЛаб» НИИ СП им. Н.В. Склифосовского, куда поступали образцы сыворотки больных с подозрением на инфаркт миокарда в период с 18 по 22 мая 2009года. В качестве тест-системы использовали трехкомпонентный кардиотест «ИммунТех» производства фирмы YD Diagnostics, Южная Корея.
Рисунок 8. Примеры результатов анализа кардиомаркеров с использованием иммунохроматографического теста. Объяснения в тексте.
На тесте А мы видим только яркую контрольную полосу, ни один из кардиомаркеров тест не обнаруживает. Такой результат анализа указывает на то, что вероятность инфаркта миокарда у данного пациента невысока. Однако здесь следует указать, что по результатам только иммунохроматографического анализа диагноз ставить нельзя. Необходимо учитывать всю совокупность диагностикой информации. При наличии клинической картины, характерной для инфаркта миокарда исследование на кардиомаркеры следует повторить через 4 и 8 часов.
Тест Б показывает присутствие в крови пациента миоглобина с концентрацией намного выше порога обнаружения, видна очень слабая окраска зоны CK-MB, а тропонин I не обнаружен. Этот результат анализа указывает на то, что риск инфаркта миокарда у пациента довольно высокий. Отсутствие тропонина, возможно, связано с тем, что прошло немного времени с начала процесса некроза кардиомиоцитов и тропонин еще не успел поступить в кровь пациента.
Тест В показывает характерную картину инфаркта миокарда – присутствуют все три кардиомаркера.
На тесте Г мы видим наличие окраски зоны тропонина I, очень слабая окраска зоны креатинкиназы МБ (на пороге обнаружения) и отсутствует миоглобин. Наличие тропонина в крови пациента говорит о том, что процесс некроза кардиомиоцитов имел место. Отсутствие миоглобина и обнаружение креатинкиназы МБ на пороге чувствительности говорит о том, что, по-видимому, инфаркт миокарда имел место более 96 часов назад.
Из приведенных примеров мы видим, насколько повышается эффективность диагностики инфаркта миокарда, когда наряду с традиционными методами диагностики мы применяем метод иммунохроматографического анализа кардиомаркеров. Особенно это эффективно, когда определяется сразу три кардиомаркера и в динамике.
Помимо качественной бесприборной ИХА-диагностики разработаны системы количественного приборного иммунохроматографического анализа. Идея заключается в том, что в этих тестах вместо визуального красителя (коллоидного золота) используется флуоресцентная метка, что увеличивает чувствительность теста, но требует использования специального прибора, который дает возможность количественно оценивать присутствие маркеров. Эти системы также могут работать на цельной крови, время анализа – 15-20 минут. Описанные системы дают возможность проводить диагностику непосредственно в отделении, у постели больного. Однако стоимость диагностики чрезвычайно высока: до тысячи рублей за один анализ. Наиболее известный в России диагностикум количественной ИХА-детекции – система Triage фирмы Biosite (США).
Широкое применение иммунохроматографических методов экспресс-диагностики кардиомаркеров позволит значительно повысить эффективность лечения инфарктов миокарда и снизить смертность. Экспресс-тесты необходимо применять во всех лечебно-профилактических учреждениях, а не только в кардиологических отделениях стационаров. При любом недомогании человек, прежде всего, обращается в поликлинику. При отсутствии у пациента четко выраженной клинической картины инфаркта миокарда и отсутствии четких признаков в кардиограмме не всякий врач примет решение о срочной госпитализации больного. Определение кардиомаркеров в поликлинике позволит в ряде случаев снизить вероятность диагностической ошибки и принять врачу правильное решение. По тем же причинам необходимо иметь экспресс-тесты для диагностики инфаркта миокарда в фельшерско-акушерских пунктах. Положительный результат анализа позволит обоснованно вызвать скорую помощь или бригаду санавиации из ближайшего райцентра. Малые размеры и вес иммунохроматографических тестов позволяют использовать их участковым врачом или врачом общей практики при посещении больного на дому.
Особенно высока актуальность использования необходим иммунохроматографических экспресс-тестов в неотложной медицине.
Очевидно, что применение в этой сфере таких методов диагностики как компьютерная томография, ультразвуковое исследование, различные инвазивные методики и «классические» лабораторные анализы крайне затруднено, поскольку подавляющее большинство неотложных случаев происходит не в условиях стационара, а в «уличных» или «домашних» условиях. К тому же, данные методы часто требуют предварительной подготовки пациента, что в неотложной ситуации просто невыполнимо. В Российской Федерации врач неотложной скорой медицинской помощи, выезжая на вызов, связанный с какой-либо неотложной ситуацией, может основываться только на данных физикального обследования и результатов электрокардиографии, которая информативна далеко не во всех случаях острого инфаркта миокарда.
В настоящее время требованиям, предъявляемым к диагностическим методам в условиях неотложной медицины, а это, прежде всего быстрые и точные результаты, наиболее полно удовлетворяет именно ИХА экспресс-диагностика. Данная диагностика может быть проведена непосредственно в месте оказания помощи пациенту. А учитывая, что время доставки больного машиной скорой помощи до больницы составляет, как правило, не менее 30 минут, можно утверждать, что экспресс-диагностика поможет сохранить жизнь многим пациентам, не говоря уже о снижении общей стоимости лечения.
Однако использование ИХА рекомендуется не только в «походно-полевых» условиях. В 2006 году американские врачи сравнили экономические показатели лечения больных в стационаре в случае определения кардиомаркеров с помощью иммунохроматографической экспресс-диагностики и в случае определения их в лаборатории. Оказалось, что несмотря на относительную дороговизну экспресс-диагностики, общие затраты на лечение снизились благодаря уменьшению времени от забора крови до получения результата. Благодаря этому снизились затраты на лечебные процедуры, фармакологические препараты, уменьшилось время пребывания больных в стационаре.
Таким образом, иммунохроматографическая экспресс-диагностика может быть рекомендована для диагностики ИМ как в лечебных учреждениях, так и в неотложной медицине.
Список литературы.
- Рекомендации по лечению острого коронарного синдрома без стойкого подъема сегмента ST на ЭКГ. Утверждены на Российском национальном конгрессе кардиологов 11 октября 2001 г.// https://www.cardiosite.ru/medical/recom-ostcorsin.asp
- Morrow DA, Cannon CP, Jessa RL et al. National Academy of Clinical Biochemistry Laboratory Medicine Practice Guidelines: Clinical Characteristics and Utilization of Biochemical Markers in Acute Coronary Syndromes //Clinical Chemistry 2007. V.53(4). P.552-574.
- Сапрыгин ДБ. Современный статус применения миокардиальных биомаркеров некроза при остром коронарном синдроме. //Лабораторная медицина 2009. Т.10 С.35-38.
- Apple FS, Chung AY, Kogut ME et al. Decreased patient charges following implementation of point-of-care cardiac troponin monitoring in acute coronary syndrome patients in a community hospital cardiology unit. //Clin Chim Acta. 2006. V.370(1-2). P.191-195.
Теги: Кардиотест, Диагностика, Профилактика инфаркта, Шибанов А.Н., Тропонины, Трехкомпонентный Кардиотест «ИммунТех»
« Назад к списку статей Поделиться в
Дифференциальная диагностика стенокардии и других сердечно-сосудистых заболеваний
Врач- кардиолог отделения кардиологии №1 Вербицкий В.Л.
У некоторых больных с типичной клиникой стенокардии и положительными нагрузочными пробами (по объективным критериям) при коронарографии не находят каких-либо изменений в коронарных артериях; у таких больных нет признаков и спонтанной стенокардии. В этих случаях можно говорить об ИБС при неизмененных коронарных артериях. В англоязычной литературе этот вид патологии называют «синдром икс».Специальные исследования показывают, что у этих больных значительно снижена способность коронарных артерий к дилатации, что обнаруживается при оценке коронарного кровотока с помощью радионуклидов аргона или рубидия в условиях дипиридамоловой пробы. При биопсии миокарда у этих больных находят методом электронной микроскопии дегенеративные изменения в кардио-миоцитах. Таким образом, и снижение коронарного резерва, и данные биопсии позволяют думать о «синдроме икс», как о начальных проявлениях дилатационной кар-диомиопатии. Этот диагноз становится еще достовернее, если у больных появляется стойкая или преходящая (появляющаяся на нагрузках) блокада левой ветви пучка Гиса.
При синдроме пролапса митрального клапана бывает давящая или жгучая боль в третьем—четвертом меж-реберье слева от грудины. Значительно реже боль локализуется позади грудины или мечевидного отростка. Неинтенсивная боль может продолжаться часами, усиливаясь после физических и эмоциональных нагрузок. В момент усиления боль может охватывать всю область сердца. У части больных боль купируется нитроглицерином. Боль часто сочетается с нарушениями ритма сердца (экстрасистолия, мерцательная аритмия, атриовентрику-лярная блокада).Предполагают, что пролапс митрального клапана предрасполагает к спазму коронарных артерий. Этот синдром чаще встречается у больных астенического телосложения с плоской грудной клеткой — с уменьшенным ее переднезадним размером. У больных с пролапсом митрального клапана часто выявляются нарушения сегмента ST и зубца Т, особенно при проведении пробы с физической нагрузкой. На ФКГ и при ауксультации у больных выявляется мезосистоли-ческий шум на верхушке, которому часто предшествует мезосистолический щелчок. Диагностика пролапса митрального клапана значительно улучшилась благодаря широкому применению в клинике ультразвуковых методов исследования сердца. Оно позволяет обнаружить выпадение в предсердие одной или обеих створок митрального ‘клапана. Ценные диагностические данные позволяет получить вентрикулография. Установление диагноза пролапса митрального клапана не исключает одновременного наличия у больного стенозирующего коронарного атеросклероза.
Клапанный стеноз устья аорты, как и артериальная гипертензия, ведет к перегрузке и гипертрофии левого желудочка, повышая потребность миокарда в кислороде. Наблюдаемое при пороке этого типа укорочение периода диастолического наполнения левого желудочка способствует уменьшению коронарного кровотока. Эти больные часто предъявляют жалобы на боль в области сердца. На ранних стадиях заболевания они носят характер кардиалгии, а при выраженном аортальном стенозе возникают типичные приступы стенокардии.Если у больных стенокардией выслушивается систолический шум на аорте, то необходимо проведение всех доступных диагностических исследований, направленных на выявление аортального стеноза. Диагноз аортального стеноза ставят на основании характерного систолического шума (ромбовидный шум на фонокардиограмме), физи-кальных, рентгенологических и электрокардиографических признаков гипертрофии левого желудочка. Рентгенологически часто выявляется обызвествление аортального клапана.Большое дифференциально-диагностическое значение имеют данные эхокардиографического исследования. Выявление аортального стеноза не исключает одновременного наличия атеросклероза коронарных артерий. Аортальный стеноз у больного стенокардией, сочетающийся с приступами сердечной астмы, имеет тяжелый прогноз.
При митральном пороке сердца больные нередко предъявляют жалобы на боль в области сердца, у некоторых неотличимую от стенокардии. Причиной этой боли может быть характерная для митрального стеноза легочная гипертензия, патогенетически связанная с недостаточностью кровоснабжения гипертрофированного правого желудочка. Иногда болевые ощущения имеют невротическую основу, но типичные приступы стенокардии с высокой вероятностью указывают на сопутствующее стенози-рующее поражение коронарных артерий сердца, что подтверждается данными коронароангиографии.При проведении дифференциальной диагностики стенокардии нужно исключать аорталгии — боль, сопровождающую воспалительные и дегенеративные заболевания аорты. При редком в наше время сифилитическом аортите возникает аортальная недостаточность, патологический процесс также захватывает устья коронарных артерий сердца, что может сопровождаться типичными приступами стенокардии. При неспецифическом аорто-артериите типичная стенокардия отмечается редко, характерна длительная боль в области сердца без иррадиации.
При аневризме дуги аорты поставить правильный диагноз помогают многочисленные сопутствующие симптомы, вызванные сдавлением соседних органов (кашель, дисфагия, осиплость, нарушения зрения, обмороки, асимметричный пульс, сдавление верхней полой вены).При расслоении аорты боль с самого начала имеет максимальную интенсивность. Характерна самая широкая иррадиация: боль, начавшись за грудиной, затем ирради-ирует в шею, спину, в область живота, вдоль позвоночника и даже в ноги. «Паучьи» пальцы и другие признаки синдрома Марфана могут навести врача на мысль о связи боли в грудной клетке с расслоением аорты, к которому эти больные предрасположены.
Боль в области сердца является самым частым и одним из ранних симптомов миокардита. Они разнообразны, в отличие от стенокардии длятся часами и сутками. В остром периоде болезни интенсивность боли может меняться, но боль практически постоянная. При диагностике необходимо учитывать связь с перенесенной недавно инфекцией, повышение температуры, лейкоцитоз, увеличение обоих желудочков сердца. При более или менее длительном течении обязательными симптомами миокардита становятся кардиомегалия и сердечная недостаточность. Дифференциально-диагностические трудности чаще возникают при нетяжелом поражении сердца, когда после ангины, гриппа или другой инфекции появляются неприятные ощущения в области сердца, сопровождающиеся изменениями конечной части желудочкового комплекса ЭКГ. У больных отмечается наклонность к тахикардии и одышке, выслушивается систолический шум. Чаще эти симптомы — проявления инфекционно-аллергического миокардита, постепенно они претерпевают обратное развитие.
Боль в области сердца — частое явление у лиц, страдающих алкоголизмом. При этом часто ставят диагноз ИБС, а болевые ощущения расценивают как стенокардию. Затруднения в диагностике связаны с тем, что больные скрывают злоупотребление алкоголем. На ЭКГ часто выявляются неспецифические изменения сегмента ST и зубца Т. Велоэргометрическая проба может быть положительной. При рентгенографии выявляется расширение границ сердца. На эхокардиограмме устанавливают дилатацию левого желудочка. Динамическое наблюдение за больными показывает утяжеление поражения миокарда и появление тяжелых аритмий, спровоцированных большим количеством алкоголя. Диагностика алкогольной кардиопатии облегчается при одновременных признаках поражения печени. Многие сердечно-сосудистые расстройства у этих больных связаны с вегетативными нарушениями, которые проявляются весьма рано, еще до развития тяжелого поражения миокарда. При коронарографии, как правило, стенозирующие поражения коронарных артерий не выявляются.
За ИБС очень часто принимают кардиалгический синдром у больных нейроциркуляторной дистонией (нами использовано одно из многих обозначений заболевания). Кардиалгический синдром при нейроциркуляторной дис-тонии длительный и упорный. Боль в основном колющая или ноющая, локализуется главным образом в области верхушки сердца или во втором—четвертом межреберье слева от грудины. Боль купируется или уменьшается приемом валокордина, валидола, седативных препаратов, при применении горчичников.
Вегетативно-дистонический синдром при нейроциркуляторной дистонии проявляется лабильностью пульса и АД, периферическими сосудистыми нарушениями, вегетативно-сосудистыми пароксизмами преимущественно симпатико-адреналового генеза. Астенический синдром характеризуется как физической, так и интеллектуальной истощае-мостью, значительным снижением работоспособности. Слабость (неврогенной природы) проявляется прежде всего в утренние часы. В течение дня ощущение слабости и усталости может возрастать, заставляя больных ложиться в постель. Для нейроциркуляторной дистонии характерен синдром невротических дыхательных расстройств: ощущение нехватки воздуха, неудовлетворенность вдохом и зевота, потребность периодически делать глубокие вдохи. Иногда на первое место выходит ощущение удушья или комка в горле. Реже встречаются периоды «пароксизмальной одышки невротика».Яйца с нейроциркуляторной дистонией никогда не чувствуют себя полностью здоровыми, у них всегда выявляется какой-либо синдром или сочетание нескольких. Начало или обострение заболевания, как правило, связано со стрессовой ситуацией (психическое и физическое перенапряжение), реже с инфекционным воздействием или с гормональной перестройкой (беременность, аборт, дизовариальные расстройства, климакс).
Длительное существование сердечно-сосудистых расстройств без четкой органической патологии сердца склоняет в пользу диагноза нейроциркуляторной дистонии. Изменения ЭКГ касаются только конечной части желудочкового комплекса. При нормальных размерах сердца и нормальном положении электрической оси регистрируются двухфазные или отрицательные зубцы Т, особенно в грудных отведениях.Чтобы точнее интерпретировать нарушения ЭКГ, предложен ряд функциональных и фармакологических проб. Пробы с гипервентиляцией и ортостатическая приводят к появлению или углублению изоэлектрических или отрицательных зубцов Т в грудных отведениях. После прекращения пробы ЭКГ приближается к исходному уровню. Пробы с пропранололом и хлоридом калия при положительных результатах характеризуются переходом отрицательного или двухфазного зубца Т в положительный. Положительные результаты пробы чаще наблюдаются при нейроциркуляторной дистонии, указывая, что изменения конечной части желудочкового комплекса связаны с функциональными нарушениями. Однако не следует переоценивать дифференциально-диагностическое значение этихпроб. Положительная проба с пропранололом скорее говорит о повышенной активности симпатико-адреналовой системы, что бывает и при коронарной патологии. Вело-эргометрическая проба у большинства больных отрицательная. Больные часто отказываются ее проводить до достижения диагностических критериев из-за боязни или усталости. В этих случаях большую ценность приобретают другие нагрузочные пробы. Дипиридамоловая проба у’этих больных, как правило, отрицательна. Изопротереноловая проба изредка бывает ложноположительной при гипер-симпатикотонии. Большую диагностическую ценность имеет чреспищеводная электрическая стимуляция предсердий.
У больных этой категории крайне важно проведение всего комплекса нагрузочных проб. Если все пробы отрицательны, то диагноз ИБС с уверенностью снимается. Если часть проб положительна, то больным необходимо сделать коронарографию. Исключение коронарной патологии позволяет более четко сформулировать диагноз и выбрать лечение.
При установлении диагноза нейроциркуляторной дистонии нужно учитывать возможные варианты течения заболевания (от легкого до тяжелого). Для легкого характерны относительная моносимптоматика, возможно спонтанное исчезновение симптомов, сохранение трубоспособ-ности. ЭКГ, как правило, изменена незначительно. Лекарственная терапия часто не нужна. Среднетяжелое заболевание длительное, с обилием симптомов, снижением или временной утратой нетрудоспособности; больным необходима медикаментозная терапия. Тяжелое течение характеризуется стойкостью и множественностью патологических симптомов без тенденции их к исчезновению, трудоспособность снижена.
Тяжесть клинических проявлений нейроциркуляторной дистонии определяется главным образом выраженностью тахикардиального и астенического синдромов, а также наличием вегетативно-сосудистых пароксизмов, присоединением кардиофобии и других выраженных психоэмоциональных расстройств. Среди множества жалоб больного нейроциркуляторной дистонией нужно выделять скупые, но вполне поддающиеся идентификации симптомы стенокардии напряжения. Надо учитывать возможность сочетания ИБС и нейроциркуляторной дисточнии, что дает возможность поставить оба диагноза одновременно. Обычно в таких случаях врач опирается на данные коронарографии.