Исследование системы свертывания крови — один из важных диагностических факторов наблюдения беременности. Для этого существует особый пакет лабораторных показателей — коагулограмма. Но в некоторых случаях, например, при ЭКО, проблемах с вынашиванием или зачатием врач назначает дополнительное обследование. В перечень таких анализов и входит Д-димер — определение в крови продуктов распада фибрина, приводящих к повышенному риску тромбообразования.
Сдать анализ на Д-димер вы можете в нашей клинике или на дому с 9 до 13.00 в рабочие дни.
Что такое D-димер
Д-димеры представляют собой небольшие белковые фрагменты. Они образуются при расщеплении фибрина — вещества, синтез которого происходит в печени при распаде тромба.
Зачем нужно делать анализ на Д-димер
Во время беременности в организме женщины происходит ряд гормональных изменений, которые влияют на многие органы и системы, в том числе и на систему гемостаза (свертывания крови). Поэтому повышенный уровень Д-димера является физиологической нормой. Тем не менее его уровень желательно постоянно контролировать и при существенном повышении срочно принимать меры для предотвращения тромбоза. При варикозном расширении вен (а оно наблюдается как минимум у трети беременных) нарушения свертываемости крови могут привести к серьезным, порой угрожающим жизни матери и ребенка, последствиям.
В настоящее время лечение беременных препаратами, влияющими на систему гемостаза, широко распространено. С трудом найдется пациентка, которой бы за 40 нед беременности не назначали дипиридамол. Распространяется практика «коррекции» некоторых показателей гемостазиограммы антикоагулянтами. По-разному, зачастую совершенно произвольно, определяются продолжительность лечения, сочетание используемых препаратов, отсутствуют лабораторные методы контроля за лечением, доказывающие эффективность и безопасность дозировок антикоагулянтов. Не последнее место занимает и стоимость лечения. Физиологической реакцией организма на беременность является гиперкоагуляция в прокоагулянтном звене системы гемостаза, вероятно, с адекватным ответом антикоагулянтного звена, который трудно оценить ввиду ограниченных возможностей современной клинической биологии. Важно, что уровни маркеров гиперкоагуляции не коррелируют с уровнем клинического риска тромбоза у беременных группы высокого риска развития венозной тромбоэмболии (ВТЭ) [7].
Рациональная антикоагулянтная терапия беременных представляется нам системой лечения по определенным показаниям с соответствующим лабораторным контролем для коррекции показателей гомеостаза у беременной и предупреждения акушерских осложнений, тромбозов и кровотечений. Предполагается использование дозировок препаратов, фармакологическое действие которых хорошо известно, на срок, необходимый для реализации терапевтического эффекта.
За последние 3 десятилетия существует стойкая тенденция к росту материнской смертности от ВТЭ. Кроме того, в большинстве промышленно развитых стран увеличивается возраст рожающих женщин, растет доля беременных, страдающих тяжелой экстрагенитальной патологией. Успехи современной медицины приводят к увеличению продолжительности жизни пациенток и способствуют наступлению беременности у женщин с системными заболеваниями соединительной ткани, онкологическими заболеваниями, патологией сердечно-сосудистой системы, органов дыхания, эндокринной патологией, болезнями системы крови, антифосфолипидным синдромом и т.д. Правильная диагностика и лечение позволяют улучшить перинатальные исходы при таких тяжелых осложнениях беременности, как привычное невынашивание, синдром задержки внутриутробного роста плода, гестоз. Все перечисленные ситуации связаны с интенсификацией внутрисосудистого тромбообразования как в сосудистом русле беременной, так и в системе маточно-плацентарно-плодового кровотока, поэтому использование коагулогически активных веществ является патогенетически обоснованным. При назначении антикоагулянтов следует помнить, что механизмы тромбообразования различны в артериальном и венозном отделах сосудистого русла, в макрососудах и системе микроциркуляции (дистальнее уровня прекапиллярного сфинктера).
К контингенту беременных, которым показана антикоагулянтная терапия, относятся пациентки с:
1) тромбозом глубоких вен и тромбоэмболией легочной артерии во время настоящей беременности,
2) механическими клапанами сердца,
3) антифосфолипидным синдромом (при корректно поставленном диагнозе),
4) при тромбофилии: дефекте антитромбина-III, сочетании наследственных тромбофилий, таких как дефицит белков S и C, резистентность к активированному белку С в связи с лейденской мутацией FV, гиперпротромбинемия в связи с мутацией протромбина G20210A, гипергомоцистеинемия, мутация в ингибиторе активатора плазминогена I типа,
5) проявлением артериального тромбоза,
6) неразвивающейся беременностью и снижением числа тромбоцитов и/или фибриногена при их подготовке к опорожнению полости матки,
7) фетоплацентарной недостаточностью, подтвержденной результатами фетометрии, допплеровского исследования и/или гормональных исследований и/или с помощью кардиотокографии.
Целью антикоагулянтного лечения являются предупреждение тромбоэмболических осложнений, кровотечений, улучшение циркуляции крови в системе мать-плацента-плод, обеспечение неосложненного течения и пролонгирования беременности.
По нашему мнению, необходимым и достаточным приемом для профилактики тромбоэмболической болезни (ТЭБ) является использование балльной шкалы оценки риска и назначение антикоагулянтной профилактики, как это практикуется в общехирургической практике [9].
Оценка 1 балл дается при возрасте старше 40 лет, массе тела более 80 кг, наличии полостной хирургической операции в анамнезе, после которой прошло менее 6 мес, значительном варикозном расширении вен нижних конечностей, недавней иммобилизации. В 2 балла оцениваются соблюдение постельного режима более 3 сут, хроническая обструктивная болезнь легких в тяжелой стадии, воспаление кишечного тракта, тяжелая инфекция (пневмония), состояние после родоразрешения (в пределах 1 мес), применение оральных контрацептивов или гормональной заместительной терапии. В 3 балла оцениваются наличие онкологического заболевания, сердечной недостаточности, перенесенного менее 3 мес назад инфаркта миокарда, наличие в анамнезе эпизода ТЭБ. При сумме 5 баллов и более назначают профилактически эноксапарин в дозе 40 мг однократно подкожно до полной мобилизации пациентки, продолжительность лечения до 2 нед.
Факторы риска ВТЭ у беременных объединяют 2 группы [14]. В 1-ю группу входят факторы, касающиеся самой пациентки: возраст старше 35 лет, ожирение (индекс массы тела более 29 кг/м2) в ранние сроки беременности, тромбофилия, венозные тромбоэмболии в анамнезе, выраженное варикозное расширение вен нижних конечностей, серьезные экстрагенитальные заболевания, например нефротический синдром, наличие инфекции либо воспалительного процесса, иммобилизация, параплегия, гиподинамия при длительных путешествиях, дегидратация, внутривенное введение наркотиков, синдром гиперстимуляции яичников. Во 2-ю группу включены факторы, составляющие осложнения беременности: кесарево сечение, особенно экстренное у роженицы, оперативные роды через естественные родовые пути, массивное акушерское кровотечение, рвота беременных, гестоз.
Более 12 лет назад появилась работа [23] о достоверно бóльших перинатальных потерях у пациенток с такими видами тромбофилии, как дефицит антитромбина-III, белка S, белка С, лейденской мутации FV.
M. de Swiet [29] обращает внимание на возраст беременных и увеличение частоты ТЭБ у беременных старше 40 лет (в 100 раз по сравнению с группой в возрасте 20-25 лет). Дополнительными факторами риска являются избыточная масса тела и наличие в анамнезе более 3 беременностей, оперативные роды (кесарево сечение), подавление лактации эстрогенами. Антенатальные факторы риска ТЭБ включают экстракорпоральное оплодотворение, гестационный диабет, многоплодную беременность и возраст матери старше 35 лет, а постнатальные — гестоз, эклампсию, предлежание плаценты, отслойку плаценты и кесарево сечение [17] .
Методом подтверждения диагноза тромбоза глубоких вен нижней конечности у беременных является компрессионная ультрасонография, а эмболии легочной артерии — вентиляционно-перфузионное сканирование легких [13]. Низкая специфичность D-димера не позволяет использовать этот лабораторный показатель у беременных в качестве лабораторного теста подтверждения ТЭБ [11, 13, 22].
При определении режима лечения обязательно должны соблюдаться следующие условия: во-первых, безопасность препарата для плода и матери; во-вторых, эффективность применяемого режима лечения и/или профилактики, в-третьих, дозировки для начального курса лечения и поддерживающей терапии во время беременности, родов и послеродового периода [13].
Рассмотрим наиболее часто применяемые препараты антикоагулянтного действия, используемые в акушерской практике.
Нефракционированный гепарин (НФГ).
НФГ получают из слизистой оболочки кишечника свиней либо из легких крупного рогатого скота. Препараты различных фирм имеют свои особенности фармакодинамики, что, впрочем, нивелируется тем, что дозировки препарата подбираются в зависимости от реакции системы гемокоагуляции пациентки.
А. Постоянное внутривенное введение.
Успех лечения НФГ зависит от достаточной начальной дозы, которая должна составлять по меньшей мере 30 000-35 000 ЕД/сут [13]. Этот режим лечения используется в острых случаях с обязательным контролем за эффективностью и безопасностью лечения с помощью лабораторного теста — показателя активированного частичного тромбопластинового времени (АЧТВ) [29].
Б. Подкожное прерывистое введение
[13]:
а) мини-дозы НФГ: по 5000 ЕД каждые 12 ч без лабораторного контроля;
б) умеренные дозы НФГ: подкожно каждые 12 ч с контролем изменения содержания антифактора Ха до 0,1-0,3 ЕД/мл через 6 ч после инъекции;
в) адаптированные дозы НФГ: подкожно каждые 12 ч, контролируя изменения показателя АЧТВ до величин, превышающих в 1,5-2 раза нормальные, через 6 ч после инъекции.
В. Ингаляции
[1].
Показания к назначению ингаляций гепарина:
1) профилактика присоединения акушерских осложнений: гестоза, фетоплацентарной недостаточности;
2) наличие гестоза легкой или средней степени тяжести;
3) декомпенсация сахарного диабета;
4) лечение фетоплацентарной недостаточности.
Ингаляции проводят с помощью ультразвукового ингалятора, разводя гепарин дистиллированной водой 1:4, ингаляции проводят 2 раза в сутки с интервалом 12 ч. При профилактике гестоза суточная доза составляет 300 ЕД/кг, длительность курса — 7 дней, требуется 2-3 курса, интервал между курсами 2 дня, необходимо прекратить лечение за 10 дней до родоразрешения; при других показаниях суточная доза составляет 500 ЕД/кг, продолжительность курса — 21 день, количество курсов — 1-2, интервал между курсами — 2 нед, необходимо прекратить лечение за 14 дней до родоразрешения.
Низкомолекулярные гепарины (НМГ).
НМГ (табл. 1)
получаются путем деполимеризации НФГ азотистой кислотой либо индукцией бензилового кольца и щелочным гидролизом, либо деполимеризацией из амилового нитрата, либо перекисным окислением и, наконец, расщеплением гепариназой [26].
В целом рациональная терапия гепаринами представлена в табл. 2.
Как и НФГ, НМГ не проникают сквозь плацентарный барьер в молоко, являются безопасными для плода и считаются средством выбора для лечения ВТЭ у беременных [10, 13].
Профилактическая доза НМГ тинзапарина, по мнению K. Khasia и соавт. [18], должна составлять 4500 ЕД/сут при массе тела пациентки менее 100 кг и 5000 ЕД/кг при массе более 100 кг. Авторы полагают, что окончательная доза НМГ должна быть установлена с учетом активности антифактора Ха.
В 2001-2005 гг. основным НМГ в Дании, применяемым во время беременности, являлся тинзапарин — 95,2% наблюдений, а на долю далтепарина натрия пришлось 4,8% [4]. По данным A. Andersen и соавт. [4], показаниями к лечению беременных низкомолекулярными гепаринами в Дании являлись эпизод тромбоэмболии с/или без тромбофилии — 37,3%, перинатальные потери и врожденная тромбофилия — 35%, привычный выкидыш и врожденная тромбофилия — 7,2%, другие причины — 20,5%.
Принимая во внимание плохие перинатальные исходы для матери и плода у пациенток с дефицитом антитромбина III, S. Schulman [27] с целью профилактики тромботических осложнений рекомендует назначение НФГ в дозировке, способной увеличить АЧТВ до 1,3-1,5 референсных значений через 5-6 ч после инъекции при трехкратных подкожных инъекциях либо использование НМГ с показателем активности антифактора Ха, равным 0,1-0,2 ЕД/мл.
Антивитамины К (варфарин).
Применение антивитаминов К у беременных ограничивается страхом врачей перед возможным тератогенным действием препаратов и риском кровотечения как у матери, так и у плода. Недостатками препаратов следует также считать замедленное начало действия и последействие препарата, непредсказуемый клинический эффект в зависимости от дозы, что требует лабораторного контроля, узкий «терапевтический коридор», множественные взаимодействия с лекарственными средствами и пищевыми продуктами, изменяющие действие препарата [5]. Антивитамины К применяются у беременных с искусственными клапанами сердца, при аллергических реакциях на гепарин, при наличии высокого титра антифосфолипидных антител [29]. Антивитамины К не секретируются в материнское молоко и могут использоваться у кормящих женщин [16].
При сравнении режимов антикоагулянтной терапии у беременных с искусственным клапаном сердца наименьшее число тромбоэмболических и геморрагических осложнений отмечено при тактике использования гепарина в ранние сроки беременности и в период органогенеза до 12 нед, затем при переводе беременных на прием непрямых антикоагулянтов с возвращением к гепаринотерапии перед родами [24].
Многие лекарственные средства влияют на эффективность антивитаминов К; усиливают эффект такие препараты, как эритромицин, ко-тримоксазол, флуконазол, изониазид, метронидазол, амиодарон, клофибрат, пропафенон, пропранолол, сульфинперазон, фенилбутазон, пироксикам, этиловый спирт, циметидин, омепразол. Ослабляют действие антивитаминов К гризеофульвин, нафциллин, рифампин, холестирамин, барбитураты, карбамазепин, хлордиазепоксид, сукральфат [15].
Аспирин.
Действие аспирина заключается в необратимом ингибировании циклооксигеназы, что повреждает синтез тромбоксана А2 и метаболизм простагландинов. При этом агрегация тромбоцитов, индуцированная коллагеном, аденозиндифосфатом, тромбином и тромбоксаном А2, снижается [6].
Лечение аспирином обычно проводится вместе с терапией гепарином. Доказана эффективность применения 75 мг аспирина с подкожным введением 5000 ЕД гепарина с интервалом 12 ч либо в сочетании с применением НМГ парнапарина в дозе 0,3 мл подкожно у пациенток с наличием антифосфолипидных антител и привычным выкидышем для улучшения перинатальных показателей [25].
Японские исследователи в 20 подтвержденных наблюдениях ВТЭ у беременных (срок до 30 нед) использовали НФГ с контролем АЧТВ для подбора адекватной дозы с последующим переходом на низкие дозы аспирина после исчезновения тромба; при этом ни у одной пациентки не применяли установку фильтра в нижней полой вене. Необходимость продолжения антикоагулянтного лечения после исчезновения тромбоза отсутствует в японской популяции ввиду того, что отсутствует резистентность к активированному белку С [21].
Существенным вопросом клинической практики является тактика использования антикоагулянтов в родах и после них. Большинство исследователей рекомендуют отмену гепарина за 24 ч до родовозбуждения при программированных родах, а в группе очень высокого риска развития тромбоэмболических осложнений внутривенное введение НФГ отменяют за 4-6 ч до родовозбуждения; при избыточной дозировке гепарина возможно использование раствора протамина сульфата, возобновление антикоагулянтной терапии возможно через 12 ч после родов [13]. В группах высокого риска (например, первый эпизод ТЭБ при беременности, механический клапан сердца с явлениями тромбоза, множественная врожденная тромбофилия с явлениями венозного тромбоза) допустима гепаринотерапия в родах, например, подкожно по 7500 ЕД 2 раза в день [29]. При затяжных родах более 18 ч и если в ближайшие 3 ч роды не произойдут, возможно использование профилактической дозы НМГ [16]. Разработана оригинальная система [19], которая обеспечивает антикоагуляцию в родах у пациенток группы высокого риска, получающих НМГ в лечебной дозе, без опасности геморрагических осложнений.
Накануне программированных родов или планового кесарева сечения начинается инфузия инфузоматом раствора НФГ 15 000 ЕД/24 ч — 625 ЕД/ч, а вечером подкожную инъекцию препарата отменяют.
За 4 ч до родоразрешения (с началом активной фазы родов) или проведения эпидуральной аналгезии при абдоминальном родоразрешении инфузию прекращают и возобновляют через 2-4 ч после родоразрешения.
Лабораторный контроль за лечением антикоагулянтами.
Использование АЧТВ.
При режиме контроля непрерывного внутривенного введения гепарина АЧТВ должно быть увеличено в 1,5-2 раза от нормального через 6 ч от начала терапии.
Определение показателя активности антифактора Ха.
Сложность использования НМГ в клинической практике обусловлена тем, что эти препараты могут обладать значительной антитромботической активностью in vivo без проявления антикоагулянтного эффекта при лабораторном исследовании в пробирке [26].
Контроль за лечением НМГ осуществляется ежемесячно, при этом уровень антифактора Xа должен составлять 0,5-1,2 ЕД/мл (максимальное значение — спустя 3-4 ч после инъекции) при двукратном назначении препарата и 1,0-2,0 ЕД/мл, если препарат назначается один раз в сутки [13, 16]. При уровне активности антифактора Xа менее 0,4 ЕД/мл у пациентки не будет кровотечения, обусловленного приемом гепарина [29].
При наличии искусственных механических клапанов сердца у беременных при двукратном подкожном введении НМГ пиковые концентрации антифактора Ха должны составлять 0,7-0,8 ЕД/мл и параллельно должна выполняться эхокардиография [2].
Профилактическая доза тинзапарина должна составлять 0,5-0,8 ЕД/мл в течение 2 ч после инъекции, причем при маленькой дозе переходят на подбор дозы по вышеупомянутому показателю [18].
Существует мнение [28] о низкой прогностической ценности определения активности антифактора Хa в отношении прогрессирования тромбоза и риска развития кровотечения.
Контроль за лечением непрямыми антикоагулянтами-антивитаминами К.
Для контроля за лечением варфарином в настоящее время применяется международное нормализованное отношение (МНО — INR,
international normalized ratio
). МНО — это отношение протромбинового времени пациента к контрольному протромбиновому времени, возведенное в степень международного индекса чувствительности используемого тромбопластина. Эти сложности нужны для стандартизации лабораторного реагента тромбопластина, что позволяет сравнивать величины МНО, полученные в любом месте земного шара. Для предотвращения тромбозов МНО должно составлять 2-3, исключение составляют пациентки с механическими клапанами сердца и с антифосфолипидным синдромом, у которых этот показатель должен соответствовать 3-4 [20].
Осложнения антикоагулянтной терапии.
К осложнениям при лечении гепарином относятся кровотечения, гепарининдуцированная тромбоцитопения, остеопороз [13]. M. Damodaran и соавт. [10] сообщают о большей кровопотере в родах и о достоверно большем числе врожденных аномалий развития у плодов беременных, получавших НМГ, поэтому, по мнению авторов, лечение НМГ должно основываться на четких клинических показаниях.
В 166 наблюдениях длительного использования НМГ не было случаев развития тромбоэмболических эпизодов либо значительных гематом, как и переломов вследствие остеопороза при хороших перинатальных показателях, хотя в 9,6% наблюдений имелась повышенная кровопотеря после родов [4].
До настоящего времени остается открытым вопрос о профилактическом лечении антикоагулянтами. Их все шире применяют для улучшения перинатальных исходов беременности при сосудистых плацентарных осложнениях [8]. Для решения вопроса о профилактическом применении антикоагулянтов у беременных их делят на группы высокого и низкого риска. В отсутствие других факторов риска повторный эпизод тромбоза или тромбоэмболии у беременных имеет вероятность возникновения, равную 12%, поэтому либо ограничиваются наблюдением, либо назначают аспирин в низких (до 100 мг/сут) дозах. У пациенток группы высокого риска отмечаются более одного эпизода ВТЭ за беременность, тромбофилия, семейный анамнез ТЭБ. Таким пациенткам с момента подтверждения беременности проводятся подкожные инъекции НФГ либо НМГ [29]. Профилактическое назначение НМГ и его эффективность оценены M. Aldea и соавт. [3] у 14 624 беременных. Факторами риска являлись ожирение, наличие варикозно-расширенных вен, миомы матки, артериальной гипертензии, кардиопатии, эпизодов венозного тромбоза в анамнезе. 22% пациенток получали профилактическое лечение НМГ, лечение антикоагулянтами отменяли за 12 ч и возобновляли через 12 ч после родов. Неэффективность гепаринопрофилактики (4 случая венозного тромбоза на фоне применения препаратов) авторы связывают с применением малой дозы препарата (один раз в сутки) и обращают внимание на применение НМГ по показаниям — при имеющихся факторах риска, чтобы чрезмерно не увеличивать стоимость лечения. Вопрос о дозировке гепарина при его профилактическом применении у пациенток с врожденным дефицитом антитромбина поднимается в публикации I. Dubedal и соавт. [12]: суммарно дозы НМГ составили 2500-17 500 ЕД/сут; при суточной дозе менее 7500 ЕД/сут более чем у 50% беременных развились тромбоэмболические осложнения, при более высокой дозе — у 15% (разница достоверна).
Противопоказания к гепаринотерапии:
1) тромбоцитопения — содержание тромбоцитов менее 100 · 109/л;
2) артериальная гипертензия — АД систолическое выше 160 мм рт. ст.;
3) сосудистое или паренхиматозное кровотечение;
4) ацидоз — снижение ожидаемого антикоагулянтного эффекта;
5) печеночная и почечная недостаточность.
Таким образом, назначение антикоагулянтных препаратов беременным должно проводиться по клиническим показаниям группам пациенток с высоким риском развития ВТЭ либо для улучшения перинатальных исходов при настоящей беременности. Контроль за лечением антикоагулянтами не проводится в случае ингаляционной терапии гепарином, применения мини-доз НФГ при подкожном введении до 15 000 ЕД/сут, внутривенном введении до 20 000 ЕД/сут, профилактическом лечении НМГ одной дозой в сутки. Контроль проводится с помощью определенного лабораторного теста в определенное время при подкожном введении НФГ — контроль за изменением АЧТВ до уровня, превышающего норму в 1,5-2 раза через 4-6 ч от момента инъекции препарата, при подкожном введении НМГ контролируют активность антифактора Ха через 4-6 ч после инъекции до уровня 0,3-0,6 или 0,6-1,2 ЕД/мл в зависимости от режима терапии, лечение варфарином проводится под контролем МНО до уровней 1,5-2,5 в зависимости от групп пациенток. Перспективным, надежным и удобным методом лечения беременных является использование варфарина за исключением сроков от 5 до 15 нед беременности (период органогенеза) и срока перед родами, учитывая длительный период полувыведения препарата. Лечение аспирином или курантилом при угрозе развития ВТЭ патогенетически не обосновано и не должно использоваться. Антикоагулянтная терапия должна применяться по показаниям и в течение продолжительного времени, иногда на протяжении всей беременности. Проблемой будущего является разработка методики гепаринотерапии при эмболии околоплодными водами.
Подготовка к исследованию
Для получения максимально точного результата необходимо придерживаться определенных правил подготовки к исследованию. За день до взятия крови следует соблюдать особую диету, которая подразумевает исключение из рациона ряда продуктов питания:
- жареные блюда;
- продукты с высоким содержанием жиров (масло, сало, сливки, жирные йогурты и сметана);
- блюда, содержащие пряности и уксус (в частности консервация).
Не рекомендуется есть чипсы, сухарики и другие снеки с большим количеством раздражающих приправ, ароматизаторов — эти продукты во время беременности следует исключить полностью. Также нужно постараться избегать помещений с курящими людьми.
Кровь для анализа на Д-димер берется из вены строго натощак. В идеале от последнего приема пищи и до взятия крови должно пройти 12 часов, но при беременности этот промежуток времени выдержать достаточно сложно, поэтому его можно уменьшить до 8 часов. Утром, в день исследования разрешается пить чистую негазированную воду (последний раз — за 30 минут до забора крови).
Также на точность результатов анализов может повлиять психоэмоциональное состояние беременной женщины. Поэтому накануне исследования следует избегать встреч с неприятными и конфликтными людьми и просмотра “тяжелых” драматических фильмов.
В клинику следует прийти немного заранее чтобы немного отдохнуть перед взятием крови.
Важно! Обязательно сообщите лаборанту и своему лечащему врачу, если вы принимаете какие-либо лекарственные препараты. По возможности прием лекарств следует приостановить, но это решать может только врач, который назначил исследование.
При наличии острых инфекционных заболеваний обследование откладывают до полного выздоровления.
Причины повышения Д-димера
Одной из причин повышения уровня Д-димера и активации системы коагуляции является подготовка организма к родам, которые в любом случае сопровождаются кровопотерей различной степени интенсивности. Поэтому максимальный уровень Д-димера будет наблюдаться именно на поздних сроках беременности. А вообще его уровень увеличивается примерно втрое по сравнению с небеременными здоровыми женщинами.
Повышение Д-димера нередко наблюдается наряду с другими признаками позднего токсикоза беременности (гестоза). К ним относятся:
- стойкое повышение артериального давления, которое плохо поддается лечению гипотензивными препаратами;
- появление белка в моче;
- отечность верхних и нижних конечностей, лица и шеи.
Справка! Гестоз — это состояние, которое опасно своими осложнениями — эклампсией и преэклампсией. Эти патологии характеризуются нарушениями мозгового кровообращения и при отсутствии лечения представляют серьезную угрозу для жизни матери и ребенка.
Если Д-димер повышен незначительно
Небольшое превышение уровня Д-димеров может наблюдаться в следующих случаях:
- при многоплодной беременности;
- после операций (даже если они проводились за год-два до исследования);
- при гриппе, ОРЗ и ОРВИ;
- при травмах и ожогах.
В этих случаях Д-димер повышается временно, его уровень возвращается к нормальным значениям после стабилизации состояния.
Патологические причины повышения Д-димера
В ряде случаев повышение уровня Д-димера может наблюдаться при некоторых хронических заболеваниях, нередко протекающих бессимптомно. К ним относятся:
- обычный и гестационный сахарный диабет (последний характерен только при беременности и проходит после родов);
- заболевания печени и желчного пузыря;
- различные заболевания почек, нарушающие их функцию;
- сердечно-сосудистые патологии (в том числе воспалительного происхождения — миокардиты, перикардиты);
- постоянное воздействие аллергенов.
Важно! Повышение D-димера иногда может быть одним из первых признаков начинающейся отслойки плаценты. Симптомы: тянущая боль в области живота различной степени интенсивности, выделения с примесью крови, тошнота и головокружение. Появление этих признаков требует немедленного оказания медицинской помощи!
Что делать, если D-димер повышен
При незначительном превышении нормы и при нормальном самочувствии лечение можно проводить в условиях дневного стационара. Терапия включает в себя инъекции и капельницы кроворазжижающих препаратов.
Снизить Д-димер также помогут следующие рекомендации (но они не заменят основное лечение):
- Пейте больше чистой негазированной воды;
- Занимайтесь физкультурой (особенно полезны специальные занятия для беременных, аквааэробика);
- Больше гуляйте на свежем воздухе ;
- Не переутомляйтесь;
- Уделите внимание правильному питанию.
Важно! Если кто-либо из ваших родственниц страдал нарушениями системы свертывания крови во время беременности, вы попадаете в группу повышенного риска тромботических осложнений. В этом случае рекомендуется консультация генетика, так как в ряде случаев эти патологии передаются по наследству. Желательно это сделать еще на этапе планирования беременности.
Что такое фибриноген?
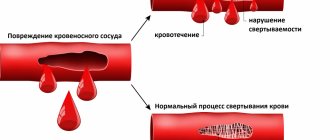
Фибриноген – это белок, один из основных факторов свертывания крови. Он необходим для образования тромбов и остановки кровотечения, помогает в заживлении поврежденных тканей и восстановлении их кровоснабжения. При повреждении стенки сосудов любого калибра в крови запускается каскад биохимических реакций, финалом которых является превращение фибриногена в фибрин. Формируется кровяной сгусток. Практически сразу после этого запускается другой каскад реакций – противосвертывающей системы крови.
Фибриноген синтезируется клетками печени и постоянно присутствует в крови в определенной концентрации. При повреждении стенки сосудов он, с помощью фермента тромбина, превращается в фибрин, который образует полимеры в виде нитей белого цвета – они входят в состав кровяного сгустка. Изменение концентрации фибриногена в крови грозит кровотечениями или тромбозами.
Во время беременности через сосуды плаценты ежеминутно проходит около 600 мл крови. После того как плацента отделяется и выходит во время родов, на слизистой оболочке матки остается кровоточащая поверхность. Во время родов женщина теряет около 500 мл крови (во время кесарева сечения вдвое больше – в среднем 1000 мл). Но затем матка сокращается, сосуды сжимаются, и кровотечение останавливается. Очень важно, чтобы при этом был баланс в работе свертывающей и противосвертывающей систем крови.
Во время беременности под действием гормонов свертывающая система крови активизируется. Организм как бы «готовится» к тому, чтобы в ответственный момент справиться с физиологической кровопотерей.
Уровень фибриногена в крови будущей мамы постепенно повышается и в третьем триместре увеличивается в 2–3 раза по сравнению с обычными значениями. Это происходит под влиянием гормонов.