Гипоксемический криз (одышечно-цианотический приступ)
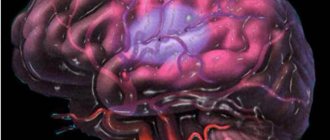
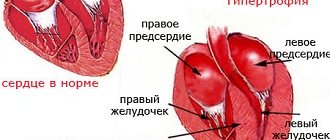
Одышечно-цианотический приступ — приступ гипоксии (пароксизмальной одышки с выраженным цианозом) у ребенка с врожденным пороком сердца синего типа, чаще всего с тетрадой Фалло. Возникает в результате внезапного уменьшения легочного кровотока, связанного со спазмом выходного отдела правого желудочка сердца, увеличения сброса крови справа налево и гипоксемии в большом круге кровообращения.
Приступы гипоксии развиваются преимущественно у детей раннего возраста — от 4–6 месяцев до 3 лет. Провоцирующими факторами одышечно-цианотического приступа могут быть психоэмоциональное напряжение, повышенная физическая активность, интеркуррентные заболевания, сопровождающиеся дегидратацией (лихорадка, диарея), железодефицитная анемия, синдром нервно-рефлекторной возбудимости при перинатальном поражении ЦНС и др.
Одышечно-цианотический приступ характеризуется внезапным началом. Ребенок становится беспокойным, стонет, плачет, при этом усиливаются цианоз и одышка. Принимает вынужденную позу — лежит на боку с приведенными к животу ногами или присаживается на корточки. При аускультации сердца тахикардия, уменьшение интенсивности или исчезновение систолического шума над легочной артерией. Продолжительность гипоксического приступа — от нескольких минут до нескольких часов. В тяжелых случаях возможны гипоксемия, ацидоз, судороги, потеря сознания, вплоть до комы, и летальный исход.
ОСТРАЯ СЕРДЕЧНАЯ НЕДОСТАТОЧНОСТЬ У ДЕТЕЙ, НАХОДЯЩИХСЯ В КРИТИЧЕСКОМ СОСТОЯНИИ (обзор литературы)
Д. Н. Сурков, В.И. Снисарь Кафедра анестезиологии, интенсивной и баротерапии ФПО Днепропетровской государственной медицинской академии.
Острая сердечная недостаточность различной степени выраженности сопровождает течение большинства критических состояний у детей и, поэтому, встречается в практике интенсивной терапии детского возраста довольно часто [2, 4, 11, 13, 15]. При этом, стройной системы взглядов на данную проблему, которая включала бы в себя общепринятую терминологию, классификацию, четкие клинические и инструментальные критерии вариантов развития и степени выраженности, а также исходящие из этого практические рекомендации по лечебной тактике, — не существует. В этой связи целью данного обзора явилось изучение наиболее значимых литературных данных по данному вопросу, а также попытка их систематизации с позиции врача — интенсивиста. Точное определение какого-либо патологического состояния или нозологической формы имеет исключительно важное значение, так как от смысла, который вкладывается в это определение, зависят и диагностика, и разработка наиболее эффективных путей терапии данного заболевания. Так, A. Gyton пишет, что сердечная недостаточность — это недостаточность сердца как насоса. Однако, учитывая то, что она долго может протекать не только с нормальным, но даже повышенным минутным объемом сердца (например, при тиреотоксикозе, бери-бери), это определение нельзя признать универсальным [6]. Можно рассматривать сердечную недостаточность как состояние, при котором сердце не способно перекачивать достаточное количество крови для обеспечения метаболизма периферических тканей [23]. Это определение E. Draunwald с соавт., собственно, является вариантом предыдущего и не может включать формы недостаточности сердца, протекающие с увеличенным минутным объемом. Кроме того, трудно сказать, какой уровень метаболизма тканей требуется в каждом конкретном случае. По мнению Ф.З. Меерсона, сердечная недостаточность — «…это состояние, при котором нагрузка, падающая на сердце, превышает его способность совершать работу». В данном случае подразумевается превышение притока крови к сердцу над оттоком от него, в связи с чем, сам автор замечает: «Это простое определение не является, однако, вполне точным, так как несоответствие между притоком и оттоком должно сравнительно быстро привести к летальной дезинтеграции функции кровообращения и не может лежать в основе хронической недостаточности сердца, которая занимает главное место в патологии человека» [10]. Своеобразную точку зрения представляет Н.М. Мухарлямов: «Под сердечной недостаточностью следует понимать в настоящее время такое патологическое состояние, когда вначале выявляется мобилизация компенсаторных механизмов, а затем — истощение последних с недостаточным обеспечением организма кровью» [12]. Критически рассматривая это определение, следует сказать, что мобилизация компенсаторных механизмов происходит в начале любого патологического процесса, повреждающего миокард, а недостаточное обеспечение организма кровью может определяться не только патологией сердечной мышцы, но, например, кровотечением или сосудистым спазмом, сочетающимися или не сочетающимися с повреждением сердца. В.А. Фролов и соавт. (1994) считают, что «сердечная недостаточность — это состояние, характеризующееся снижением резервных возможностей сердца». Под это определение подходят как острая, так и хроническая и даже скрытая формы недостаточности сердца. По мнению авторов, «патология тем и отличается от нормы, что при развитии патологического процесса биологическая система, израсходовав все возможности жестко не запрограммированных колебаний, начинает функционировать узконаправленно, максимально мобилизуясь для достижения необходимого эффекта, но это приводит к исчерпанию резервных возможностей организма, последующей патогенной рассинхронизации его функций, перенапряжению и возможному полому механизмов саногенеза» [19]. Существует несколько классификаций недостаточности кровообращения вообще и сердечной недостаточности, в частности. Общепризнанной считается классификация по Н.Д. Стражеско и В.Х. Василенко (1935), в которой острая сердечная недостаточность подразделяется на левожелудочковую (сердечная астма и отек легких), правожелудочковую и бивентрикулярную. Определенный интерес представляет клиническая классификация острой левожелудочковой недостаточности T. Killip и J. Kimball (1967), применяющаяся, в частности, при остром инфаркте миокарда [3]:
I класс — клинические признаки сердечной недостаточности отсутствуют.
II класс — отмечается умеренная одышка, ритм галопа и/или застойные хрипы менее чем над 50% площади легочных полей.
III класс — застойные хрипы определяются более чем над 50% легких или развивается отек легких.
IV класс — кардиогенный шок.
Однако столь выраженные формы острой сердечной недостаточности у детей встречаются достаточно редко, представляют собой варианты декомпенсации и предполагают проведение, фактически, реанимационных мероприятий. Хроническая сердечная недостаточность достаточно широко изучена и является, преимущественно, прерогативой кардиологов. В практике педиатрической интенсивной терапии достаточно частой и сложной является проблема острой сердечной недостаточности (ОСН). По мнению А.В. Папаян, Э.К. Цыбулькина (1984) в настоящее время нет общепринятой классификации острой сердечной недостаточности у детей. Использование для этой цели классификации хронической сердечной недостаточности не может быть безоговорочным, поскольку при острых состояниях само заболевание уже в покое способствует развитию сердечной недостаточности I степени [13]. По Э.К. Цыбулькину (1994) ОСН клинически проявляется:
- синдромом малого сердечного выброса (СМСВ) в виде артериальной гипотонии и признаков централизации кровообращения;
- застойной сердечной недостаточностью (ЗСН) с перегрузкой малого или большого кругов кровообращения. Признаки застоя в большом круге: периферические отеки, увеличение печени, контурирование шейных вен, асцит, гидроторакс. Признаки застоя в малом круге: одышка, влажные хрипы в нижних отделах легких, клиника отека легких, неэффективность ингаляции больших концентраций кислорода.
Наиболее частые причины СМСВ:
- аритмический шок — брадиаритмии (синусовые или вследствие AV-блокады, фибрилляция желудочков, групповые желудочковые экстрасистолы) или тахиаритмии (чрезмерные тахикардии — гипермотильный токсикоз Кишша или острая коронарная недостаточность у детей раннего возраста, наджелудочковая пароксизмальная тахикардия, мерцание и трепетание предсердий и др.);
- кардиогенный шок — острая очаговая (инфаркт) или тотальная гипоксия миокарда (состояние с гипоксией и ацидозом);
- острая тампонада перикарда (ранение или разрыв миокарда, перикардит, пневмомедиастинум и пневмоперикард) или экстракардиальная тампонада сердца при астматическом статусе III-IV степени, интерстициальной эмфиземе;
- терминальная стадия ЗСН на фоне декомпенсированных пороков сердца, миокардитов или миокардий различного генеза [20].
У детей причинами развития синдрома острой сердечной недостаточности могут являться:
- острые бронхо-легочные изменения (пневмонии, синдром острого повреждения легких [11], ателектазы, гидро- и пневмоторакс, пр.), при которых главными механизмами формирования сердечной недостаточности являются собственно гипоксия и легочная гипертензия вследствие внутрилегочного шунтирования крови [24, 41];
- любые состояния, связанные (несмотря на нормоволемию) с тканевой гипоксией: экзо- и эндогенные токсикозы [15], синдром системного воспаления [17, 35], ожоговая болезнь [2], тяжелые гнойно-септические процессы, т.е. состояния, при которых вследствие гиперкатаболизма системный транспорт кислорода и глюкозы не покрывает возросших потребностей тканей и органов [36]. В подобной ситуации существенно возрастает минутный объем кровотока, что достигается у детей вследствие не увеличения ударного объема, а более за счет повышения частоты сердечных сокращений. При этом происходит повышение потребления миокардом кислорода, а также сокращение времени диастолы, что приводит, с одной стороны, к уменьшению наполнения желудочков в фазу изоволюмического расслабления и редуцированию сердечного выброса, с другой стороны — к снижению коронарного кровотока, ишемии миокарда и снижению его контрактильности.
По степени выраженности А.В. Папаян и Э.К. Цыбулькин (1984) выделяют 3 степени острой сердечной недостаточности:
Острая сердечная недостаточность I степени характеризуется тахикардией и одышкой, отчетливо проявляющейся у ребенка в покое. Самым важным симптомом является изменение соотношения между частотой сердечных сокращений и дыхания. В этих случаях у детей до 1 года отношение частоты пульса к частоте дыхания будет свыше 3,5; у детей старше 1 года — 4,5. Имеются признаки поражения сердце: глухость тонов, расширение границ относительной сердечной тупости.
Острую сердечную недостаточность II степени, самой важной особенностью которой следует считать компенсаторную гиперволемию, в зависимости от тяжести можно подразделить на 2 состояния: с преобладанием декомпенсации только в одном круге кровообращения или с тотальной недостаточностью кровообращения. При недостаточности II А степени, если преобладают явления застоя в большом круге, у больного увеличиваются размеры печени, могут быть периорбитальные отеки. ЦВД повышается только в том случае, если декомпенсация развивается быстро, в течение минут или нескольких часов. Если недостаточность нарастает постепенно в течение 1-2 сут., то ЦВД может оставаться нормальным на фоне прогрессивного набухания печени. Печень в этих случаях играет роль буфера. Обязательна приглушенность тонов сердца, возможно расширение границ относительной сердечной тупости. Если преобладают явления застоя в малом круге кровообращения, помимо относительной тахикардии, усиливается цианоз, степень которого не уменьшается под влиянием оксигенотерапии. В легких появляются рассеянные мелкопузырчатые хрипы, определяется акцент II тона на легочной артерии. При недостаточности II Б степени к перечисленным признакам присоединяются олигурия, периферические отеки, возможен отек легких.
Острая сердечная недостаточность III степени — гипосистолическая форма сердечной недостаточности с развитием артериальной гипотензии на фоне клиники перегрузки малого круга кровообращения [13].
Синдром гемодинамического шока представлен острой циркуляторной недостаточностью, связанной с падением артериовенозного градиента давления. Три несвязанных группы процессов, кардиогенный, вазогипотонический и гиповолемический механизмы, являются отправной точкой патогенеза синдрома шока. Кроме того, клиническая практика зачастую сталкивается со сложными процессами, включающими два или три патогенетических механизма одновременно [30]. Существует 4 наиболее важных контролирующих механизма циркуляторной системы человека для поддержания гемодинамики — ренин-ангиотензиновая система, автономная нервная система, локальная артериальная ауторегуляция и стрессовое расслабление сосудов. [36] При этом, застойная сердечная недостаточность характеризуется: 1) нейрогуморальной вазоконстрикцией, тахикардией; 2) задержкой натрия и воды; 3) увеличением плазменной концентрации норадреналина [40]. В практике интенсивной терапии детского возраста следует выделять синдром острой сердечной недостаточности [40], который может быть связан с непосредственным поражением сердечной мышцы (врожденные и приобретенные пороки сердца, миокардиты [16], отравления кардиотоксическими ядами [15], др.), а также может сопровождать любое критическое состояние в связи с развивающейся гипоксией и энергодефицитом [41]. В последнем случае изменения в деятельности сердца носят обратимый характер и связаны, как правило, с нарушением систоло-диастолических соотношений сердечного цикла и, как следствие, с развивающимися преходящими ишемическими и дистрофическими изменениями в сердечной мышце. Для понимания особенностей развития острой сердечной недостаточности у детей необходимо рассмотреть такое понятие, как потребление кислорода миокардом (MVO2). Гемодинамика представляет собой функцию сердечного оттока и сосудистого сопротивления. В свою очередь, сердечный отток зависит от частоты сердечных сокращений и ударного объема. На величину последнего влияют преднагрузка, постнагрузка и сократимость миокарда. Большую часть MVO2 организм использует для поддержания сокращений миокарда. При этом увеличение сократимости приводит к повышению потребления миокардом кислорода. Имеется также прямая корреляция между частотой сердечных сокращений (ЧСС) и MVO2. Учащение сердечных сокращений на 50 % обычно сопровождается 50 % увеличением MVO2. Потребление кислорода также зависит от количества наружной работы, совершаемой сердцем. Последняя может быть разделена на генерацию аортального давления (работа давления) и на изгнание ударного объема (работа объема). Работа давления (изометрическое сокращение) имеет намного более высокую энергетическую цену, чем работа объема (изотоническое сокращение). Ясно, что поддержание кровяного давления за счет повышения ударного объема сердца более экономично. В детском возрасте увеличение сердечного индекса происходит за счет повышения ЧСС при малоизменющемся ударном объеме. Так как при этом напряжение стенки миокарда может не изменяться, то рост MVO2 для данного прироста ЧСС у детей больше, чем у взрослых [14]. К настоящему времени выполнено огромное количество исследований, преимущественно экспериментальных, посвященных сущности биохимических изменений миокарда, приводящих к нарушению его сократительной активности. Результаты этих исследований свидетельствуют, что решающее значение в ухудшении насосной функции сердца принадлежат нарушениям утилизации энергии, обусловленных изменениями основных сократительных белков, проявляющихся уменьшением количества миофибриллярных белков, в том числе белков актиномиозинового комплекса [40], так и изменениями физико-химической структуры миозина, приводящими к снижению его АТФ-азной активности. Одновременно нарушается и процесс накопления энергии (ресинтеза макроэргов) из-за дистрофических изменений в митохондриях. При этом существенно снижается синтез АТФ, обеспечивающий функционирование ионных каналов клеточных мембран и эндоплазматического ретикулума [31]. В этих условиях изменяется четко синхронизированное в интактном миокарде движение ионов через клеточные мембраны. Механистически развитие сердечной недостаточности можно рассматривать на основании данных микроволновой резонансной томографии. «Скручивающее» движение левого желудочка описано на протяжении систолы, которое включает вращение по часовой стрелке основания и против часовой стрелки — верхушки. На протяжении диастолы происходит «раскручивающее» движение. В нормальном сердце, диастолическое «раскручивание» продолжается преимущественно на протяжении изоволюмического расслабления, аналогично систолическому «скручиванию», которое занимает место преимущественно на протяжении изоволюмического сокращения. Продление «раскручивающего» движения было обнаружено в гипертрофированном и гибернированном сердце. Таким образом, сердечная недостаточность связана с глубокими нарушениями в механической функции сердца, что проявляется изменениями в систолическом «скручивающем» и диастолическом «раскручивающем» движении [32]. В развитии острой сердечной недостаточности существует стадийность. При этом на ранних этапах страдает дистолическое расслабление, после чего и, зачастую, вследствие чего наступает нарушение систолического сокращения [25, 26, 29, 32]. Соответственно, в течении острой застойной сердечной недостаточности (ЗСН) [28] выделяют существенно отличающиеся формы, соответственно этиологии, клинической картине и патофизиологии левожелудочковой (ЛЖ) дисфункции [27]. Систолическая и диастолическая дисфункции характеризуются сниженным сердечным выбросом при нормальной (нарушение диастолической функции) или сниженной (систолическая дисфункция) ЛЖ насосной функцией. Систолическая дисфункция включает комбинацию легочного застоя со сниженной систолической фракцией выброса. Нарушение диастолической функции сопровождается легочным застоем в присутствии нормального или только незначительно увеличенного желудочка с нормальной фракцией выброса [25, 26]. Взаимосвязь между нарушениями систолической и диастолической функции левого желудочка хорошо известна, но пока не зарегистрирована достаточно полно. Более того, количественная классификация нарушений диастолической функции все еще отсутствует [29]. Диастола является энергопотребляющим процессом. Ионы кальция должны нагнетаться в саркоплазматический ретикулум против градиента. Кроме того, разъединение тропомиозиновых мостиков требует гидролиза молекулы аденозинтрифосфата. Уменьшение способности эндоплазматического ретикулума утилизировать кальций из цитоплазмы кардиомиоцитов приводит к повышению его концентрации во время диастолы и тем самым препятствует расслаблению миокарда [33]. При нарушении диастолической функции желудочки сердца не могут адекватно наполняться при нормальном давлении и требуют компенсаторного повышения его в предсердиях. В основе патогенеза нарушения диастолической функции миокарда лежит нарушение его релаксации (расслабления) и растяжимости (комплайнса) [8]. Нарушение диастолического расслабления является одним из самых ранних изменений, регистрируемых еще до наступления клиники сердечной недостаточности. Систолическая дисфункция миокарда (снижение сократимости) развивается в более поздние сроки [1]. Поэтому оценка диастолической функции может быть более чувствительной мерой миокардиальной дисфункции, чем систолические размеры [22]. Изучение острого транзиторного нарушения диастолической функции миокарда является перспективными в плане выявления предикторов развивающейся острой сердечной недостаточности и выбора различных вариантов медикаментозной терапии, направленных на предотвращение декомпенсации сердечной деятельности, развитие синдрома малого сердечного выброса и кардиогенного шока [22, 27]. Примером острой нарушения диастолической функции у детей может служить особый вариант токсикоза при вирусной инфекции, названный острая коронарная недостаточность или токсикоз Кишша. Суть этого варианта состоит в том, что доминантой в его течении и исходе является сердечная недостаточность, развивающаяся как результат чрезмерной синусовой тахикардии у предварительно здорового ребенка. Тахикардию считают чрезмерной в связи с тем, что за счет значительного сокращения времени диастолы резко затрудняется венозный приток и критически уменьшается ударный объем. Эти изменения в первую очередь отражаются на коронарном кровотоке, приводя к недостаточному кровоснабжению миокарда. Сердечная недостаточность развивается двухэтапно. На I этапе сокращение времени диастолы не сопровождается декомпенсированным падением сердечного оттока, хотя признаки застойной недостаточности по большому кругу уже присутствуют. На II этапе (декомпенсации) уменьшение диастолы приводит к гипосистолии, сопровождающейся артериальной гипотензией, отеком легкого и комой [20]. Ватолиным К.В. и соавт. было установлено, что нарушение диастолической функции ЛЖ наиболее выражено при транзиторной дисфункции миокарда левого желудочка (ТДМЛЖ) [4]. С целью контроля гемодинамики у детей в отделении реанимации и интенсивной терапии традиционно используют инвазивные методы (прямой метод Фика, метод разведения красителей, термодилюции). Тяжесть состояния больных и необходимость точного и достоверного контроля центральной гемодинамики и ее коррекции оправдывают риск инвазивного вмешательства. Однако, учитывая огромные преимущества неинвазивных методов исследования, все более часто они применяются в условиях реанимации и интенсивной терапии. В практике педиатрической интенсивной терапии широко применяется метод тетраполярной грудной реографии по Кубичеку
(1966 г.) в модификации. Метод обеспечивает расположение измерительных электродов в области равномерного электрического поля, поэтому является методически более корректным. Метод предполагает синхронную запись ЭКГ, ФКГ, РГ (или каротидной СФГ) и дифференциальной РГ, что требует применения многоканальных регистраторов. При измерении СВ методом тетраполярной грудной реографии и прямыми методами (термодилюция, разведения красителей) r, по данным литературы, колеблется от 0,31 до 0,99. Ряд авторов, используя метод в отделении реанимации, получили r = 0,94 [7]. Вместе с тем у больных с пороками сердца было найдено низкое соответствие с прямыми методами. Более того, некоторыми авторами при одновременном измерении СВ методом тетраполярной грудной реографии и электромагнитной флоуметрии в процессе гемодилюции не получено не только достоверных данных о СВ по абсолютной величине, но и отражения объективной динамики показателя [9].
Эхокардиография
широко используется для оценки состояния детей с застойной сердечной недостаточностью. Из-за её уникальной способности оценивать размер и геометрию левого желудочка (ЛЖ), ЛЖ систолическую и диастолическую функцию, размер и функцию правого желудочка, сердечные клапаны, перикард, и врожденные аномалии развития, эхокардиография ценна в установлении специфических кардиологических диагнозов, руководства терапией, и оценки прогноза в ЗСН [5, 21]. Эхокардиографические показатели функции желудочков зависят от преднагрузки, постнагрузки и сократимости. Следовательно, все показатели функции желудочков должны быть осмыслены, поскольку эхокардиографические размеры не обязательно отражают сократимость желудочка. Не существует неинвазивных методов определения сократимости, но эхокардиография позволяет определить их опосредованно. Эталон — допплеркардиография, которая по точности не уступает инвазивным методам исследования (Зарецкий В.В. с соавт., 1979; Cross G., Light L.H., 1974; Forrester J.S. et al., 1977; Merrill P., Spenser M.D., 1984) [9]. Двумерная эхокардиография не отражает сократимости миокарда, но достаточно надежно выявляет региональные нарушения движения стенок. Анализ характера региональных нарушений движения стенок из парастернальной позиции короткой оси или апикальной четырех камерной позиции может обеспечить некоторую информацию относительно повреждения миокарда. Методы исследования систолической функции включают измерение:
- фракции укорочения и септации клапанов в точке Е;
- фракции выброса в М- и В-режиме;
- допплеркардиография для измерения скорости укорочения циркулярных волокон миокарда [21].
Сообщают об использовании допплеркардиографии
входящего потока митрального клапана как средства оценки диастолической функции. Было замечено, что три допплеровских паттерна входящего потока митрального клапана не зависят от стадии заболевания. Это связано с тем, что допплерография входящего потока митрального клапана фактически измеряет перепад давлений между предсердием и желудочком. Переход между различными паттернами динамичен и может происходить в течение нескольких часов в зависимости от состояния гемодинамики пациента и любых терапевтических вмешательств, которые, возможно, были предприняты. При этом, первый допплеровский паттерн, паттерн I, формируется рано в ходе диастолических отклонений, когда давление в предсердиях нормально. Он проявляется уменьшением Е-волны (пассивное наполнение желудочка) с длительным временем замедления и повышением волны А (активное наполнение в течение предсердного сокращения). При повышении давления в левом предсердии допплеровский паттерн входящего потока приобретает вид «нормального». Наиболее неблагоприятный показатель диастолических отклонений — паттерн II, при котором волна Е увеличена с коротким временем замедления и очень маленькой А-волной. Указанные параметры допплеровских паттернов входящего потока могут дать ключ к определению диастолических отклонений, принимая во внимание, что величина IVRT, Vmax E, Е/А отражает степень релаксации, а КДО и Vmax A — состояние податливости (комплайнса) [5, 18, 21]. Вычисление сердечного выброса может быть произведено неинвазивно с помощью непрерывного двумерного и допплерэхокардиографического исследования и использования уравнения. Поток для одного сердечного цикла, или SV, рассчитывается как
SV = CSA x V x RR/1000 мл/л,
где CSA (см2) — площадь поперечного сечения клапана, через который измеряется поток; V (см/с) — средняя скорость поперек клапана, и RR — число ударов в секунду. Чтобы вычислить сердечный выброс, нужно умножить SV на частоту сердечных сокращений [22]. Таким образом, исследование сердечного цикла в режиме реального времени является обязательным у детей, находящихся в отделениях интенсивной терапии [34, 42]. Данные допплеровского определения сердечного выброса и трансмитральных паттернов позволят дифференцировать зависимость тех или иных клинических проявлений от степени функциональных нарушений сердечной деятельности [5, 21, 38, 39].
СПИСОК ЛИТЕРАТУРЫ
Алмазов В.А., Шляхто Е.В. (1995) Сердечная недостаточность: современные тенденции терапии // Харьковский медицинский журнал. — 2: 19-22.
Альес В.Ф., Андреев А.Г., Ульянова Г.И., Гранова Л.В., Астамиров М.К. (1998) Доставка, потребление и экстракция О2 в острый период ожоговой болезни у детей // Анест. и реанимат. — 1: 4-7.
Амосова Е.Н. (1996) Острая сердечная недостаточность при инфаркте миокарда // Журнал практического врача. — 1: 13-16.
Ватолин К.В., Ефимов М.С., Пыков М.И. с соавт. (2000) Оценка диастолической функции сердца у новорожденных реанимационного профиля с внутричерепными кровоизлияниями // Неотложные состояния у детей. 6-й конгресс педиатров России (г. Москва). Материалы съезда. — с.74.
Воробьев А.С., Бутаев Т.Д. (1999) Клиническая эхокардиография у детей и подростков: Руководство для врачей. Специальная литература, СПб., 423 с.
Гайтон А. (1970) Минутный объем сердца. Медицина, М., 64 с.
Земцовский Э.В., Гусейнов Б.А., Извекова А.В., Полухина Е.Л., Чистова И.Я. (1989) О точности реографического метода определения ударного объема крови // Кардиология. — 6: 75-79
Коркушко О.В., Мороз Г.З., Гидзинская И.Н. (1992) Изучение диастолической функции сердца в клинике // Кардиология. — 5: 92-95.
Лебедева Р.Н., Аббакумов В.В., Борисова И.В., Свирщевский Е.Б., Бондаренко А.В., Чаус Н.И., Караваев Б.И. (1989) Современные методы оценки гемодинамики в условиях отделения интенсивной терапии (сравнительный аспект) // Анест. и реаниматол. — 4: 3-8.
Меерсон Ф.З. (1968) Гиперфункция, гипертрофия, недостаточность сердца. Медицина, М., 112 с.
Миленин О.Б., Ефимов М.С. (1990) Нарушение гемодинамики в остром периоде синдрома дыхательных расстройств (по данным допплерэхокардиографии) // Педиатрия. — 4: 3-9.
Мухарлямов Н.М. (1978) Ранние стадии недостаточности кровообращения и механизмы ее компенсации. Медицина, М., 96 с.
Папаян А.В., Цыбулькин Э.К. (1984) Острые токсикозы в раннем детском возрасте. 2-е изд., перераб. и доп. Медицина, Л., 73 с.
Руководство по педиатрии (Неотложная помощь и интенсивная терапия) (1999) / Под редакцией М. Роджерса, М. Хелфаера. Питер, СПБ., 1120 с.
Савина А.С. (1992) Острая сердечная недостаточность и ее лечение при отравлениях кардиотоксическими препаратами // Кардиология. — 4: 67-70.
Сидельников В.М., Волосовець О.П., Кузьменко А.Я., Кривопустов С.П. (1992) Функціональний стан міокарда в періоді діастоли у дітей з набутими захворюваннями серця // Педіатрія, акушерство і гінекологія. — 3: 17-19.
Сиприя А.Г., Тальвик Р.М. (1993) Прогностическое значение некоторых показателей центральной гемодинамики, кислородного баланса и внутрилегочного шунта у больных с сепсисом в критическом состоянии // Анест. и реанимат. — 5: 43-45.
Трекова Н.А., Яворовский А.Г., Флеров Е.В., Юматов А.Е., Ковалевская О.А., Асмангулян Е.Т., Гришин В.В. (1999) Влияние современных методов вводной анестезии на систолическую и диастолическую функцию левого и правого сердца у больных ишемической болезнью сердца // Анест. и реанимат. — 5: 4-5.
Фролов В.А., Казанская Т.А., Дроздова Г.А. (1994) Об определении понятия «сердечная недостаточность» // Патологическая физиология и экспериментальная терапия. — 4: 3-7.
Цыбулькин Э.К. (1999) Угрожающие состояния у детей. Экстренная врачебная помощь: Справочник. Специальная Литература, СПб., 119 с.
Шиллер Н., Осипов М.А. (1993) Клиническая эхокардиография. Мир, М., 347 с.
Bengur A.R., Meliones J.N. (1998) Cardiogenic shock // New Horiz. Sci. and Pract. of Acute Med. — 6(2): 139-149.
Draunwald E., Ross S., Sonnenblick E. (1976) Mechanisms of contraction of the normal and failing heart. 2-d Ed. Boston.
Ducas J., Stitz M., Gu S., Schick U., Prewitt R.M. (1992) Pulmonary vascular pressure-flow characteristics. Effects of dopamine before and after pulmonary embolism // Am. Rev. Respir. Dis. — 146(2): 307-312.
Federmann M., Hess O.M. (1994) Differentiation between systolic and diastolic dysfunction // Eur. Heart J. — 12(15): 2-6.
Federmann M., Risti B., Hess O.M. (1994) Left ventricular insufficiency: systolic versus diastolic dysfunction // Schweiz. Med. Wochenschr. — 124(26): 1196-1202.
Gaasch W.H. (1994) Diagnosis and treatment of heart failure based on left ventricular systolic or diastolic dysfunction // JAMA. — 271(16): 1276-1280.
Hsueh C.W., Lee W.L., Chen C.K. et al. (1998) Dopamine and dobutamine have different effects on heart rate variability in patients with congestive heart failure // Chung Hua I Hsueh Chin, Taipei. — 61(4): 199-209.
Kosmala W., Spring A., Witkowska M. (1997) Relationship between systolic and diastolic function of the left ventricle in patients with impaired relaxation of the left ventricle without symptoms of heart failure. Attempt at quantitative estimation of diastolic function in the impaired relaxation stage // Pol. Arch. Med. Wewn. — 98(11): 414-423.
Kovac Z. (1995) Pathogenic role of intracellular energy insufficiency (hypoenergy) in the development of circulatory collapse (hemodynamic shock) // Lijec. Vjesn. — 117(2): 11-15.
Kozlik-Feldmann R., Kramer H.H., Wicht H., Feldmann R., Netz H., Reinhardt D. (1993) Distribution of myocardial beta-adrenoceptor subtypes and coupling to the adenylate cyclase in children with congenital heart disease and implications for treatment // J. Clin. Pharmacol. — 33(7): 588-595.
Matter C., Nagel E., Stuber M., Boesiger P., Hess O.M. (1996) Assessment of systolic and diastolic LV function by MR myocardial tagging // Basic Res. Cardiol. — 91(2): 23-28
McDonagh T., Robb S., Murdoch D. et al. (1998) Biochemical detection of left — ventricular systolic dysfunction // Lancet. — 351(9095): 9-13.
Murdoch I.A., Marsh M.J., Tibby S.M., McLuckie A. (1995) Continuous haemodynamic monitoring in children: use of transoesophageal Doppler // Acta Paediatr. — 84(7): 761-764.
Myocardial function in the critically ill: factors influencing left and right ventricular performance in patients with sepsis and trauma (1985) // Surg. Clin. North. Am. — 65(4): 867-893.
Schamberger M.S. (1996) Cardiac emergencies in children // Pediatr. Ann. — 25(6): 339-344.
Schwarzhaupt A., Grossmann C., Kiencke U. (1998) Simulation of metabolic process in human circulation: evaluation of pH value and CO2 balance // Biomed. Tech., Berl. — 43(10): 275-280.
Shoemaker W.C. (1996) Oxygen transport and oxygen metabolism in shock and critical illness. Invasive and noninvasive monitoring circulatory dysfunction and shock // Crit. Care Clin. — 12(4): 939-969.
Shoemaker W.C. (1996) Temporal physiologic patterns of shock and circulatory dysfunction based on early descriptions by invasive and noninvasive monitoring // New Horiz. — 4(2): 300-318.
Steifa M., Toman J., Spiranova L. (1997) Acute and chronic heart failure // Vnitr. Lek. — 43(2): 105-110.
Stocker F., Wyler F. (1994) Pediatric cardiological emergencies // Ther. Umsch. — 51(9): 601-606.
Velmahos G.C., Shoemaker W.C., Wo C.C., Demetriades D. (1999) Physiologic monitoring of circulatory dysfunction in patients with severe head injuries // World J. Surg. — 23(1): 54-58.