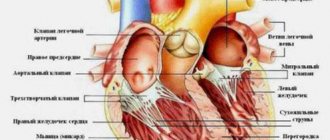
Жизнь после операции
Рекомендации пациентам после радиочастотной катетерной аблации фибрилляции предсердий (ФП):
- Наблюдение кардиолога (терапевта) по месту жительства;
- Ограничение физических нагрузок в течение 2 недель;
- Контроль суточного мониторирования ЭКГ (ХМЭКГ), ЭХОКГ через 3 месяца по месту жительства;
- Приём Варфарина или новых оральных антикоагулянтов (Прадакса, Ксарелто, Эликвис) не менее 3 месяцев, возможно до 6-12 месяцев, при постоянной форме ФП пожизненный приём;
- Приём антиаритмических препаратов (ААП) не менее трех месяцев;
- При возникновении пароксизма ФП – вызвать скорую медицинскую помощь 03, снять ЭКГ;
- После оперативного лечения ФП в течение трех месяцев эффективность операции не оценивается. В это время могут сохраняться ощущения перебоев в работе сердца, дискомфорт, возможны срывы ритма. У 10-15 % пациентов по истечению трех месяцев сохраняются пароксизмы ФП, может потребоваться повторная консультация аритмолога для решения вопроса о необходимости повторной процедуры.
Об операции криоабляции
Криоабляция – один из самых эффективных, безопасных и простых способов лечения нарушений сердечного ритма. Применяется с целью изолирования устья легочных вен (источник паталогической пульсации, который приводит к фибрилляции предсердий) и прекращения передачи, распространения нежелательных электрических импульсов по предсердиям. Осуществляется без разрезов с применением местной анестезии, путем контролированного разрушения аритмогенных участков с помощью заморозки. В кардиологическом центре ФНКЦ ФМБА достаточно молодой, но успешный вид операции проводится с 2021 года.
Холтеровское мониторирование проводится двумя способами:
- Точечная– заменяет радиочастотную, вместо высокочастотного тока подается жидкий азот и точечно замораживает поврежденные участки;
- Баллонная – в бедренную артерию вводится катетер с баллоном на конце, достигая легочных вен баллон раздувается, полностью заполняя место впадения вены в предсердие, и прижигает холодом паталогический участок.
Основные преимущества криотерапии
эффективность — во время проведения операции паталогический очаг, провоцирующий учащённое сердцебиение, полностью блокируется, сердечный ритм восстанавливается
длительность – проведение операции занимает 1-1,5 часа
безопасность – за счет быстроты проведения снижается время лучевой нагрузки на пациента, уменьшается вероятность тромбообразований. Риск возникновения послеоперационных осложнений минимален
простота исполнения – операция не требует рассечения грудной клетки, проводится с помощью одного прокола бедренной артерии
Коротко о главном
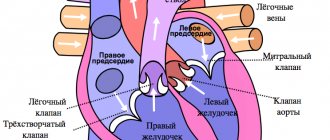
Аритмия сердца – нарушение ритма камер сердца или проводимости. Основной механизм развития – патология деятельности проводящей системы сердца, которая вызвана либо органическим или функциональными нарушениями сокращений миокарда, либо внесердечными причинами (тиреотоксикоз, заболевания нервной системы и др.). Патология частоты сердечных сокращений (ЧСС) увеличивает нагрузку на миокард и уменьшает снабжение органов кислородом. Некоторые аритмии угрожают развитием остановки сердца, возникновением инфарктов и инсультов, тромбоэмболическими осложнениями.
Показания к проведению баллонной криоабляции
Показанием для проведения операции является – фибрилляция предсердий.
Как и любая, хоть и малоинвазивная операция, криоабляция имеет противопоказания:
- жизнеугрожающее состояние пациента;
- наличие тромбов в предсердии;
- тромбоз ушка левого предсердия;
- острый инфаркт миокарда;
- острый инсульт;
- инфекционные заболевания;
- воспалительные процессы в организме;
- заболевания почек, печени, органов дыхания;
- аллергическая реакция на контраст, используемый во время операции.
Зачем делают операцию по прижиганию сердца при аритмии и тахикардии?
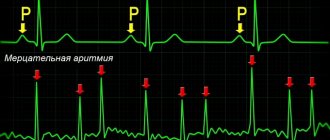
Прижигание сердца при мерцательной аритмии
У здорового человека мышцы всегда сокращаются одновременно, а у больного мерцательной аритмией такого не происходит. Создается циркуляция импульсов и формируется очаг возбуждения. Зачем делают операцию по прижиганию сердца при аритмии и тахикардии?
- Операция в большинстве случаев считается необходимой при мерцательной аритмии.
- Сначала во время диагностики пациенту в больнице ставят диагноз и назначают лечение лекарственными средствами.
- Если после медикаментозного лечения динамика не станет положительной, то человеку нужна абляция.
- Такое прижигание необходимо людям больным тахикардией желудочного типа. Это самое опасное заболевание, потому что у человека ускоряются сердечные сокращения, и со временем может развиваться фибрилляция. Это приводит к тому, что миокарда совсем перестает функционировать.
Показания для проведения прижигания сердца могут быть разными, но все обследования и назначения, должен проводить только квалифицированный кардиолог.
Подготовка к операции
Чтобы определить, есть ли противопоказания к проведению операции и гарантировать успешный исход абляции, пациенту необходимо пройти ряд исследований. Их можно разделить на две части:
- клинико-лабораторные анализы:
- клинический анализ крови;
биохимический анализ крови: общий белок, креатинин, мочевина, общий билирубин, прямой билирубин, глюкоза, панкреатическая амилаза;
- общий анализ мочи;
- коагулограмма развёрнутая;
- АДФ агрегация тромбоцитов;
- определение группы крови и резус фактора;
- маркеры инфекций: ВИЧ, гепатит В, гепатит С, сифилис;
- Pro-BNP, СРБ, тропонин.
- Инструментальные исследования:
- рентген органов грудной клетки;
ЭКГ;
- ЭхоКГ;
- ЭГДС;
- УЗДС брахиоцефальных артерий;
- УЗДС артерий нижних конечностей;
- УЗДС вен нижних конечностей;
- ФВД;
- УЗИ внутренних органов;
- ЧПЭхоКГ;
- коронарография;
В зависимости от наличия сопутствующих заболеваний могут быть назначены дополнительные исследования, анализы и консультация узких специалистов (невролог, эндокринолог, офтальмолог и т.д.).
После проведенных исследований пациенту необходимо подготовиться к операции:
- за несколько дней до проведения криобляции врач отменяет прием лекарственных препаратов;
- в день перед операцией разрешается завтрак, обед и легкий ужин;
- за 12 часов до исследования нельзя ничего есть, необходимо отказаться от приема жидкости за 8 часов;
- на ночь пациенту ставят очистительную клизму;
- с утра в день операции пациент принимает душ и проводит гигиенические процедуры (необходимо сбрить волосы в месте введения катетера – чаще в паховой области);
- перед операцией пациента осматривает хирург и анестезиолог. Вводится мягкое седативное средство, которое поможет расслабить и успокоить волнение.
Кардиологический центр ФНКЦ ФМБА предлагает пациентам плановую госпитализацию для проведения всех необходимых исследований и подготовки к абляции. Наш многопрофильный центр оснащен собственной лабораторией и современным оборудованием. Поэтому сдать анализы и пройти все исследования вы можете в нашей клинике. Мы гарантируем точность результатов и скорость их предоставления.
Диагностика
Чтобы сократить диагностический поиск, сообщите врачу о заболеваниях, способствующих развитию патологии: • порок сердца; • миокардиопатия; • атеросклероз; • артериальная гипертензия; • сахарный диабет; • болезни щитовидной железы; • заболевания почек. Если вы принимаете лекарственные препараты, расскажите об этом доктору. На приём необходимо взять с собой все имеющиеся медицинские документы, последние данные ЭКГ, УЗИ сердца, лабораторных анализов. Основной метод установления диагноза при нарушении ритма сокращений миокарда – электрокардиография и ее модификации: провокационные пробы, холтеровское мониторирование (регистрация ЭКГ в течение часов, суток или даже нескольких дней).
Проведение криоабляции
Криоабляция с целью изоляции легочных вен проводится в отделении рентгенохирургии.
Во время операции осуществляются следующие манипуляции:
- хирург-аритмолог делает прокол в паховой области, через бедренную артерию вводит диагностический катетер и ведет его к сердцу;
- достигая правого предсердия, врач делает пункцию (прокол) межпредсердной перегородки. Это позволяет обеспечить доступ к левому предсердию;
- вводится контрастное вещество, с помощью диагностического катетера врач определит паталогический очаг и увидит необходимое место для абляции на экране рентгеновского аппарата;
- вслед за диагностическим катетером вводят криобаллонный, достигая левого предсердия баллон раздувают;
- врач подводит баллон к устью легочной вены и закрывает проход, тем самым останавливая кровоток между предсердием и веной;
- как только закрытие подтверждено, врач вводит холодовой агент в криабаллон;
- криабаллон, испаряясь, забирает тепло из поврежденной ткани сердца. На этом месте ткань рубцуется и не может больше генерировать и распространять электрические импульсы, которые были причиной нарушений ритма сердца;
- баллон сдувается, катетеры извлекаются. На место прокола накладывают тугую антисептическую повязку;
- пациента из операционной перевозят в отделение интенсивной терапии.
Криоабляция — современный метод лечения аритмий, который появился в медицинской практике совсем недавно, но успел зарекомендовать себя, как эффективный и безопасный. Ежедневно наши хирурги-аритмологи проводят эту операцию и видят, насколько она эффективна и безопасна. Если у вас есть опасения или сомнения, вы всегда можете позвонить нам и проконсультироваться со специалистом.
Радиочастотная катетерная абляция (РЧА) сердца.
Радиочастотная катетерная абляция (РЧА) сердца.
РЧА сердца – хирургическое катетерное вмешательство, с использованием специальных катетеров, пункционно введенных в полость сердца через сосуды, и радиочастотной энергии, направленное на устранение нарушений сердечного ритма (аритмии).
Радиочастотная абляция — один из самых современных методов лечения некоторых видов нарушений ритма сердца. Этот вид лечения относится к малоинвазивным вмешательствам, так как для его проведения не требуется никаких разрезов и доступов к сердцу, но иногда РЧА выполняется при операциях на открытом сердце. Радиочастотная абляция проводится с помощью тонкого гибкого катетера-проводника, который вводится через кровеносный сосуд и подводится к источнику неправильного ритма в сердце, вызывающего аритмию. Далее по этому проводнику подается радиочастотный импульс, который разрушает участок ткани, отвечающий за неправильный ритм. Впервые высокочастотную энергию для устранения дополнительных АВ-путей проведения, применяемую и по сей день, произвели в 1986 году М.Borggrefe и соавт. С этого времени и началось бурное развитие интервенционной аритмологии в лечении аритмий сердца.
Подобная деструкция патологического очага может осуществляться также путем прочих физических воздействий, в соответствии с чем выделяют и другие виды абляции:
- Лазерная абляция.
- Ультразвуковая абляция.
- Криодеструкция, т. е. абляция с применением низких температур.
Показаниями к проведению РЧ-абляции являются нарушения сердечного ритма, которые уже невозможно скорректировать медикаментозно:
- Мерцательная аритмия предсердий.
- Желудочковая и наджелудочковая тахикардия.
- Синдром Вольф-Паркинсона-Уайта, или синдром WPW.
- Пароксизмальные тахикардии.
Наряду с показаниями к РЧА, абляция имеет и перечень противопоказаний:
- Тяжелое общее самочувствие больного.
- Острые инфекционные заболевания.
- Тяжелые заболевания дыхательной системы и (или) почек.
- Эндокардит – воспаление внутренней оболочки сердца.
- Нестабильная стенокардия в течение 4 недель.
- Острый инфаркт миокарда.
- Сердечная недостаточность у пациента в стадии декомпенсации.
- Тяжелая артериальная гипертензия.
- Аневризма левого желудочка с тромбом.
- Наличие тромбов в полостях сердца.
- Гипокалиемия и прочие проявления электролитного дисбаланса в крови.
- Анемия, т. е. патология клеточного состава крови.
- Аллергическая реакция, вызванная рентгенконтрастным веществом.
- Йодонепереносимость
- Стеноз ствола левой коронарной артерии более 75%, высокая степень клапанного или подклапанного стеноза аортального клапана (при необходимости вхождения в полость ЛЖ)
- Тромбофлебит
- Двусторонняя ампутация конечностей
Радиочастотная (РЧ) энергия имеет широкий диапазон и зависит от сопротивления и диэлектрических свойств тканей. Радиочастотный ток – это ток с меняющейся полярностью при частоте от 30 кГц до 300 МГц. Все генераторы РЧ тока, используемые для аблации, работают в диапазоне 300 кГц — 1 МГц. Для аблации структур сердца применяют немодулированный ток, поскольку именно он приводит к образованию коагуляционного некроза.
Существует два варианта подачи электрической энергии: монополярный и биполярный. При монополярной аблации переменный ток проходит между дистальным концом «активного» электрода через ткани к «пассивному» электроду на поверхности грудной стенки. Обычно «пассивным» или референтным электродом служит пластина. Эксперименты показали, что позиция пластины незначительно влияет на размер воздействия, в то время как увеличение ее площади ведет к отклонению импеданса и приводит к увеличению энергии и перегреву электрода. В случае биполярной коагуляции ток проходит между двумя активными электродами в полостях сердца.
Ведущим механизмом коагуляции тканей под воздействие радиочастотного тока является превращение электрической энергии в тепловую. Если плотность тока высокая, а электропроводность низка, то это приводит к возбуждению ионов, которые начинают следовать изменениям направления переменного тока. Оба этих фактора имеют место в ткани окружающей «активный» электрод. Это возбуждение ионов ведет к образованию фрикционной теплоты так, что ткань прилегающая к электроду, а не сам электрод, является главным источником теплоты. Повышение температуры в миокардиальной ткани приводит к некоторым электрофизиологическим эффектам. На изолированных папиллярных мышцах свиных сердец было отмечено, что при температуре ткани 38-45°С в течение 1 минуты происходит повышение функции K-Na каналов клеток вплоть до критического уровня. Нагревание до 45-50°С ведет за собой инактивацию этих структур. Анормальный автоматизм клеток отмечен при повышение температуры свыше 45°С, повышенная возбудимость свыше 50°С. Биологическая смерть клеток зависит от двух факторов – времени воздействия и температуры. Обратимые клеточные изменения происходят при длительном нагревании даже при температуре ниже 45°С, в то время, как необратимая смерть клеток вероятно происходит между 52°С и 55°С. Денатурация внутреннего слоя протеинов мембран клеток играющего важнейшую роль в транспортных обменных процессах является важнейшим механизмом терминальной клеточной смерти. При температуре выше 100°С происходит испарение клеточной жидкости и повреждение клеточной мембраны миоцита, саркоплазматического ретикулума и митохондрий. Если температура превышает 140°С, может произойти карбонизация ткани. В этой связи с целью обеспечения более мягкой коагуляции тканей следует поддерживать температуру тканей на уровне ниже 100°С. Температуру ткани, находящейся в контакте с электродом, можно контролировать специальным катетером для аблации со встроенными в конец катетера термисторами или термопарами. Непосредственно разогревания электрода электрическим током не происходит вследствие его хорошей электропроводности.
Прогрессивное воздействие достигается благодаря созданным устройствам контроля температуры высокочастотной энергии (Haverkampf et al. 1991). Контроль температуры означает, что температура на конце катетера не только изменяется в течение процесса коагуляции, но и поддерживается на определенном уровне благодаря механизму обратной связи для подаваемой мощности. Такое устройство позволяет создавать ограниченное поражение с предсказуемой степенью in vitro и обеспечивает хороший контакт между электродом, вызывающим аблацию, и миокардом. Мониторинг температуры становится практически сложным при увеличении размера электрода или его геометрии. Так, например, для линейной аблации ФП и ТП используются удлиненные электроды, имеющие одну термопару, таким образом невозможно предсказать какой стороной происходит контакт поверхности электрода с эндокардом и температура краевой повехности может оказаться намного выше, чем тела электрода, где расположен термодатчик. Таким образом, температура в серединной точке остается недооцененной.
В некоторых экспериментальных исследованиях продемонстрирован трехмерный окончательный элементарный анализ влияния геометрии электрода, угла наклона контакта электрод-ткань и циркуляции окружающей крови на размер аблационного повреждения.
Длительность радиочастотной аблации так же является важным критерием, влияющим на трансмуральность воздействия. Наибольшее увеличение размера повреждения происходит в течение первых 30 секунд аблации, а затем наступает плато. Некоторое усовершенствование аблации было достигнуто в результате использования электрода с охлаждением наконечника инфузией физиологического раствора. Такая конструкция позволяет использовать высокие цифры энергии воздействия, увеличивая размер повреждения, но избегая при этом высоких цифр импеданса. Эта концепция была подтверждена в экспериментах in vivo и in vitro. Охлаждение в течение аблации приводит к повышению температуры глубже поверхности эндокарда. Максимальная температура регистрируется на глубине 1 мм и более от поверхности эндокарда, таким образом даже выше, чем в области контакта электрода с поверхностью эндокарда. Катетеры для холодовой аблации могут быть закрытого типа, когда охлаждающий раствор циркулирует внутри системы и открытого типа, имеющие маленькие дырочки через которые происходит орошение электрода и жидкость вытекает наружу.
Таким образом, радиочастотная аблация является безопасной и эффективной методикой. В ходе проведения экспериментальных исследований не отмечено возникновения таких серьезных осложнений, как аритмии, расстройства гемодинамики, ишемия, тромбоз или эмболия. Наибольшую опасность представляет собой перегревание и последующее повреждение аблационного катетера и выпаривание ткани. С целью ограничения риска этих осложнений многие исследователи считают необходимым проводить измерение биофизических параметров (сила тока, напряжение, температура) на конце катетера.
Возможные осложнения РЧА сердца делятся на 4 группы:
1. Осложнения, обусловленные лучевой нагрузкой (примерно 1 миллизиверт) — 2. Осложнения, связанные с пункцией и катетеризацией сосудов (повреждение артерий, тромбофлебит, артериовенозная фистула, пневмоторакс); 3. Осложнения при катетерных манипуляциях (повреждение клапанов сердца, эмболия – системная или в легочную артерию, перфорация коронарного синуса или стенки миокарда, перфорация сердца, тампонада, инфекция – системная или в месте пункции);
4.Осложнения, обусловленные радиочастотным воздействием (АВ-блокада)
5. Случайное нарушение целостности тканей сердечной мышцы в момент абляции.
6. Сбои в работе электрической системы сердца, усугубляющие нарушение сердечного ритма и требующие трансплантации кардиостимулятора.
7. Стеноз легочных вен, т. е. сужение их просвета.
Осложнения после РЧА сердца крайне редки: вероятность негативных последствий абляции не превышает 1%. Потому РЧА причисляется к категории операций с малой степенью риска. Однако для профилактики осложнений существует ряд специальных мер, принимаемых на каждом из этапов обнаружения и лечения тахикардии.
Риск подобных осложнений повышается в тех случаях, когда пациент является диабетиком, если у него нарушена свертываемость крови, а также если он преодолел 75-летний возрастной порог.
Данная операция относится к классу малоинвазивных вмешательств. Преимущества же такого хирургического вмешательства очевидны: минимальная травматичность, как правило, отсутствие необходимости в назначении общей анестезии, небольшая продолжительность операции, короткий послеоперационной койко-день
Как подготовиться к РЧА.
Подготовка к данной операции заключается в проведении электрофизиологического исследования (ЭФИ) сердца. Необходимость РЧА у конкретного пациента констатируется его лечащим врачом на основании истории заболевания и данных таких диагностических методов, как:
- Электрокардиография (ЭКГ) – популярный метод электрофизиологической инструментальной диагностики, основанный на регистрации и исследовании электрических полей, которые образуются при работе сердца;
- Длительная регистрация ЭКГ (ХМЭКГ) – электрофизиологическая диагностика, суть которой заключается в непрерывном регистрировании электрокардиограммы на протяжении минимум 24 часов.
После регистрации с помощью ЭКГ приступа тахикардии пациент госпитализируется в стационар для прохождения полного курса обследования и сдачи перечня необходимых анализов, на основе которых ему может быть назначена радиочастотная абляция сердца:
- Лабораторные анализы крови (биохимический анализ, исследование гормонального фона, определение уровня липидов, электролитов и т. п.);
- Стресс-тест, эхокардиография;
- Ультразвуковое исследование сердца (УЗИ);
- Магнитно-резонансная томография (МРТ).
Общие принципы подготовки к операции включают в себя: • Последний прием пищи вечером накануне операции (12 часов голода). • В месте установки катетера (паховая и подключичная область) должны быть выбриты волосы
• В ночь перед исследование проводиться очищение кишечника. • Спросите своего врача, следует ли вам принимать обычные лекарства утром. • Все антиаритмические препараты отменяются за 2–3 дня до исследования (пять периодов полувыведения), для кордарона это 28 дней. • Если у вас сахарный диабет, спросите своего врача, следует ли Вам принимать инсулин или другие сахароснижающие пероральные препараты перед исследованием.
Методика проведения РЧА сердца.
РЧА сердца проводится в плановом порядке в специально оборудованной операционной, оснащенной:
• рентгенотелевизионной системой для рентгеноскопии и/или рентгенографии; • оборудованием для слежения за жизненно важными функциями организма и проведения реанимационных мероприятий (дефибриллятор, дыхательный аппарат, мониторы);
• специализированным ЭФИ-оборудованием для записи поверхностных электрокардиограмм и внутрисердечных электрограмм и снабженным • специализированным электрокардиостимулятором и набором инструментов для проведения катетеризации сердца и электродов-катетеров для проведения ЭФИ и РЧА;
• защитным оборудованием для пациента и персонала (костюмы, фартуки, очки, передвижные стенки и т. д.).
Пациент для проведения операции РЧА поступает в операционную натощак, в слегка седатированном состоянии. Области предполагаемых пункций сосудов тщательно обрабатываются и накрываются стерильным бельем. Проведение катетеров всегда производится с использованием чрескожной техники. Для пункции используются обычно бедренные вены справа и/или слева, подключичная вена слева и/или справа и яремная вена справа, а также вены предплечья. Для артериального доступа обычно используется правая бедренная артерия, однако возможна пункция бедренной артерии слева и лучевых артерий.
Местная анестезия места пункции, после этого производится пункция вены с помощью иглы, которая вводится в сосуд, и проводится необходимой длины проводник, после чего игла вытаскивается. Далее по проводнику вводится интродьюсер, а затем электрод-катетер в соответствующую камеру сердца. Разместив катетеры в различных камерах сердца, их подключают к соединительной коробке, которая переносит электрические сигналы от электродов в сердце к записывающему оборудованию и позволяет стимулирующему импульсу от ЭКС достигать поверхности различных камер сердца. Выполняется ЭФИ сердца. Электрические сигналы, полученные от эндокардиальной поверхности сердца, фильтруются, усиливаются и выводятся на мониторе компьютера. Программируемый ЭКС должен обладать способностью для постоянной и программируемой стимуляции, подачи множества экстрастимулов (до 7), регулировки амплитуды и длительности импульса, а также возможностью воспринимать внешние и внутрисердечные сигналы.
При проведении ЭФИ пациент может ощущать дискомфорт в грудной клетке, сердцебиения, небольшую болезненность. Ощущения, возникающие при проведения ЭФИ, в виде перебоев сердца, секундных остановок, ускорения или замедления ритма являются результатом работы врача, т.е с помощью электрических импульсов, подаваемых непосредственно в сердце, врач полностью контролирует сердцебиение, провоцируя приступ сердцебиения или прекращая его во время поиска аритмогенных участков. При обнаружении аритмогенных зон (дополнительных предсердно-желудочковых соединений, эктопической активности и т. п.) на нее воздействуют радиочастотной энергией с помощью «лечебного» электрода. После чего в обязательном порядке (примерно через 20 минут) проводят еще раз ЭФИ для оценки эффективности воздействия. Если электрофизиологические показатели удовлетворяют врача, то операцию заканчивают. Удаляют катетеры. На места пункций накладывают гемостатические (давящие) повязки.
Вас переводят в отделение и назначают постельный режим в положении на спине на несколько часов (в некоторых случаях до суток) с целью предупреждение кровотечения из места пункции. Наблюдение в стационаре от одного до 3 дней.
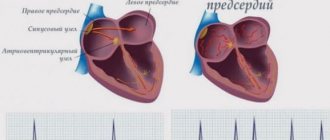
Хирургическое лечение фибрилляции предсердий
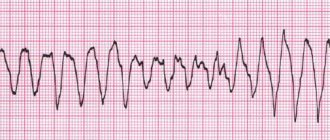
Фибрилляцией предсердий (ФП) в медицинской терминологии называется нарушение ритма сердца (мерцательная аритмия). Оно может быть спровоцировано повышенным количеством электрических контуров в предсердиях, которые приводят к беспорядочным сокращениям желудочков сердца и к недостаточности эффективного сокращения предсердий. Это, в свою очередь, становится причиной образования сгустков крови в предсердиях, что может в итоге привести к закупорке сосудов головного мозга и смерти пациента.
Среди основных методов лечения при мерцательной аритмии на сегодняшний день – медикаментозная терапия, катетеризация, а также хирургическая лабиринтная методика (Maze) – довольно сложная и потому не очень популярная среди кардиохирургов.
«Новым словом» в лечении мерцательной аритмии стала радиочастотная абляция сердца (РЧА) устьев легочных вен – малоинвазивная операция путем небольших проколов, осуществляемая с применением последних компьютерных технологий и в условиях постоянного рентгеновского контроля.
После абляции: хаотичные импульсы, провоцирующие аритмию, не могут попадать в полость предсердия
Реабилитация после РЧА
В целом реабилитация после РЧА длится несколько месяцев, в течение которых пациенту может быть назначен прием антиаритмических препаратов (к примеру, «Пропафенон», «Пропанорм» и др.), в том числе и тех, которые больной принимал до абляции. Постельный режим с контролем сердечного ритма и артериального давления показан больному лишь в самые первые сутки после операции, в течение которых происходит быстрое восстановление и стабилизация нормального общего самочувствия пациента. Необходимость же повторной РЧА, как показывает практика, у прооперированных пациентов возникает реже, если пациент пересмотрит свой привычный образ жизни:
- Ограничит потребление напитков с алкоголем и кофеином;
- Снизит объем соли в своем рационе;
- Станет придерживаться соответствующей диеты;
- Выберет оптимальный режим физической активности;
- Бросит курить и откажется от других вредных привычек.
Результаты абляции
Абляция сердца может быть успешной, но некоторым больным приходится повторять процедуру. Возможно, придется принимать лекарственные препараты, даже после проведения абляции.
После операции
После абляции пациент находится под присмотром наших специалистов в палате послеоперационной реабилитации. Первые несколько часов медицинский персонал следит за жизненными показателями больного, сердечным ритмом и болевыми симптомами. Первые сутки пациенту предписан постельный режим. За это время сердце перестроится на новый ритм, начнет заживать рана в месте введения катетера. На вторые сутки разрешается постепенно вставать и медленно передвигаться по палате. Если все показатели в норме, больного выписывают на 3 день. Перед выпиской пациента осматривает врач, дает свои рекомендации и памятку по реабилитации.
Криобляционная терапия весьма действенная и способна полностью избавить пациента от аритмии, но эффект от проведенной операции во многом зависит от самого пациента. В период реабилитации (1-3 месяцев) необходимо выполнять все предписания врача и рекомендации по восстановлению:
- избегать тяжелых физических нагрузок;
- избегать психоэмоционального перенапряжения и стрессов;
- отказаться от закаливания, горячих ванн, походов в баню и других мероприятий с возможными перепадами температур;
- следить за правильным питанием и соблюдать диету: отдать предпочтение вареным блюдам, а не жареным, исключить жирные продукты, не употреблять фастфуд, отказаться от чрезмерного употребления соли и сахара, добавить в рацион рыбу, нежирное мясо, свежие овощи и фрукты;
- отказаться от вредных привычек (курение, употребление алкоголя, переедание);
- прием лекарственных препаратов согласовывать с лечащим врачом;
- своевременно посещать кардиолога для планового осмотра. ЭКГ необходимо сделать через месяц после операции, потом через 3 и 6 месяцев.
Лечение аритмии сердца — прижигание: цена, стоимость такой операции по восстановлению ритма
Любого пациента волнует вопрос стоимости той или иной медицинской манипуляции. В России многие операции проводятся бесплатно, их оплачивает государство. На вопрос, входит ли лечение аритмии сердца, а именно прижигание в перечень бесплатных услуг, вам ответит только врач.
Однако, стоит заметить, что хорошие специалисты, которые проводят подобные манипуляции, находятся в столице и других больших городах. Лечение в данном случае может варьироваться в пределах 300 000 рублей. Цена операции по восстановлению ритма в Израиле или Германии может доходить до 20 000 евро. В стоимость будет входить полная диагностика до лечения, сама манипуляция и реабилитация.