© Автор: З. Нелли Владимировна, врач НИИ трансфузиологии и медицинских биотехнологий, специально для СосудИнфо.ру (об авторах)
Вазодилататоры или сосудорасширяющие препараты представляют собой группу медикаментозных средств, выпускаемых в различных лекарственных формах (таблетки, капсулы, растворы для инъекций), относимых к различным фармацевтическим группам и назначаемых при артериальной гипертензии и многих патологических состояниях сосудов головного мозга, сердца, позвоночника, верхних и нижних конечностей.
Разнородная группа
Сосудорасширяющие препараты способны различным образом (в зависимости от их механизма действия) оказывать влияние на сосудистые стенки, снижать их тонус и, за счет этого, увеличивать диаметр сосудов, улучшая в них кровоток. Однако не все фармацевтические средства, отнесенные к данной категории, в одинаковой степени воздействуют на различные типы кровеносных сосудов. В «компетенции» каждой из групп этих медикаментов находятся сосуды, имеющие определенный калибр (артериолы, артерии, венулы, магистральные сосуды) и принадлежащие конкретным тканям и органам.
расширение сосуда и улучшение кровотока под действием вазодилататора
К примеру, для расширения мелких сосудов микроциркуляторного русла таких органов, как глаза, почки, применяются одни препараты, а для воздействия на мелкие сосуды кожных покровов, верхних и нижних конечностей используются другие сосудорасширяющие средства (периферические вазодилататоры).
В таком случае можно предположить, что сосуды сердца вряд ли «почувствуют» действие предыдущих лекарств, им нужны свои, особые препараты, что на самом деле и происходит. Для расширения коронарных сосудов при лечении стенокардии либо сердечной недостаточности назначают препараты из группы сердечных вазодилататоров. В целом, с учетом механизма действия и принадлежности сосуда (артериальное или венозное русло), на который оказывают преимущественное влияние вазодилататоры, различают три подгруппы сосудорасширяющих препаратов:
- Средства, воздействующие на артериолы (прямые артериальные вазодилататоры): альфа-неселективные адреноблокаторы (АБ), гидралазин, антагонисты кальция;
- Лекарства, в «круг интересов» которых входят венулы: органические нитраты (нитроглицерин, нитронг);
- Препараты, оказывающие одновременное влияние на одни (артериолы) и другие (венулы) сосуды: неорганические нитраты, альфа-1-неселективные АБ.
Помимо этого, современная фармакологическая отрасль располагает и такими сосудорасширяющими средствами, которые наделены возможностями увеличивать просвет сосудов крупного калибра и магистралей. Это – системные вазодилататоры, они способны в короткие сроки уменьшать значения артериального давления и повышать интенсивность кровоснабжения во всех тканях организма.
применимость вазодилататоров в зависимости от фармакологической группы
Доктор, прежде чем назначить препараты той или иной группы, изучает не только состояние пациента, вызванное происходящим в его организме патологическим процессом, но и берет во внимание состояние кровеносных сосудов больного.
№ 12. Прямые вазодилататоры в лечении артериальной гипертензии
Вы читаете цикл статей о гипотензивных (антигипертензивных) препаратах. Если вы хотите получить более целостное представление о теме, пожалуйста, начните с самого начала: обзор гипотензивных средств, действующих на нервную систему.
Рассказывая о препаратах, использующихся в лечении гипертонии (артериальной гипертензии), нельзя пропустить группу прямых вазодилаторов
, потому что без нее обзор будет недостаточно полным.
Вазодилататор
(ударение на предпоследний слог) в дословном переводе означает «
расширяющий сосуд
», «
сосудорасширитель
» (от лат.
vas
,
vasis
— сосуд,
dilatatio
— расширение). По правилам латинского языка, латинская буква
l
обозначает мягкий звук [
ль
], поэтому более правильно использовать термин
вазодилЯ
таторы
, но латинский язык изучается на 1-м курсе и во многом забывается к окончанию медвуза. Я буду использовать более распространенный вариант с твердым [л
].
Вазодилататоры по механизму действия
делят на прямые и непрямые. К
непрямым вазодилататорам
относят:
- альфа1-адреноблокаторы и неселективные альфа-адреноблокаторы,
- блокаторы серотониновых рецепторов,
- антагонисты кальция,
- ингибиторы АПФ
(важная группа лекарств, разговор о ней впереди) и др.
К прямым вазодилататорам
, напрямую расширяющим кровеносные сосуды, относят 4 типичных препарата (
гидралазин, миноксидил, диазоксид, нитропруссид натрия
) и группу
нитратов
(
нитроглицерин
и др.). Нитраты — отдельная важная группа лекарств, применяющихся для снятия ишемических болей при стенокардии, о ней нужен отдельный разговор.
Таким образом, в настоящее время под прямыми вазодилататорами
обычно имеют в виду всего
4 препарата
:
- гидралазин,
- миноксидил,
- диазоксид,
- нитропруссид натрия.
Что желательно знать
из сегодняшней темы?
- Три первых препарата (гидралазин, миноксидил, диазоксид
) расширяют
только мелкие артерии
(артериолы), в том время как нитропруссид натрия расширяет также и
венозные сосуды
. - Все 4 препарата обладают большим количеством побочных эффектов
(некоторые ПЭ из них весьма любопытны!) и с целью лечения артериальной гипертензии используются редко. - Все прямые вазодилататоры вызывают задержку жидкости
в организме (отеки) и
сердцебиение
(тахикардию). - Гидралазин
(точнее, аналог
дигидралазин
) входит в состав комбинированных лекарственных средств:
адельфан
и
адельфан-эзидрекс
. Применять их длительно нежелательно. - Применение миноксидила
внутрь выявило необычный побочный эффект — усиленный рост волос, поэтому миноксидил сейчас применяется наружно для лечения
мужского типа облысения
(андрогенная алопеция). - Диазоксид
тоже имеет редкий побочный эффект: он
тормозит секрецию инсулина
поджелудочной железой и потому применяется в эндокринологии для повышения уровня сахара в крови. - Нитропруссид натрия
вводится только внутривенно, действует быстро, но очень недолго. Поскольку нитропруссид натрия расщепляется до цианидов, то его передозировка внешне очень напоминает кому при отравлении
угарным газом
(СО).
А теперь по каждому препарату немного подробнее.
Гидралазин
Гидралазин является прямым периферическим вазодилататором, действующим на артериолы. Расширение сосудов связывают с торможением фосфорилирования миозина — белка, участвующего в мышечном сокращении. Гидралазин вызывает рефлекторную тахикардию
(увеличение ЧСС). При длительном использовании развивается
толерантность
(привыкание) к действию гидралазина.
Исследования в СССР в 1985-1988 гг. показали, что монотерапия гидралазином в течение 1 года оказалась малоэффективно
й при мягкой и умеренной гипертонии (эффект был достигнут лишь у 23% больных по сравнению с 50% у пропранолола). При значительной АГ (нижнее АД выше 114 мм рт. столба) гидралазин
не помог ни в одном случае
.
Гидралазин отсутствует в аптеках и отдельно не используется
из-за низкой эффективности и обилия побочных эффектов. Он может быть назначен как дополнительный препарат в комбинации с
мочегонными
и бета-адреноблокаторами. У пожилых людей должен применяться в меньшей дозировке.
Гидралазин в настоящее время сохраняет некоторое значение, потому что в аптеках до сих продаются недорогие комбинированные антигипертензивные препараты в форме таблеток: адельфан
и
адельфан-эзидрекс
(подробнее о них я писал в теме про симпатолитики). Около 20 лет назад
адельфан
был очень популярен среди пенсионеров, потому что других более-менее эффективных препаратов от гипертонии было мало. Помимо
дигидралазина
, в состав
адельфана
входит симпатолитик
резерпин
, в то время как
адельфан-эзидрекс
дополнительно включает распространенное мочегонное
гидрохлортиазид
. Дигидралазин отличается от гидралазина
большей предсказуемостью эффекта
, поскольку скорость распада дигидралазина в организме не зависит от генетических особенностей пациента (бывают так называемые
быстрые
и
медленные ацетиляторы
).
Побочные эффекты
гидралазина:
- из-за рефлекторной симпатической стимуляции сердца и почек возникают тахикардия
и
отеки
(задержка жидкости в организме), - возможны ишемические изменения на ЭКГ вплоть до развития инфаркта миокарда (это напоминает побочные эффекты нифедипина),
- через 0.5-2 года лечения появляются аутоиммунные реакции
. В 80% случаев это артриты (воспаление суставов) и артралгии (боли в суставах), но также бывают гломерулонефрит (воспаление почечных клубочков), волчаночный синдром (напоминает системную красную волчанку) и др. - возможны тромбоцитопения
(уменьшение количества тромбоцитов в крови) и даже
панцитопения
(уменьшение количества всех клеток в крови), - периферический неврит, нейропатия
(поражение нервов). В этом случае должен назначаться
пиридоксин
(витамин B6), - желудочно-кишечные расстройства (тошнота, диарея),
- кожная сыпь,
- импотенция,
- слезотечение или конъюнктивит,
- заложенность носа и др.
Обилие побочных эффектов, в том числе аутоиммунных, не позволяет использовать комбинированный препарат адельфан
(адельфан-эзидрекс) длительно.
Миноксидил
Миноксидил, как и гидралазин
, оказывает прямое сосудорасширяющее действие на артерии. Поскольку препарат не расширяет венозное русло, то он
не вызывает ортостатической гипотонии
(
резкое падение АД с обмороком при переходе из горизонтального в вертикальное положение
). Снижение АД сопровождается
рефлекторной тахикардией
и увеличением
ударного объема
(
количество крови в мл, выбрасываемой сердцем за 1 сокращение
), а так же
задержкой натрия и воды
(отеки). Миноксидил обладает ренопротективным эффектом (защищает почки от последствий высокого артериального давления).
Из-за многочисленных побочных эффектов миноксидил
(таблетки) сейчас
не применяется для лечения артериальной гипертензии
, несмотря на эффективность даже при гипертонических кризах. Действие препарата наступает недостаточно быстро (начало через 0.5-1 часа, пик — через 4-8 часов). Миноксидил считается препаратом 4-й линии лечения АГ и обычно назначается только в сочетании с
бета-адреноблокаторами
или
ингибиторами АПФ и мочегонными
.
Побочные эффекты
миноксидила при использовании внутрь и парентерально (в/в, в/м):
- тахикардия и сердцебиение (из-за рефлекторной стимуляции симпатической нервной системы),
- отеки и задержка жидкости,
- снижение сегмента ST и изменения зубца T в отведениях I и V4-V6 (в 90% случаев в первые 2 недели),
- стенокардия напряжения, инфаркт миокарда,
- выпотной перикардит (воспаление перикарда с накоплением жидкости в полости околосердечной сумки
) из-за задержки жидкости и неадекватного усиления кровотока в перикарде и миокарде, - легочная гипертензия,
- пульсирующая головная боль, нарушение зрения,
- временный подъем в крови уровня щелочной фосфатазы, мочевины, креатинина,
- желудочно-кишечные нарушения,
- полименорея (обильные месячные
), - кожная сыпь и др.
Также может возникать болезненность грудных желез, гинекомастия
(
увеличение и уплотнение зачатков молочной железы у мужчин, нередко болезненное
), сексуальные нарушения.
Особо нужно выделить такой побочный эффект, как гипертрихоз
(
чрезмерная волосатость
) и
гирсутизм
(
избыточный рост темных, жестких, длинных волос волос по мужскому типу у женщин
). Гипертрихоз возникает почти у всех пациентов при приеме миноксидила внутрь более 4 недель — волосы растут на висках, на лбу, лице, на ушных раковинах и других волосистых участках тела. Это обусловлено повышением уровня
тестостерона
(мужской половой гормон) и усилением кожного кровотока. Гипертрихоз и гирсутизм ограничивают применение препарата у женщин, хотя это проходит через 1-2 месяца после прекращения приема.
Способность миноксидила вызывать рост волос сейчас используется именно для лечения андрогензависимого облысения
(мужской тип облысения). При местном применении (раствор
Регейн
, спрей
Генеролон
и др.) миноксидил почти не всасывается и потому не оказывает обычных побочных эффектов. Считается, что рост волос связан с расширением сосудов и улучшением кровообращения и питания волосяных луковиц в коже, что стимулирует их переход из фазы покоя в фазу роста.Максимальный эффект
миноксидила достигается в начале облысения (не позже 10 лет, лучше до 3-5 лет), у молодых пациентов, при локализации лысины в области темени размером не более 10 см и наличии в центре лысины более 100 волос разного типа. Миноксидил неэффективен при потере волос из-за приема лекарств, нарушения питания (дефицит витамина A, железа и т.д.), тугих причесок («хвост», «пучок»). Рост волос обычно начинается через 4 месяца ежедневного лечения. После отмены препарата рост новых волос прекращается и через 3–4 месяца возможно восстановление залысин на прежних местах.
Диазоксид
Диазоксид по химической структуре является производным тиазидных диуретиков
(к ним относится
гидрохлортиазид
), хотя сам мочегонным эффектом не обладает. Как и другие прямые вазодилататоры, вызывает
задержку натрия и воды
(возможны отеки). Действует только на артериолы. При внутривенном введении диазоксид быстро снижает систолическое и диастолическое АД с увеличением ЧСС и потому может применяться для лечения гипертонических кризов при неэффективности других препаратов.
Диазоксид тормозит выделение инсулина
из поджелудочной железы, что приводит к росту уровня сахара в крови, поэтому препарат сейчас применяется в основном для
лечения врожденного гиперинсулинизма
(бывает у 1 на 50 тыс. человек).
Также диазоксид оказывает сильный релаксирующий (расслабляющий) эффект на матку
. Если ввести препарат во время родов, то роды остановятся.
Побочные эффекты
диазоксида:
- отеки и сердечная недостаточность (чаще у детей),
- гипотония, тахикардия, ишемия миокарда,
- кожная сыпь,
- кетоацидоз,
- изменение вкусовых ощущений, тошнота и рвота,
- гипертрихоз, гирсутизм,
- головная боль, головокружение, шум в ушах,
- изменения содержания клеток крови и др.
Нитропруссид натрия
Прямой дилататор артериол и вен
(в отличие от трех предыдущих, действующих лишь на артериолы). Нитропруссид натрия применяется
только внутривенно
, оказывает мгновенное (через 30-60 секунд) действие, хотя оно непродолжительно и
завершается через 3-5 минут
после прекращения инфузии. Препарат увеличивает ЧСС в малой степени.
Нитропруссид натрия хорошо снижает нагрузку на сердце и потому особо эффективен при острой левожелудочковой недостаточности
, обусловленной повышенным артериальным давлением. Препарат расширяет сосуды сердца и улучшает кровоснабжение миокарда при инфаркте и нестабильной стенокардии. Гипотензивный эффект нитропруссида натрия обусловлен нитрозогруппой, поэтому действие препарата похоже на эффекты
нитроглицерина
. Нитропруссид натрия тормозит агрегацию тромбоцитов, т.е. замедляет свертывание крови и образование тромбов.
Недостатки
нитропруссида натрия:
- высокая стоимость,
- необходимость точного дозирования (нужны специальные дозаторы
) с тщательным контролем АД, - после прекращении инфузии возможен тяжелый синдром отмены
с подъемом АД, - побочные эффекты.
Дозатор-инфузомат
. Моторчик прибора с настраиваемой скоростью давит на поршень шприца, раствор препарата по трубочке постоянно поступает в капельницу и вводится больному внутривенно.
Показания
к применению нитропруссида натрия:
- гипертонические кризы,
- управляемая гипотензия во время хиругических операций,
- острый инфаркт миокарда без гипотонии,
- артериальные спазмы, устойчивые к применению нитроглицерина.
Нитропруссид натрия в эритроцитах превращается в цианиды
, они в свою очередь в крови реагируют с тиосульфатами и в печени превращаются в
тиоцианаты
, которые затем выводятся почками в течение нескольких дней.
Цианиды токсичны
, т.к. являются солями мощного яда —
синильной кислоты
, которая блокирует фермент
цитохромоксидазу
в дыхательной цепи, полностью прекращая усвоение кислорода тканями и приводя к смерти. При нарушенной работе печени риск отравления возрастает. Скорость инфузии нитропруссида натрия не должна превышать способность организма удалять цианиды и не должна длиться больше 24 часов.
- При низком АД применение нитропруссида противопоказано.
- Беременным также нельзя, поскольку нитропруссид проникает сквозь плаценту.
- При расслаивающей аневризме аорты нитропруссид натрия можно использовать только в сочетании с внутривенными бета-блокаторами, поскольку препарат увеличивает скорость выброса крови из желудочков, а это может способствовать распространению аневризмы.
Побочные эффекты
нитропруссида натрия:
- боли в желудке, тошнота, рвота,
- резкая гипотония,
- нефротоксичность (токсическое действие на почки),
- тахикардия, одышка,
- головная боль, головокружение, потеря сознания,
- нервозность,
- дефицит витамина B12 (цианокобаламин
).
При большой скорости введения нитропруссида натрия могут развиться проявления цианидного или тиоцианидного отравления с клинической картиной комы
:
- розовый цвет кожи,
- слабый пульс и дыхание,
- расширение зрачков.
При длительной инфузии и при нарушении функции почек необходимо контролировать уровень тиоцианидов
в плазме крови.
Розовый цвет кожи
(не меняется даже у трупа) в сочетании с сильной одышкой бывает в 2 случаях: при отравлении
цианидами (синильной кислотой)
и при
отравлении угарным газом
(CO). Однако наличие
запаха горького миндаля
исключает отравление CO (т.е. при отравлении цианидами будет наблюдаться розовый цвет кожи и запах горького миндаля).
Горький миндаль содержит гликозид амигдалин
, который (под влиянием фермента эмульсина) легко разлагается на сахар, бензальдегид и синильную кислоту. Поэтому семена горького миндаля, содержание амигдалина в которых доходит до 3,5 %, нельзя употреблять в пищу.
Продолжение следует…
Одни и те же лекарства, а болезни – разные
Больше всего пациенты осведомлены о таблетках, назначаемых при гипертонии, при остеохондрозе, либо о сосудорасширяющих средствах, весьма полезных для головного мозга и для нижних конечностей, в общем, о тех лекарствах, которые лечат наиболее распространенные болезни нашего времени.
Для головного мозга
Например, для головного мозга, вернее, улучшения его кровоснабжения и питания, но в зависимости от характера нарушения мозгового кровообращения, нередко подходят представители разных фармакологических групп:
- Антагонисты кальция, препятствующие проникновению Са++ в клетку (циннаризин, нимодипин);
- Миотропные спазмолитики, расслабляющие гладкую мускулатуру сосудов (но-шпа, папаверин);
- Алкалоиды спорыньи (за счет их альфа-адреноблокирующей способности: дигидроэрготоксин, вазобрал);
- Средства, корректирующие мозговое кровообращение, которые называются сосудистыми препаратами (кавинтон, компламин, трентал, никотиновая кислота);
- Сосудорасширяющие средства, блокирующие адренорецепторы (адреноблокаторы: атенолол, тимолол, пропранолол, метопролол);
- Другие лекарства, обладающие способностью воздействовать на сосуды и увеличивать их просвет, улучшая тем самым мозговое кровообращение (винкамин, курантил, магния сульфат, дибазол).
При гипертонии
Применение сосудорасширяющих препаратов при гипертонии, как правило, подразумевает использование их и для головного мозга, который в условиях сужения сосудов по причине артериальной гипертензии испытывает серьезные страдания, недополучая питательные вещества, переносимые кровью. В первую очередь, это блокаторы медленных кальциевых каналов и адреноблокаторы.
Между тем, список препаратов, назначаемых при гипертонии настолько велик, что перечислить всех представителей просто невозможно. Бывают случаи, когда артериальное давление требует немедленного и быстрого снижения. Разумеется, такие лекарства, как, скажем, бензогексоний (ганглиоблокатор), который в подобных случаях может быть применен, не терпят самостоятельного назначения. Данные лекарственные средства в большинстве своем довольно серьезны, требуют индивидуального подбора и обязательного участия врача. В качестве примера можно привести:
- Препараты, которые угнетающе действуют на сосудодвигательный центр (клофелин, допегит);
- Вещества, способные блокировать передачу нервных импульсов в ганглиях ВНС (ганглиоблокаторы): бензогексоний, пентамин, пирилен;
Наоборот, попытка быстро справиться с кризом с помощью, например, амлодипина (блокатор медленных кальциевых каналов) также не приведет к успеху.
Но все же чаще врачам приходится иметь дело с гипертониками, которые должны принимать лекарства, поддерживающие АД на определенном уровне. Как правило, такие препараты выпускаются в таблетках или капсулах и не доставляют хлопот пациентам. Люди пьют их годами, постепенно увеличивая дозировку «своего» лекарства или по рекомендации (и после подбора) переходят на другие группы сосудорасширяющих средств, если привычные таблетки перестали действовать или вызвали какой-то побочный эффект.
Таким образом, при гипертонии для поддержания АД в границах нормы чаще всего назначаются следующие группы медикаментозных средств, которые, впрочем, также подбираются в индивидуальном порядке, однако в аптеке, в основном, отпускаются без рецепта:
- Адреноблокаторы (альфа- и бета-адреноблокаторы);
- Блокаторы медленных кальциевых каналов;
- Ингибиторы ангиотензинпревращающего фермента (иАПФ);
- Антагонисты ангиотензина II;
- Ингибиторы ренина.
Списки препаратов – главных представителей вышеперечисленных групп в данном разделе не приводятся, поскольку ниже последует более детальное описание этих сосудорасширяющих средств.
При остеохондрозе
Люди, столкнувшиеся с такой проблемой, как шейный остеохондроз, наверняка, могут поведать, что по причине подобной болезни сосуды головы постоянно пребывают в некомфортных для себя условиях. Все это изменяет артериальное давление, отражается на состоянии памяти и внимания (голова становится «тяжелой» и «туго соображающей»), а также на общем самочувствии (боли, дискомфорт, нарушение сна, снижение трудоспособности). Не исключают применения сосудорасширяющих средств и поражения других отделов позвоночника. Таким образом, при остеохондрозе, помимо противовоспалительных препаратов (НПВП), миорелаксантов типа мидокалма, средств, оптимизирующих течение метаболических процессов в тканях (милдронат, рибоксин) и витаминов группы В, используются и сосудорасширяющие средства (ксантинола никотинат, но-шпа, папаверин), роль которых состоит в улучшении кровоснабжения тканей.
Для нижних конечностей
Сосудорасширяющие препараты применяются также при заболеваниях сосудов рук и ног. Однако нарушение питания тканей в результате сужения кровеносных сосудов больше характерно для нижних конечностей, поэтому вопросы лечения таких патологических состояний затрагиваются чаще и сосудорасширяющие средства, в числе которых значатся и периферические вазодилататоры, используются преимущественно для нижних конечностей (в основном, при облитерирующем эндартериите, атеросклерозе, диабетической ангиопатии):
- Миотропные спазмолитики (папаверин, но-шпа, дротаверин);
- Средства с аденозиновым механизмом действия (курантил, парседил);
- Алкалоиды спорыньи (вазобрал, сермион);
- Лейкотриены и простагландины (вентавис, вазапростан);
- Производные пурина (агапурин, трентал, пентоксифиллин);
- Ганглиоблокирующие препараты (пентамин, димеколин, бензогексоний);
- Антагонисты кальция (фелодипин, нифедипин, октидипин);
- Адреноблокаторы (фентоламин);
- Ингибиторы ангиотензинпревращающего фермента (эналаприл, лизиноприл, рамиприл).
Перечисление препаратов можно было бы продолжать до бесконечности, между тем, читатель, вероятно, заметил, что многие группы и названия представителей уже встречались в перечнях, рекомендуемых для лечения других болезней.
Газета «Новости медицины и фармации» 19 (436) 2012
Хроническая сердечная недостаточность (ХСН) представляет собой серьезную медико-социальную и финансовую проблему. ХСН страдает почти 1,5–2 % всего населения земного шара, а заболеваемость составляет 5–10 случаев на 1000 человек ежегодно. Распространенность ХСН в европейской популяции достигает 2,0 %, в США — 2,2 %, в России — 6 % и значительно увеличивается с возрастом. Согласно данным Роттердамского исследования, распространенность ХСН среди лиц в возрасте 55–64 лет составляет 1 %, в возрасте 75–84 лет — 7 %, а среди лиц старше 85 лет — более 10 %. На оказание медицинской помощи больным с хронической сердечной недостаточностью расходуется 2–3 % всех средств, выделяемых на нужды здравоохранения. При этом 70–80 % всех финансовых затрат на ХСН приходится на оплату стационарного лечения пациента в связи с декомпенсацией заболевания.
Хроническая сердечная недостаточность — это синдром, развивающийся в результате различных заболеваний сердечнососудистой системы, приводящих к снижению насосной функции сердца, хронической гиперактивации нейрогормональных систем, и проявляющийся одышкой, сердцебиением, повышенной утомляемостью, ограничением физической активности и избыточной задержкой жидкости в организме.
Следует отметить, что врачам общей практики необходимо помнить, что выраженность симптомов ХСН может быть совершенно различной — от минимальных проявлений, возникающих только при выполнении значительных нагрузок, до тяжелой одышки, не оставляющей пациента даже в состоянии покоя. ХСН — это прогрессирующий синдром, и те пациенты, которые сегодня имеют лишь скрытую симптоматику, в течение 1–5 лет могут перейти в группу самых тяжелых больных, плохо поддающихся лечению. Поэтому ранняя диагностика ХСН, а следовательно, и раннее начало лечения таких больных — залог успеха в терапии сердечной недостаточности.
Синдром ХСН может осложнять течение практически всех заболеваний сердечнососудистой системы. Но главными причинами, составляющими более половины всех случаев, являются ишемическая болезнь сердца (ИБС), артериальная гипертензия или сочетание этих заболеваний. При ИБС развитие острого инфаркта миокарда с последующим очаговым снижением сократимости миокарда и дилатацией полости левого желудочка (ремоделирование) является наиболее частой причиной ХСН. При длительно существующей хронической коронарной недостаточности без инфаркта миокарда может прогрессировать потеря жизнеспособности миокарда, диффузное снижение сократимости, дилатация камер сердца и развитие симптомов ХСН. Эта ситуация трактуется в мире как ишемическая кардиомиопатия. При артериальной гипертензии изменения миокарда левого желудочка, получившие название «гипертоническое сердце», также могут быть причиной ХСН. Причем у многих таких больных долгое время сохраняются нормальными сократимость миокарда и фракция выброса левого желудочка (ФВ ЛЖ), а причиной декомпенсации могут быть нарушения диастолического наполнения сердца кровью. Причиной формирования правожелудочковой сердечной недостаточности, как правило, является хроническое легочное сердце, развивающееся вследствие легочной артериальной гипертензии, обусловленной патологией бронхолегочного аппарата, сосудов легких или торакодиафрагмальными нарушениями. Данное заболевание занимает третье место среди причин сердечнососудистой смерти, после инфаркта миокарда и артериальной гипертензии, а двухлетняя выживаемость больных при наличии развернутой клинической картины составляет не более 45 %.
Основным пусковым механизмом хронической сердечной недостаточности является снижение сократительной способности миокарда и вследствие этого — сердечного выброса. Это, в свою очередь, приводит к ухудшению кровоснабжения органов и тканей и включению ряда компенсаторных механизмов, одним из которых является гиперактивация симпатоадреналовой системы (САС). Катехоламины, в основном норадреналин, вызывают сужение артериол и венул, что обусловливает увеличение венозного возврата крови к сердцу, возрастание диастолического наполнения пораженного левого желудочка и выравнивание до нормы сниженного сердечного выброса. Однако активация САС, будучи изначально компенсаторной, в дальнейшем становится одним из факторов, обусловливающих прогрессирование патологических изменений в органах сердечнососудистой системы и усугубление признаков сердечной недостаточности. Спазм артериол, в частности почечных, вызывает активацию ренинангиотензиновой системы (РАС) и гиперпродукцию мощного вазопрессорного фактора — ангиотензина II. Кроме повышения содержания ангиотензина II в плазме крови, активируются местные тканевые РАС, в частности в миокарде, что обусловливает прогрессирование его гипертрофии. Ангиотензин II стимулирует также увеличенное образование альдостерона, что, в свою очередь, повышает реабсорбцию натрия, увеличивает осмолярность плазмы крови и, в конечном счете, способствует активации продукции антидиуретического гормона (АДГ) — вазопрессина. Повышение содержания АДГ и альдостерона приводит к прогрессирующей задержке в организме натрия и воды, увеличению массы циркулирующей крови, повышению венозного давления. Происходит дальнейшее увеличение венозного возврата крови к сердцу, в результате чего дилатация левого желудочка усугубляется. Ангиотензин II и альдостерон, действуя местно в миокарде, приводят к изменению пораженного отдела сердца — к так называемому ремоделированию. В миокарде происходит дальнейшая гибель миокардиоцитов и развивается фиброз, что еще больше снижает насосную функцию сердца. Сниженный сердечный выброс ведет к увеличению остаточного систолического объема и росту конечного диастолического давления в полости левого желудочка. Дилатация еще больше усиливается. Это явление поначалу, согласно механизму Франка — Старлинга, приводит к усилению сократительной функции миокарда и выравниванию сердечного выброса. Однако по мере прогрессирования дилатации механизм Франка — Старлинга перестает работать, в связи с чем возрастает давление в вышележащих отделах кровеносного русла — сосудах малого круга кровообращения.
Среди нейрогормональных нарушений при ХСН следует отметить увеличение содержания в крови эндотелина — мощного вазоконстрикторного фактора, секретируемого эндотелием.
Наряду с вазопрессорными факторами увеличивается содержание предсердного натрийуретического пептида (ПНП), секретируемого сердцем в кровяное русло, что связано с увеличением напряжения стенок предсердий, с повышением давления наполнения соответствующих камер сердца. ПНП расширяет артерии и способствует экскреции соли и воды. Однако при ХСН выраженность этого вазодилататорного эффекта ангиотензина II и катехоламинов и потенциально полезное влияние ПНП на функцию почек ослабевают. Таким образом, в патогенезе ХСН выделяют кардиальный и экстракардиальный механизмы. При этом пусковым фактором является кардиальный механизм — снижение сократительной функции сердца или нарушение наполнения сердца в период диастолы.
Основным звеном патогенеза хронического легочного сердца является уменьшение суммарного поперечного сечения сосудов легких вследствие спазма мелких легочных артерий в ответ на альвеолярную гипоксию. Это приводит к возрастанию общего легочного сосудистого сопротивления и давления в малом круге кровообращения. В этих условиях правые отделы отделы сердца, и в первую очередь правый желудочек, испытывают перегрузку давлением, а в дальнейшем, при развитии недостаточности трехстворчатого клапана, — и объемом. Как следствие, возникает гипертрофия и дилатация правых отделов сердца. С течением болезни может произойти срыв компенсации — развивается правожелудочковая сердечная недостаточность, которая является терминальной стадией данного состояния.
В настоящее время используется следующая классификация недостаточности кровообращения, предложенная Н.Д. Стражеско:
- I стадия (начальная) характеризуется скрытой недостаточностью кровообращения, которая проявляется одышкой, сердцебиением и утомляемостью только при физической нагрузке. В покое эти явления исчезают. Гемодинамика в покое не нарушена;
- II стадия, период А: признаки недостаточности кровообращения в покое выражены умеренно, толерантность к физической нагрузке снижена. Имеются нарушения гемодинамики в большом или малом круге кровообращения, выраженность их умеренная;
- период Б: выраженные признаки сердечной недостаточности в покое, тяжелые гемодинамические нарушения и в большом, и в малом круге кровообращения;
- III стадия (конечная) характеризуется дистрофическими изменениями с выраженными нарушениями гемодинамики, нарушением обмена веществ и необратимыми изменениями в структуре органов и тканей.
Для клинической картины ХСН свойственны следующие симптомы:
1. Одышка — самый частый симптом при ХСН, носит инспираторный характер. В начале она появляется только при физической нагрузке, затем становится постоянной, даже в покое, переходя в ортопноэ — высокую степень одышки с вынужденным положением больного. Встречается у 98,4 % пациентов с ХСН.
2. Могут быть приступы сердечной астмы — остро наступившее удушье у «сердечного» больного.
3. Кашель нередко сопровождает одышку у больных с хронической левожелудочковой недостаточностью, особенно по ночам: сухой, малопродуктивный, с отхождением слизистой мокроты.
4. Быстрая утомляемость является вторым после одышки (по чувствительности) симптомом сердечной недостаточности. Выявляется у 94,3 % пациентов, страдающих ХСН.
5. Сердцебиение — третий по частоте выявления симптом ХСН (80,4 %), который выражается в ощущении больным каждого сокращения своего сердца. Чаще ощущается при тахикардии, но может быть при нормальной частоте сердечных сокращений и даже брадикардии.
6. Отеки, обнаруживаемые больными с ХСН, свидетельствуют о том, что объем внеклеточной жидкости увеличен более чем на 5 литров. Отмечается выраженная зависимость отеков от положения тела: они распространяются снизу вверх. Отеки традиционно связывают с недостаточностью правого желудочка, но они могут быть и при снижении сократимости левого желудочка. Отеки, обусловленные преимущественно правожелудочковой недостаточностью и венозным застоем, обычно появляются позже, чем увеличивается печень, они обширны, плотны на ощупь, кожа под ними изменена, цианотична, с трофическими изменениями. Отеки при дисфункции левого желудочка возникают раньше, чем венозный стаз, невелики, мягки, смещаемы, расположены на удаленных от сердца участках тела, кожа под ними бледная.
7. Чувство тяжести или боль в правом подреберье у пациентов с правожелудочковой недостаточностью обычно предшествует появлению отеков, так как печень первой реагирует на недостаточность правой половины сердца. При прогрессировании ХСН, длительном застое появляются симптомы нарушения функции печени — иктеричность кожи и слизистых, возникает портальная гипертензия.
8. Тошнота, рвота, снижение аппетита, запоры, метеоризм и другие симптомы желудочной и кишечной диспепсии — почти постоянные спутники застойной сердечной недостаточности.
9. Снижение диуреза связано со значительным снижением почечного кровотока, рефлекторным спазмом почечных артериол и повышением давления в почечных венах. Моча выделяется преимущественно ночью, изза некоторого улучшения кровоснабжения почек в покое.
10. Жалобы на понижение умственной работоспособности и настроения, раздражительность, бессонницу ночью, сонливость днем.
К объективным признакам дисфункции сердца относятся данные обязательных инструментальных и лабораторных исследований. Электрокардиография (ЭКГ) — самый доступный инструментальный метод, позволяющий объективно оценить состояние сердца.При анализе ЭКГ следует обращать внимание на наличие признаков гипертрофии правых и левых отделов сердца, ишемических и рубцовых изменений в миокарде, возникновение нарушений в проводящей системе сердца и наличие аритмий. Необходимо проведение рентгенографии грудной клетки. При этом основное внимание при подозрении на ХСН следует уделять кардиомегалии и венозному легочному застою. Кардиомегалия — свидетельство вовлеченности сердца в патологический процесс. Наличие венозного застоя и его динамика могут быть использованы для характеристики тяжести заболевания и служить объективным критерием терапии. При лабораторных исследованиях общий анализ крови позволяет выявить компенсаторный эритроцитоз с повышением уровня гемоглобина. При определении гематокрита часто определяется увеличение гемоконцентрации. Также проводят электролитный анализ крови, определение креатинина в сыворотке и скорости клубочковой фильтрации, глюкозы в крови, печеночных ферментов и общий анализ мочи. Натрийуретические гормоны используют в качестве маркеров при диагностике сердечной недостаточности, а также для контроля за эффективностью лечения. Эхокардиография позволяет решить главную диагностическую задачу — уточнить сам факт дисфункции и ее характер, провести динамическую оценку состояния сердца и гемодинамики.
Согласно рекомендациям Европейского кардиологического общества (2008), в лечении больных с хронической сердечной недостаточностью следует применять ингибиторы АПФ, блокаторы бетаадренорецепторов, антагонисты рецепторов ангиотензина II, антагонисты альдостерона и периферические вазодилататоры. Однако при выборе терапии необходимо учитывать тот факт, что большинство больных, страдающих ХСН, пожилого возраста, а значит, побочные реакции при приеме лекарств возникают значительно чаще и протекают тяжелее. У пожилых пациентов значительно сложнее контролировать эффективность проводимой терапии изза полиморбидности, а также у них значительно ниже приверженность к терапии.
По данным регистра EuroHeart Failure Survey (Komajda M. et al., 2003), у пациентов с сердечной недостаточностью вазодилататоры используются более чем в 30 % случаев, то есть практически так же часто, как и блокаторы бетаадренорецепторов и сердечные гликозиды. Однако необходимость в их дополнительном применении возрастает пропорционально функциональному классу сердечной недостаточности. Более того, по данным исследования Acute Decompensated Heart Failure, раннее (в первые 6 часов после госпитализации) внутривенное применение вазодилататоров у пациентов с острой декомпенсированной сердечной недостаточностью позволяет достоверно снизить вероятность наступления смертельного исхода на протяжении 48 часов лечения по сравнению с поздним (после 6 часов госпитального периода) их назначением (Okraince K. et al., 2006).
Периферические вазодилататоры оказывают благоприятные гемодинамические эффекты при сердечной недостаточности: за счет венодилатирующего влияния уменьшают постнагрузку на сердце, увеличивают ударный объем, уменьшают степень первичной или вторичной дилатации. Но необходимо помнить, что нитраты у гериатрических больных часто вызывают головную боль, тошноту, снижение артериального давления с рефлекторной тахикардией. У таких пациентов достаточно быстро, в течение нескольких недель, возникает толерантность к нитратам, когда эффективность их снижается и не возрастает даже при увеличении разовой и суточной дозы. В связи с этим в качестве альтернативы рассматриваются производные сиднониминов, наиболее изученным представителем которых является молсидомин (Сиднофарм). Данный препарат обладает уникальной способностью к реализации вазодилатирующего потенциала за счет реверсии дисфункции эндотелия фактически при любом исходном уровне NO, а также при высокой активности супрессантов его синтеза.
Основной механизм антиангинального действия молсидомина (Сиднофарм) заключается в уменьшении преднагрузки на сердце и благоприятном влиянии на метаболизм миокарда, в результате чего его потребность в кислороде резко снижается. Молсидомин (Сиднофарм) снижает венозное давление, конечное диастолическое давление в желудочках и давление в легочной артерии, расширяет крупные коронарные артерии, а также улучшает коллатеральное кровообращение при атеросклерозе коронарных сосудов.
После приема внутрь молсидомин (Сиднофарм) метаболизируется в печени, превращаясь в фармакологически активное производное SIN1, из которого неэнзимным путем образуется нестойкое соединение SIN1А, содержащее свободную фармакологически активную группу NO и разлагающееся в крови и тканях до фармакологически неактивного SIN1С. Самопроизвольное отщепление NO в процессе этих превращений, аналогично действию нитратов, последовательно приводит к расслаблению гладких мышц сосудов и вазодилатации (Kmill M., Ochmanski W., 1998).
В то же время молекулярный механизм вазодилатирующего действия сиднониминов имеет немаловажное отличие от соответствующего механизма действия нитратов: отсутствие предварительного взаимодействия с SHгруппами для активации цГМФ. В связи с этой особенностью молсидомина (Сиднофарм) клинически значимая толерантность к нему не развивается.
У пациентов с ангиографическим подтверждением ИБС и сердечной недостаточностью во время продолжительной (в течение 4 недель) терапии молсидомином (Сиднофарм) в дозе 4 мг 3 раза в сутки per os при повышении работоспособности и лучшей переносимости физической нагрузки развития толерантности не выявлено (Jansen W. et al., 1987).
SIN1 сохраняет вазодилатирующую активность даже у пациентов с доказанной толерантностью к органическим нитратам, что является отражением протекторного влияния препарата в отношении сосудистого эндотелия. Его внутривенное или интракоронарное введение оказывает быстрый вазодилатирующий эффект, не сопровождающийся синдромом обкрадывания (Березин А.Е., 2010). Результаты повторной коронарографии в нескольких проекциях до и через 2 мин после внутрикоронарного введения SIN1 в дозе 1 мг, а также до и после второй инъекции через 60 мин показали увеличение среднего диаметра 44 нормальных сегментов левой коронарной артерии на 12 % непосредственно после введения SIN1 и на 8 % — спустя 60 минут (Serruys P.W. et al., 1987).
В рандомизированном двойном слепом плацебоконтролируемом исследовании применение у пациентов с ИБС молсидомина (Сиднофарм) в дозе 12 мг/сут в течение 48 часов увеличило на 60 % потокопосредованную дилатацию сосудов после первого приема препарата (Herman A.G., Moncada S., 2005).
Антитромбоцитарные свойства молсидомина (Сиднофарм) и его активного метаболита SIN1 изучены при применении per os у здоровых добровольцев и внутривенно у пациентов с инфарктом миокарда (Wautier J.L. et al., 1989), а также в сравнении с аналогичными свойствами изосорбида5мононитрата и плацебо. В отличие от изосорбида5мононитрата через 30 и 60 минут после применения молсидомина (Сиднофарм) отмечено значительное (на 100 и 120 % соответственно) повышение пороговых уровней фактора активации тромбоцитов, вызвавшее их необратимую агрегацию, и значительное снижение кривых агрегации, что очень важно при лечении сердечной недостаточности.
В ряде специально спланированных рандомизированных контролируемых исследований выявлен благоприятный гемодинамический и клинический эффект молсидомина (Сиднофарм) у пациентов с сердечной недостаточностью, развившейся вследствие ИБС, артериальной гипертензии, кардиомиопатии и хронической обструктивной болезни легких (Kmiec M., Ochmanski W., 1998). W. Rudolph, J. Sirshinger (1985) отмечали не только повышение фракции выброса левого желудочка, но и существенный регресс клинических симптомов заболевания, повышение переносимости физических нагрузок, улучшение качества жизни при вполне приемлемом профиле переносимости этого лекарственного средства.
У пациентов со сниженной ФВ левого желудочка добавление молсидомина (Сиднофарм) в дозе 6 мг/сут к стандартной терапии сопровождалось существенным достоверным возрастанием ФВ ЛЖ после 3 месяцев его приема (Spring A. еt al., 1998). По данным Н.М. Мухарлямова и В.Ю. Мареева (1985), на фоне лечения молсидомином (Сиднофарм) в разовых дозах 6–8 мг наблюдалось выраженное клиническое и гемодинамическое (объективизированное результатами эхокардиографии и катетеризации легочной артерии) улучшение у пациентов с тяжелой декомпенсированной хронической сердечной недостаточностью.
Клиническая эффективность адъювантного применения молсидомина (Сиднофарм) оценивалась у пациентов с легочной гипертензией. В испытании были отобраны пациенты с сердечной недостаточностью, развившейся вследствие документированной легочной артериальной гипертензии, отвечающие на ингаляционное введение синтетического простагландина или прием силденафила в рекомендованных дозах. Оказалось, что 24часовая внутривенная инфузия молсидомина (Сиднофарм) более эффективно способствует реверсии признаков сердечной недостаточности и уровня систолического давления в легочной артерии, чем изосорбид5мононитрат (Lehmann G. еt al., 1998).
Таким образом, Сиднофарм (молсидомин) сохраняет свои позиции как лекарственное средство, позволяющее эффективно контролировать симптомы сердечной недостаточности при проведении комбинированной терапии. Улучшение физического состояния на фоне терапии Сиднофармом (молсидомином) позволяет пациентам сохранять не только повседневную, но и во многих случаях профессиональную активность, если она не связана с тяжелым физическим трудом, а положительная динамика физического и психологического статуса способствует существенному улучшению качества жизни.
Подготовила Т. Чистик
Точки приложения сосудорасширяющих препаратов
Сосудорасширяющие препараты – группа довольно-таки разнородная, но, решая одну задачу (расширение кровеносных сосудов) каждое лекарство для достижения цели идет своим путем. Это значит, что для каждой подгруппы этих лекарственных веществ существуют свои точки приложения, тогда как к остальным они остаются «равнодушными», например:
- Одни заняты блокадой альфа- и бета-адренорецепторов;
- В компетенции других находится регуляция активности РААС (ренин-ангиотензин-альдостероновая система);
- Третьи – вообще относятся к антагонистам кальция, которые блокируют медленные кальциевые каналы и тем самым препятствуют току данного химического элемента внутрь клетки, чтобы его концентрация не достигла опасных для жизни цифровых значений;
- Четвертые – непосредственно расслабляют гладкую мускулатуру, воздействуя на клетки гладкомышечных волокон (имеются в виду миотропные спазмолитики, например, но-шпа, папаверин, которые применяются не столько для снижения АД, сколько для облегчения симптомов других болезней).
Вазодилататоры в лечебной практике широко применяются при лечении различных патологических состояний:
- При гипертонии;
- Ишемической болезни сердца;
- Хронической сердечной недостаточности:
- Заболеваниях, причиной которых стало нарушение периферического кровообращения;
- Болезнях головного мозга, связанных с уменьшением просвета мозговых сосудов в результате их сужения;
- Сахарном диабете и осложнениях этой патологии;
- Вегето-сосудистой дистонии;
- Артрозе;
- Болезнях органов зрения.
В этой связи, наверное, уместно было бы несколько разъяснить читателю суть перечисленных выше механизмов, ведь большинство пациентов, зная, что сосуды у них сужены и их нужно расширить, правильно называют группы препаратов (например, β-блокаторы, антагонисты кальция и т. д.), но при этом представления не имеют, что делает в их организме то или иное лекарственное средство и за счет чего достигается положительный результат или лечение не дает ожидаемого эффекта, если лекарство выбрано неправильно. Последующие разделы, возможно, будут интересны пациентам, которые более детально желают разобраться в механизмах действия вазодилататоров.
Механизмы действия сосудорасширяющих средств
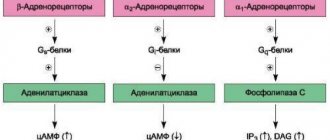
Блокада α- и β- адренорецепторов
Чрезмерное воздействие различных БАВ (биологически активных веществ), в частности, адреналина, вызывает изменение просвета кровеносных сосудов в сторону уменьшения, что проявляется, в первую очередь, повышением артериального давления. Для того, чтобы нивелировать негативный (сосудосуживающий) эффект этих веществ, больному назначаются лекарственные средства, обладающие способностью блокировать адренергические импульсы и, таким образом, нейтрализовать воздействие БАВ.
Адреноблокаторы представляют довольно обширную группу лекарственных средств, которая, однако, в зависимости от рецепторов, на которые они могут воздействовать и блокировать делится на 2 подгруппы: блокаторы α- и β- адренорецепторов. К первому списку препаратов (α-адреноблокаторы) отнесены:
- Теразозин;
- Силодозин;
- Альфузозин;
- Йохимбин;
- Ницероголин;
- Дигидроэрготоксин;
- Фентоламин;
- Пророксан.
Второй список препаратов, блокирующих адренорецепторы (бета), могут представлять лекарственные средства, которые легко узнать по окончанию «-олол»:
- Атенолол:
- Метопролол;
- Бисопролол;
- Эсмолол;
- Окспренолол;
- Метипранолол;
- Пропранолол.
Помимо этого, в группе β-блокаторов выделяют кардиоселективные (атенолол, метопролол, эсмолол) и неселективные – бета 1,2- адреноблокаторы (соталол, пропранолол, тимолол), группа альфа-блокаторов также разделяется на несколько подгрупп: α-1, α-2, α-1,2-адреноблокаторы.
Угнетение ангиотензинпревращающего фермента
Работа РААС расстраивается в результате многих патологических процессов, запускаемых при стимуляции выработки ренина в почках, нарушении продукции гормона альдостерона в надпочечниках, синтеза гликопротеида агиотензиногена в печени.
Поступающий в кровь ренин, вступает в реакцию а ангиотензиногеном, превращая его в ангиотензин I, который, в свою очередь, под воздействием фермента АПФ трансформируется в ангиотензин II – мощный сосудосуживающий компонент. Ангиотензин II, помимо этого, провоцирует спазм гладкомышечных волокон и своим присутствием нарушает адекватный синтез брадикинина, одновременно способствуя стимуляции продукции альдостерона, а это ведет к уменьшению внутреннего диаметра кровеносных сосудов, повышению артериального давления, нарушению кровообращения в микроциркуляторном русле.
Очевидно, что для предотвращения развития такой реакции и образования в ее результате ангиотензина II, необходимо подавление синтеза фермента АПФ. Данная роль была возложена на сосудорасширяющие препараты, названные ингибиторами ангиотензинпревращающего фермента или ингибиторами АПФ (иАПФ). Это – доступная, весьма популярная, и широко распространенная группа. Чаще всего иАПФ используются при гипертонии и прочих патологических состояниях сердечно-сосудистой системы.
пример действия иАПФ при хронической сердечной недостаточности
Список препаратов – ингибиторов АПФ довольно широк, где для пациентов, страдающих артериальной гипертензией, очень знакомы лекарственные средства, которые, подобно бета-блокаторам, также имеют свою отличительную частицу в конце слова («-прил»):
- Каптоприл;
- Эналапррил;
- Лизиноприл;
- Моноприл;
- Рамиприл;
- Аккуприл;
- Хинаприл.
Отдельные ингибиторы ангиотензинпревращающего фермента при гипертонии назначаются сразу в виде комбинированных (с диуретиками – энам Н, лизитон Н, капозид либо антагонистами кальция – экватор) средств.
Блокада отдельных (медленных) кальциевых каналов
схема перегрузки кардиомиоцитов ионами кальция
Оказывается, кальций, который так жизненно необходим мышечным волокнам для полноценного их функционирования, может не всегда быть полезен. Активное продвижение ионов этого химического элемента из межклеточного пространства по кальциевым каналам внутрь клетки и излишнее его сосредоточение в клетках способно перегрузить ткани, которые ответят чрезмерным напряжением. Таким образом, пострадать могут ткани, состоящие из гладкомышечных волокон, независимо от их места расположения (скелетная мускулатура, атриовентрикулярные пути, миофибриллы сердечной мышцы, кровеносные сосуды).
Не допустить проникновения ненужных клеткам количеств кальция (Са++) помогают медикаментозные препараты, встающие на пути движения ионизированной формы данного элемента. Они попросту блокируют медленные кальциевые каналы, расположенные в клетках гладкой мускулатуры, чем и предотвращают накопление Са++. Данные лекарства расслабляют гладкую мускулатуру (в том числе, кровеносных сосудов) и тем самым снижают артериальное давление, кроме этого, представители группы антагонистов кальция (так называют эти фармацевтические средства) регулируют сердечный ритм.
Очевидно, что подобные вещества в таких случаях берут на себя роль сосудорасширяющих препаратов. Среди часто назначаемых блокаторов медленных кальциевых каналов можно назвать:
- Нифедипин;
- Фелодипин;
- Лацидипин;
- Амлодипин;
- Верапамил;
- Дилтиазем.
Большинство антагонистов кальция также можно распознать по окончанию названий («-дипин»).
Рисунок: пример действия антагонистов кальция
в) Миотропные сосудорасширяющие средства
Вещества этой группы действуют непосредственно на гладкомышечные волокна кровеносных сосудов, вызывая их расслабление. Вследствие этого кровеносные сосуды расширяются; расширение артериальных сосудов ведет к снижению артериального давления. Миотропные сосудорасширяющие средства препятствуют сосудосуживающим влияниям как симпатической нервной системы, так и системы ренин — ангиотензин.
Апрессин
(гидралазин) расширяет преимущественно артериальные сосуды и мало влияет на тонус вен, поэтому при его применении не бывает ортостатической гипотензии. Снижение артериального давления при использовании апрессина сопровождается тахикардией и повышением секреции ренина. Поэтому препарат целесообразно комбинировать с веществами, снижающими влияния симпатической нервной системы (β-адреноблокаторы, резерпин). Апрессин назначают внутрь в таблетках; продолжительность действия 6-12 ч.
Побочные эффекты
: тошнота, головная боль, головокружение, кожные высыпания; в больших дозах препарат может вызывать синдром системной красной волчанки.
Диазоксид
(гиперстат) преимущественно расширяет артериальные сосуды. При попадании в кровь почти полностью связывается белками плазмы крови и в этом состоянии не проявляет активности. Препарат достаточно эффективен лишь при внутривенном введении, так как только в этом случае удается создать в крови достаточную концентрацию свободного, не связанного с белками плазмы крови препарата. Диазоксид является одним из лучших средств для купирования гипертензивных кризов. Продолжительность действия 3-12 ч.
Натрия нитропруссид
— одно из самых эффективных гипотензивных средств миотропного действия: расширяет как артериальные, так и венозные сосуды. Растворы препарата вводят внутривенно капельным способом (при однократной инъекции длительность действия препарата 2-5 мин). Натрия нитропруссид применяют для купирования гипертензивных кризов и для управляемой гипотензии.
Магния сульфат
снижает артериальное давление лишь при парентеральном (внутримышечном, внутривенном) введении. При назначении внутрь гипотензивный эффект обычно не развивается, так как препарат плохо всасывается в желудочно-кишечном тракте.
Механизм гипотензивного действия магния сульфата сложен. В основном сосудорасширяющее действие препарата связано с его миотропными спазмолитическими свойствами. Кроме того, препарат обладает слабым ганглиоблокирующим действием и способностью угнетать сосудодвигательный центр. Последнее свойство магния сульфата связано с его наркотической активностью.
Используют магния сульфат чаще всего при гипертензивных кризах и при нефропатии (поздний токсикоз беременных, сопровождающийся повышением артериального давления) для быстрого снижения артериального давления.
В качестве гипотензивного средства растворы магния сульфата чаще всего вводят внутримышечно.
При неэффективности внутримышечных инъекций магния сульфата прибегают к его внутривенному введению, которое, однако, следует проводить крайне осторожно. При внутривенном введении особенно отчетливо проявляются наркотические свойства магния сульфата, а так как наркотическая широта препарата невелика, в этом случае легко наступает угнетение дыхания.
При первых признаках угнетения дыхания введение препарата следует прекратить и ввести внутривенно антагонист магния сульфата — кальция хлорид или кальция глюконат.
Дибазол
применяют чаще всего для лечения гипертензивных кризов. В этих случаях препарат вводят внутривенно. При назначении внутрь дибазол малоэффективен.
Новое на atreya-ayurveda.ru аюрведическая клиника на ул осенняя дом 16
Высокая популярность сосудорасширяющих средств в народе
Высокая популярность сосудорасширяющих препаратов объясняется их широким применением при очень многих патологических состояниях, однако не все пациенты спешат принимать полученные синтетическим путем лекарства, ведь средства, умеющие расширять сосуды и улучшать кровоснабжение, можно извлечь из природных источников.
Вещества, способные позитивно воздействовать на кровеносные сосуды человека, несут многие представители растительного мира. Некоторые из них становятся основой для получения лекарств, реализуемых аптечной сетью (например, гинкго билоба), другие – можно собрать самостоятельно и приготовить лечебный продукт в домашних условиях. Из таких растений, как шлемник байкальский, боярышник (цветки и ягоды), петрушка (семена), базилик, душица, знающие люди готовят настои, отвары, выжимают масла. Но это может быть вспомогательное лечение или помощь на первых этапах болезни.
Видео: обзор народных сосудорасширяющих средств
В иных случаях придется прибегнуть к лекарствам, выпущенным фармацевтической промышленностью и здесь хочется предостеречь пациентов: только врач знает, какие синтетические сосудорасширяющие препараты помогут человеку относительно безболезненно переносить течение хронических процессов, то есть, самолечение будет неуместным.