Фиброзное кольцо – это внешняя оболочек межпозвоночного диска, отвечающая в принципе за его целостность. Состоит из плотных хрящевых волокон, способных быстро адаптироваться к любым амортизационным нагрузкам. Очень эластичное и выносливое. При развитии остеохондроза в первую очередь патологические изменения затрагивают фиброзное кольцо – оно начинает растрескиваться, покрываться отложениями солей кальция, утрачивает способность получать достаточное количество жидкости и питательных веществ при диффузном обмене с окружающими паравертебральным мышцами.
В результате этого возникают различные повреждения фиброзного кольца, большую часть из которых рассмотрим в предлагаемом материале. Здесь рассказано о том, как устроено фиброзное кольцо и какие основные функции оно выполняет. Даны сведения о потенциальных причинах разрушения его тканей. Рассказано про характерные клинические симптомы, при появлении которых следует незамедлительно обратиться к врачу для проведения обследования и дифференциальной диагностики. В статье вы узнаете о современных эффективных методах восстановления целостности хрящевой ткани фиброзного кольца.
Если у вас есть симптомы и признаки, которые описаны в материале, то рекомендуем вам как можно быстрее обратиться на прием к неврологу или вертебрологу. Эти доктора обладают достаточной компетенцией для того, чтобы проводить эффективное и безопасное лечение дегенеративных дистрофических изменений в межпозвонковых дисках.
В Москве можно записаться на бесплатную консультацию к вертебрологу или неврологу в нашей клинике мануальной терапии. Прием ведут опытные доктора. Они устанавливают предварительный диагноз, по мере необходимости назначают дополнительные обследования. Дают индивидуальные рекомендации по проведению лечения и изменению образа жизни таким образом, чтобы позвоночный столб вновь обрел утраченное здоровье.
Записаться на бесплатный прием можно с помощью специальной формы, которая располагается в конце этой страницы. Также вы можете позвонить нашему администратору и согласовать удобное для визита время.
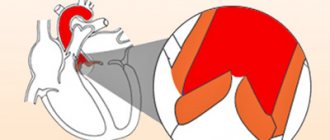
Особенности проявления фиброза сердечных клапанов
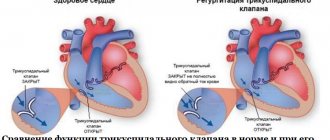
Усугубление состояния происходит не сразу. Выявить уплотнение стенки клапана по клинической картине сбоя в гемодинамике удается лишь при развитии выраженной регургитации. Для нее характерен обратный ток крови. Она возвращается в предсердие или желудочек в зависимости от пораженного клапана. Суть проблемы заключается в неполном смыкании створок. Иногда все происходит наоборот. Фиброз приводит к сращиванию створок между собой. В первом случае патологический процесс провоцирует увеличение предсердия, а во втором – сужение отверстия клапана.
Степень регургитации бывает легкой и тяжелой. Клиническая картина будет зависеть от выраженности патологии.
Поражение митрального клапана
Если уплотнены створки митрального клапана, то у больного со временем могут проявиться следующие симптомы фиброза:
- быстрая утомляемость;
- частая одышка;
- ощущение сердцебиения;
- аритмия;
- чувство нехватка воздуха;
- боли в области сердца;
- отеки ног.
Поражение аортального клапана
Фиброз аортального клапана способствует проявлению гипоксии головного мозга. У больного проявляется патологический процесс следующими симптомами:
- общая слабость;
- отек легких;
- потеря сознания;
- стенокардия.
Классификация фиброза
Каждая форма патологии имеет свои особенности.
- Очаговая форма является базовой. Для нее характерно умеренное фрагментарное поражение структуры клапанного аппарата.
- Диффузному виду свойственна большая площадь поражения (створок и подклапанного пространства). Выявляют его на запущенных стадиях развития фиброза.
- Кистозная форма воспринимается в роли отдельной патологии. Она проявляется серьезными сбоями в обменных процессах и ведет к образованию кист.
Если у митрального клапана створки уплотнены, то вовсе не обязательно, что это порок сердца. Фиброз является лишь патологическим изменением, происходящим под влиянием прочих факторов, а не диагнозом. Из-за него может развиться стеноз и клапанная недостаточность. Появление озвученных патологий требует срочного вмешательства врача. Воспринимать разрастание фиброзных тканей можно в роле субстрата для формирования порока сердечной мышцы. Однако заранее предположить его развитие маловероятно. Повышаются шансы на своевременное выявление проблемы за счет регулярного обследования.
Уплотнение, кальциноз и трещина фиброзного кольца
На начальном этапе развития остеохондроза происходит постепенное уплотнение фиброзного кольца – этот процесс опытному вертебрологу говорит о том, что хрящевые ткани не получают в достаточном количестве жидкость. Уплотнение фиброзного кольца не дает никаких клинических симптомов и может обнаруживаться случайным образом при проведении обследований позвоночного столба с помощью МРТ.
Трещина фиброзного кольца – это следующая стадия остеохондроза. Если жидкости поступает мало, то уплотненная хрящевая ткань не может в полной мере справляться с оказываемыми на неё амортизационными нагрузками. Она утрачивает свою эластичность и пластичность. Появляются сеточка из мелких трещин, которые не нарушают полностью целостности фиброзного кольца.
На фоне нарушенного диффузного питания единственной возможностью восстановлять целостность потрескавшейся поверхности межпозвоночной диска организм видит оседание солей кальция. Вторичный кальциноз фиброзного кольца – это серьезная патология, которая значительно сокращает способность хрящевых тканей усваивать жидкость, выделяемую замыкательной пластинкой и паравертебральным мышцами. При его развитии остеохондроз начинает стремительно разрушать межпозвоночный диск.
Что это такое?
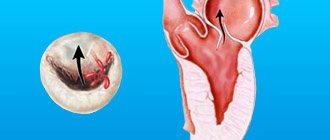
Понять, что такое фиброз створок митрального клапана, можно, взглянув на особенности его строения и функционирования. Суть работы клапанного аппарата заключается в пропускании крови (в одну сторону) при сокращении определенного отдела. Основную роль выполняют створки, которые представлены рыхлой соединительной тканью. Их питание осуществляется за счет мельчайших сосудов. У аортального клапана три створки (правая, левая, задняя), а у митрального их две (задняя, передняя).
Под влиянием раздражающих факторов соединительная ткань становится более грубой, из-за чего перестает полноценно выполнять свои функции (сохранять гибкость створок). Со временем значительно сокращается число кровеносных сосудов, питающих клапан. Клетки, из которых он состоит, начинают умирать, замещаясь на фиброзную ткань. Она представляет собой одну из разновидностей соединительных тканей, которой характерна высокая прочность.
Протрузия фиброзных колец
По своей сути протрузия фиброзных колец – это вторая стадия течения остеохондроза. Дегенеративные дистрофические изменения в межпозвоночных дисках выходят на следующий уровень. Фиброзное кольцо, не в состоянии усваивать жидкость извне, начинает забирать влагу из структуры пульпозного ядра. Оно быстро уменьшается в объеме и уже не может обеспечивать поддержку нормальной высоты диска.
При этом происходит увеличение занимаемой диском площади. Он начинает выходить за пределы тел позвонков, которые он разделяет между собой. Так начинает оказываться раздражающее давление на окружающие мягкие ткани. Появляется стойкий болевой синдром, который с трудом купируется нестероидными противовоспалительными средствами.
Протрузия с разрывом фиброзного кольца называется экструзией. Если в процессе нарушения целостности фиброзного кольца выпала часть пульпозного ядра, то это грыжа диска. Экструзия – это третья стадия течения остеохондроза.
Фиброз створок митрального клапана
Фиброз створок митрального клапана сердца – довольно опасное и тяжелое состояние. Причины его возникновения очень разнообразны. Стоит рассмотреть их поподробнее.
Причины
Довольно часто данное заболевание появляется после того, как больной перенес инфаркт миокарда. Распространенной причиной являются и возрастные изменения организма человека. С годами изнашиваются ткани, органы. Ткани сердца, МК могут быть повреждены из-за гормональных изменений, стремительного замедления обмена веществ и т. д.
- Жизнь против течения. Пролапс митрального клапана и что за ним стоит
Фиброз митрального клапана может быть вызван и следующими причинами:
- Гипертония.
- Нарушения в работе легких.
- Пороки сердца.
- Инфекционное или вирусное заражение соединительных тканей сердца.
- Сильные физические нагрузки и т. д.
Данное заболевание при отсутствии своевременного вмешательства специалистов может перерасти в фиброз миокарда. Иначе он называется миокардиофиброз.
«Старческий» порок сердца: истина и мифы
Что скрывается за диагнозом «атеросклеротический стеноз устья аорты»? Каков механизм развития аортального стеноза? Есть ли разница в лечебной тактике в России и за рубежом?
| Рисунок 1 |
Многим терапевтам и кардиологам хорошо известен такой нередко встречающийся клинический феномен: у пожилого человека без ревматического анамнеза при выслушивании сердца определяется грубый систолический шум над аортальными точками. Зачастую его практически никак не трактуют и в диагнозе не отражают. Но иногда в попытке объяснить подобную аускультативную картину врач все же выносит примерно такой вердикт: «атеросклеротический стеноз устья аорты». Но нельзя забывать, что диагноз — это формула для лечения, и от того, насколько правильно он будет сформулирован, во многом зависит дальнейшая тактика. Это касается любого диагноза, и данного — в частности. Именно поэтому следует серьезно разобраться не только и не столько в правомочности термина «атеросклеротический стеноз», сколько в том, что же в действительности скрывает за собой «неревматический» систолический шум на основании сердца.
В СССР традиционно рассматривались три основные причины приобретенного аортального стеноза: 1) ревматизм, 2) инфекционный эндокардит и 3) атеросклероз. Именно эта триада, и, как правило, именно в таком порядке перекочевывала из руководства в руководство, из одного учебника в другой до середины настоящего десятилетия, тогда как другим предпосылкам отводилось место в графе «и прочие». Большинство авторов после описания ревматического и «септического» эндокардитов в той или иной форме упоминают атеросклероз, который обычно в преклонном возрасте может привести к формированию кальцинированного стеноза аортального клапана [1].
Между тем за рубежом уже более 30 лет придерживаются иной точки зрения. Она последовательно рассматривается в англоязычных источниках, вышедших в свет в 60-е, 70-е и 80-е годы, и последнее десятилетие исключением не является. Согласно мнению западных исследователей, аортальный стеноз у взрослых может быть результатом: 1) кальцификации и дистрофических изменений нормального клапана, 2) кальцификации и фиброза врожденного двустворчатого аортального клапана или 3) ревматического поражения клапана, причем первая ситуация является наиболее частой причиной аортального стеноза [2].
Итак, налицо очевидная разница в подходах к этой проблеме в России и за рубежом. «Точкой пересечения» был и остается лишь ревматизм, тогда как отечественная и зарубежная школы «дополняют» его каждая двумя разными этиологическими формами: первая — инфекционным эндокардитом и атеросклерозом, вторая — идиопатическим кальцинозом и кальцификацией врожденного порока (чаще двустворчатого клапана). Но следует учитывать, что существуют две оговорки. Во-первых, изолированный кальциноз как трикуспидального, так и бикуспидального аортального клапана — по сути есть один и тот же процесс, наблюдающийся лишь в разных временных диапазонах. Во-вторых, инфекционный эндокардит работами современных авторов фактически исключен из списка существенных причин аортального стеноза. Таким образом, по большому счету остаются два состояния, определяющие диагностические, лечебные и методологические разночтения: атеросклероз и идиопатический кальциноз. Принципиальная разница между этими двумя патологическими состояниями станет понятна после более детального рассмотрения сенильного кальциноза устья аорты как самостоятельной нозологической формы.
- Морфологические аспекты
В 1904 году в журнале «Архив патологической анатомии» 28-летний немецкий врач Иоганн Георг Менкеберг описал два случая стеноза устья аорты со значительным обызвествлением клапанов [3]. Он предложил рассматривать изменения в створках как дегенеративные, как результат изнашивания тканей с последующим их «склерозом» и обызвествлением. Обнаружив, по-видимому, что-то подобное тому, что изображено на рис. 1, он изобразил в своей статье деформированный клапан, в котором на фоне жировой дегенерации расположено множество известковых депозитов (рис. 2). Его правота будет подтверждена спустя много лет, что найдет отражение в самом термине «дегенеративный кальцинированный аортальный стеноз». Но в начале века статья И. Г. Менкеберга существенного резонанса не вызвала. И лишь через полтора десятка лет она станет объектом внимания и ляжет в основу жарких дискуссий, ведущихся на протяжении долгого времени. Морфогенез порока также вызвал много споров.
| Рисунок 2 |
С менкеберговской гипотезой конкурировали в основном две теории: атеросклеротического поражения и поствоспалительного кальцинирования.
В нашей стране основное значение приобрела атеросклеротическая гипотеза. Считается, что детальное изучение «атеросклероза аортального клапана» в динамике развития «атеросклеротического порока» было выполнено профессором А. В. Вальтером в конце 40-х годов. Он описывал интенсивную липоидную инфильтрацию фиброзного пласта клапана на уровне замыкательной линии и на дне синусов Вальсальвы, причем отложение липоидов он наблюдал также на синусовой поверхности створок в небольших утолщениях субэндотелиального слоя. Далее имела место петрификация липоматозных очагов. Известковые массы раскалываются, что исследователь объяснял подвижностью створок, а образовавшиеся трещины заполняются плазменными белками и новыми порциями липоидов, в которых снова откладывается кальций. Раскалывание петрификатов продолжается, а вслед за этим продолжается и кальцинирование клапана. Фиброзное кольцо становится ригидным, створки твердыми и малоподвижными. Развивается аортальный стеноз [4].
Думается, в 1948 году опубликования этих данных было достаточно для обоснования атеросклеротической гипотезы, хотя критического осмысления требует даже сама идея «раскалывания» петрифицированных масс: если бы оно имело место, вероятно, в значительной степени возросла бы частота микроэмболических осложнений. Сегодня же, когда знания об атерогенезе куда более обширны, представляется возможным выдвинуть минимум два контраргумента теории А. В. Вальтера.
- Теперь известно, что основным анатомическим субстратом, для метаболизма которого требуются липоиды, является миоцит. Именно гладкомышечные клетки утилизируют вещества, транспортируемые в артериальную стенку липопротеидами плазмы. Преимущественное же поражение атеросклерозом внутреннего, а не среднего слоя сосудистой стенки объясняется тем, что в норме в преклонном возрасте происходит утолщение интимы за счет перемещения в нее гладких миоцитов из медии с последующей пролиферацией. Другими словами, своей инфильтрацией холестероловыми эфирами интима во многом обязана гладкомышечным клеткам. Так вот именно их-то в створках аортальных клапанов практически нет. На это указывают современные гистологи [5], об этом упоминалось в 1904 году еще самим Менкебергом.
- Согласно бытующей сейчас теории, атероморфогенез включает в себя три стадии: жировые полоски или пятна, фиброзные бляшки и, наконец, осложненные поражения, к числу которых и относится кальцификация фиброзной бляшки. То есть стадии кальциноза при атеросклерозе должен предшествовать этап, когда под объективом оказывается внеклеточный холестерин вперемешку с детритом, покрытый особым козырьком из большого количества гладких миоцитов, макрофагов и коллагена. Профессор А. В. Вальтер ничего подобного не описывал. И не случайно. В 1994 году, то есть почти через 50 лет после выхода работы Вальтера, В. Н. Шестаков так описывает морфогенез этого порока: «Начальной фазой этого процесса является липоидная инфильтрация обращенных к синусам Вальсальвы поверхностей клапанов. В очагах липоидоза начинается отложение солей кальция. Процесс этот медленно прогрессирует, приводя к ограничению подвижности створок» [6]. Как видно, эти наблюдения в основе своей схожи, и в обоих отсутствует стадия фиброзной бляшки. Кроме того, как давно доказано американскими учеными, при обсуждаемой нами патологии, в отличие от атеросклеротического повреждения, отсутствуют кристаллы холестерина [7]. Насколько можно судить по англоязычной периодике, не прослеживается также и корреляции между кальцинированным аортальным стенозом и степенью выраженности общего атеросклеротического поражения, в том числе и самой аорты у данного пациента.
Черту под этими рассуждениями можно подвести выдержкой из статьи об атеросклерозе профессора Вашингтонского университета Э. Бирмана: «С атеросклерозом не следует путать <…> локальное кальцифицирующее поражение клапана аорты, когда с возрастом происходит постепенное накопление кальция на аортальной поверхности клапана» [8].
Поствоспалительная гипотеза, распространенная в основном на Западе, предлагала искать связь кальцинирования с перенесенным когда-то инфекционным эндокардитом, или, что еще более вероятно, латентным ревмокардитом. Так, одни исследователи указывают на наличие в кальциевых конгломератах микробных агентов [9]. Другие публикуют сообщение о результатах гистологического исследования 200 обызвествленных аортальных клапанов, в 196 из которых обнаружены признаки ревматического поражения [10]. Сейчас сложно дать объективную оценку таким данным, но, вероятно, это были секционные находки у людей не столь пожилых и без выраженных известковых отложений. Именно к таким выводам приходишь, изучая мнение современных патологов, утверждающих, что у старых пациентов массивность петрификации всегда маскирует признаки, быть может, когда-то перенесенного ревматического эндокардита.
Однако наметившийся в первой половине века подход привел к формированию двух бытующих теперь за рубежом взглядов. Один из них предполагает, что ревматический вальвулит, даже не оставив стойких гранулематозных повреждений, делает клапан более ранимым в будущем, в значительной степени повышая риск структурной дегенерации [11] и позволяя рассматривать сенильный аортальный стеноз действительно как «дегенеративный», тогда как имеет место поствоспалительная дистрофия, постревматическая дегенерация; при этом перенесенное воспаление как бы детерминирует соединительнотканную деструктуризацию створок в пожилом и старческом возрасте, оказываясь своего рода предиктором кальцинирования клапанного аппарата аорты. Согласно другому взгляду, старческий кальцинированный стеноз является не столько результатом инфекционного эндокардита, сколько сам по себе может вызываться персистирующим в аортальных створках инфекционным возбудителем [12], то есть речь вообще идет о совершенно самостоятельной нозологической форме.
О своеобразности разбираемой патологии свидетельствует также и то, что все чаще появляются публикации об обнаружении в обызвествленных створках аортального клапана различных клеток костной ткани и даже элементов красного костного мозга [13].
- Клинические аспекты
Напоминание хорошо известных признаков аортального стеноза врачебной аудитории в данном случае не случайно. Дело в том, что у пожилых и старых пациентов доктора зачастую склонны объяснять наличие тех или иных жалоб скорее ишемической болезнью или общими инволютивными процессами в организме, нежели сформировавшимся «старческим» пороком сердца. Поэтому — коротко об основных особенностях этого заболевания.
| Рисунок 3 |
Аортальный стеноз — один из самых длительно компенсируемых пороков из-за гипертрофии миокарда, столь сильно выраженной, как можно встретить при других заболеваниях сердца (рис. 3). В связи с этим значительно возрастает конечное диастолическое давление в левом желудочке, его наполнение (особенно при физической нагрузке и в условиях тахикардии) затрудняется, что постепенно приводит к повышению давления заклинивания легочной артерии. Развивающаяся при этом одышка, таким образом, на первых порах оказывается следствием первичной диастолической дисфункции левого желудочка, а в период декомпенсации — и систолической дисфункции. С повышенным тонусом миокарда в диастолу связано и нарушение его оксигенации. В то время как увеличение массы левого желудочка усиливает потребность миокарда в кислороде, сдавленные коронарные артерии удовлетворить ее не могут. Отсюда столь типичные для этой категории больных стенокардические боли. При этом, хотя стенокардия возникает у 70% больных с аортальным стенозом, лишь у половины из них имеется коронарный атеросклероз [2]. Третья частая жалоба — обмороки — является следствием снижения сердечного выброса, развивающегося в результате, с одной стороны, уменьшения диастолического наполнения желудочка, с другой — возрастающего градиента давления на уровне аортального клапана [14]. Эквивалентами синкопального состояния могут служить головокружения.
Среди осложнений сенильного стеноза следует отметить эмболии крошащимися известковыми массами (чаще всего коронарных, почечных и церебральных артерий), плохо переносимые и прогностически неблагоприятные аритмии (связанные как с ишемической миокардиопатией, так и с увеличением и дисфункцией левого предсердия) и изредка развивающиеся желудочно-кишечные кровотечения, связанные с ангиодисплазией правых отделов толстой кишки. При этом риск инфекционного эндокардита кальцинированных клапанов снижается в сравнении с изолированными аортальными стенозами ревматической этиологии.
При осмотре редко можно обнаружить что-то специфическое для дегенеративного стеноза у пожилых больных. В отличие от молодых пациентов, имеющих нередко «медленный и малый» пульс, у них даже при тяжелом стенозе в силу снижения эластичности артерий пульс может оставаться нормальным. Пальпаторно длительный приподнимающийся верхушечный толчок определяется в V межреберье несколько кнаружи от среднеключичной линии; нередко может пальпироваться систолическое дрожание. При аускультации первый тон может не изменяться, но в силу функционально-гемодинамических изменений нередко наблюдается его
| Рисунок 4 |
ослабление. При этом второй тон, как правило, меняется, что особенно отчетливо фиксируется при длительном наблюдении за пациентом: пока кальциноз клапана не привел к стенозу, второй тон усилен (при этом в точке Боткина вслед за первым тоном иногда выслушивается систолический тон изгнания), затем из-за уменьшения подвижности створок ослаблен. Для аортального стеноза характерен грубый веретенообразный систолический шум, максимально выслушивающийся у левого края грудины и проводящийся на сонные артерии. При сенильном поражении этот шум имеет некоторые патогенетические особенности (рис. 4). Как видно из схемы, ревматический кальцинированный порок создает при систолическом изгнании гемодинамический эффект «струи», рождающий одни аускультативные феномены, а изолированный кальцинированный стеноз — эффект «спрея» с несколько другими гемодинамикой и нюансами выслушиваемой картины [15]. Так, при выраженной петрификации возникает симптом Галлавардена: высокочастотные компоненты шума проводятся в подмышечную область, имитируя шум митральной регургитации.
В диагностике клиницисту помогут рутинные инструментальные методики: ЭКГ (признаки гипертрофии и нарушения кровоснабжения миокарда левого желудочка, аритмии), рентгенография (кальциноз аортального клапана, изменение конфигурации сердца, признаки застоя в легких) и, конечно, ЭхоКГ (характер изменений в створках клапана, точная оценка степени стеноза и гипертрофии миокарда, измерение показаний внутрисердечной гемодинамики, нарушение локальной сократимости, фракция выброса, градиент давления между аортой и левым желудочком).
Лабораторные показатели, как правило, малоспецифичны и отражают экстракардиальную патологию.
- Лечебная тактика
Прогноз при изолированном дегенеративном аортальном стенозе определяется степенью сужения отверстия аортального клапана (см. табл.), но в целом, как правило, благоприятен. Это определяется длительной компенсацией с бессимптомным течением и медленной прогрессией из-за отсутствия комиссуральных сращений, как при ревматическом пороке. При этом следует помнить, что при появлении симптомов летальность и риск осложнений резко возрастает, а 15-20% больных умирают внезапно.
В России изучения этой нозологии как таковой не проводилось, а значит, практикующий врач не ориентирован на соответствующий диагностический поиск. При этом довольно редкое установление диагноза «атеросклеротический стеноз устья аорты» из-за непонимания истинной природы порока приводит к тому, что больному чаще назначают диету и холестеролснижающие средства, нежели направляют на консультацию к кардиохирургу. Но подобное «патогенетическое лечение» приводит лишь к прогрессированию петрифицированного стеноза. Консервативная же симптоматическая тактика вообще у больных аортальным стенозом малоэффективна, а кальцинированным — тем более. Вазодилатирующая и инотропная терапия требует большой осторожности, а назначения нитратов и диуретиков следует избегать.
Скорость прогрессирования стеноза устья аорты
|
| * Печатается по руководству «Кардиология в таблицах и схемах», М. — Практика, 1996, с. 343 |
Другими словами, отказ от трактовки сенильного кальцинированного стеноза устья аорты как «атеросклеротического» подведет российских кардиологов и терапевтов к формированию совершенно определенного взгляда на лечебные перспективы у таких пациентов. Единственно эффективным во всем мире признано хирургическое лечение либо путем протезирования аортального клапана (метод с наилучшими показателями отдаленной выживаемости), либо путем баллонной вальвулопластики. Второй метод имеет целый ряд существенных недостатков: большой риск осложнений и вероятность повторной обструкции, высокая интраоперационная летальность (>6%) и смертность в течение года (25%). Между тем именно этот вариант вмешательства остается основным у пожилых пациентов за рубежом; и вообще дегенеративный кальциноз стал основной причиной хирургического лечения при изолированном аортальном стенозе (51% случаев чрескожной баллонной вальвулопластики, тогда как кальциноз бикуспидального клапана и постревматическое поражение — соответственно 40 и 8% случаев). Причем возраст прооперированных больных нередко превышает 80 лет [16].
При написании последнего параграфа автор, разумеется, отдавал себе отчет в том, что проецировать зарубежную ситуацию на российскую действительность невозможно. Нередкая соматическая «запущенность» наших пациентов и стоимость кардиохирургической операции в ближайшее время не позволяют надеяться на какие-то кардинальные изменения в этом вопросе. Настоящая статья лишь подняла геронтологическую проблему, к обсуждению которой в нашей стране не обращались уже многие годы. И дело не столько в том, что 1999 год объявлен «годом пожилого человека» — отечественные медики должны располагать современной информацией и отказаться от устаревших формулировок и несуществующих диагнозов.
Литература
1. Бураковский В. И., Бокерия Л. А. Сердечно-сосудистая хирургия. М.: Медицина, 1989. 2. Goldstein J. A. Aortic stenosis // Essentials of Cardiovascular Medicine / Ed. M.Freed and C.Grines. Birmingham, 1994. 3. Monckeberg, J. G. Der normale histologische Bau und die Sklerose Aortenklappen // Virchows Archiv fur pathologische Anatomie und Physiology und fur Klinische Medizin, (1904). 176, 472. 4. Вальтер А. В. Хронические пороки аортальных клапанов. Л., ВММА, 1948, с. 23-88. 5. Ham A. W., Cormack D. H. Histology / J.B. Lippincott Company, N.Y. 1979. 6. Шестаков В. Н. Стеноз устья аорты. Внутренние болезни. Под ред. Б .И. Шулутко. С.-Пб, 1994, с. 66. 7. Edwards J. E. Calcific aortic stenosis / Circulation, 1962, 26, 817. 8. Bierman E. L. Atherosclerosis and other forms of arteriosclerosis // Harrison’s Principles of Internal Medicine. Hill Book Company, 1987, p. 235. 9. Friedberg C. K., Sohval A. R. Non-rheumatic calcific aortic stenosis // Am. Heart J. 1939 vol. 17 p. 452. 10. Karsner H. T., Koletsky S. Calcific Disease of the Aortic Valve. J. P. Lippincott, Philadelphia. 1947. 11. Hultgren H. N. Calcific disease of the aortic valve // Arch. Path., 1948, vol. 45, p. 694. 12. Poller D.N., Curry A. et al. Bacterial calcification in infective endocarditis // Postgrad. Med. J., 1989, vol. 65. № 767, p. 665. 13. Fernandez A. L., Montero J. A. Osseous Metaplasia and Hematopoietic Bone Marrow in a Calcified Aortic Valve // Tex. Heart Inst. J., 1997, 24/3, p. 232. 14. Braunwald E. Valvular heart disease / Heart Disease. Ed. by E. Braunwald — W. B. Saunders Company, 1988, p. 1023. 15. Roberts W. C., Perloff J. K. Severe Valvular Aortic Stenosis in Patients Over 65 Years of Age // Am. J. Card., 1971, vol. 27, p. 497-506. 16. Logeais Y., Leguerrier A., Rioux C. et al. // International Symposium on Surgery for Heart Valve Disease. Londres, 1989.