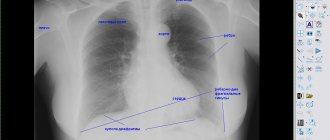
Информация для пациентов
- КЛЕТОЧНАЯ ТРАНСПЛАНТАЦИЯ: реальные достижения и возможности клинического применения
- Выбор протеза в российских условиях
- Операция аортокоронарного шунтирования без искусственного кровообращения — что следует учитывать при выборе клиники для ее выполнения?
- «Плетью обуха… перешибёшь!», или правда об аортокоронарном шунтировании и стентировании
- Задержки в выписке рецептов на клопидогрель пациентам после выполненного стентирования являются частой и смертельно опасной проблемой
Традиционным видом хирургического лечения пораженных клапанов сердца у нас в стране и за рубежом является замена их различными протезами.
На раннем этапе развития кардиохирургии врачи пытались применять в качестве заместительного материала клапанные устройства, основанные на биологических тканях ксеногенного (т.е. заимствованного у животных) или аллогенного (гомогенного) (т.е. заимствованного у человека) происхождения. Главным недостатком этих устройств явился ограниченный срок службы клапана в связи с постепенным разрушительным воздействием на биоткани со стороны организма реципиента. Так как в те годы (60-70 г.г.) любая операция на сердце воспринималась как тяжелейшее испытание для пациента (да и для хирурга), первостепенной задачей являлась разработка такого типа протеза, имплантация которого была бы окончательной в хирургическом лечении клапанного порока. Биопротезы явно не соответствовали этому условию. Начался поиск материалов и моделей для создания синтетических, механических протезов. Создано более нескольких десятков моделей, из которых только два конструктивных типа имеют современное всемирное признание и распространение: протез с одним откидным округлым диском (рис.1) и протез с двумя створками в форме полукруга (рис.2-1, рис.2-2).
| Рис.1 Отечественный однодисковый протез «ЛИКС-2» | Рис.2-1 Отечественный двустворчатый протез «Карбоникс-1» | Рис.2-2 Двустворчатый протез фирмы Sulzer Carbomedics (США) |
Имплантация механических протезов с самого раннего этапа сопровождалась частыми случаями развития нарушений мозгового кровообращения с глубокой инвалидизацией пациентов или их смертью, в связи с чем было выработано главное условие жизни больного с механическим протезом – прием препаратов, нарушающих процесс свертывания крови за счет снижения выработки белков коагуляции в печени. Целенаправленное избирательное подавление функции печени с этой целью достигалось назначением больному специфических веществ – производных кумарина. Лечение производными кумарина относится к так называемой антикоагулянтной терапии, а сами вещества названы непрямыми антикоагулянтами. Несколько десятилетий применения механических протезов дали не столь удовлетворительные результаты, как это ожидалось, вне зависимости от модели протеза. Главной проблемой после их имплантации остается высокая частота развития нарушений кровообращения в органах, в том числе в мозге, за счет отрыва от синтетических подвижных частей протеза мелких кровяных свертков, возможность образования которых существует даже при старательной и избыточной антикоагулянтной терапии. С другой стороны, медикаментозное углубление нарушений свертывания крови повышает риск кровотечений различной локализации, нередко фатальных. Поэтому у пациентов, имеющих язву желудка и двенадцатиперстной кишки, выраженную гипертоническую болезнь с опасностью мозговых кровоизлияний и пр. применение антикоагулянтов очень опасно.
В настоящее время можно с уверенностью утверждать, что попытки видоизменения механизмов крепления створок механических протезов, придание им подвижности, создание протеза из гибких синтетических структур и т.д. полностью исчерпали свои возможности в снижении частоты развития тромбоэмболических нарушений кровообращения, а применение антикоагулянтной терапии со всеми возможными ее осложнениями обязательно при любом механическом протезе.
Исчерпав резервы изменения моделей механических протезов в отношении снижения нарушений кровообращения, исследователи и клиницисты пытаются найти способы точного управления действием непрямых антикоагулянтов в надежде иметь возможность углубления антикоагулянтной терапии с минимизацией осложнений последней. С середины 80-х годов в странах Западной Европы и Северной Америки существует лабораторная система тестирования всех реактивов для выполнения анализа на степень глубины антикоагулянтной терапии (реактивов для определения т.н. протромбинового индекса, времени, отношения) в сравнении с эталоном Всемирной Организации здравоохранения (ВОЗ). Реактивы, чувствительность которых отличается от эталона ВОЗ более чем на 20%, считаются непригодными для применения. Остальные реактивы используются с корригирующим коэффициентом для определения современной формы выражения протромбинового времени – Международного нормализованного отношения (МНО).
Наконец, фирмами-производителями механических протезов созданы персональные коагулометры, основанные на определении МНО с помощью полосок с сухими реагентами. Пациент сам или с помощью родственников осуществляет забор крови путем прокалывания подушечки пальца, наносит каплю крови на определенное место на полоске с реактивами, а затем вводит полоску в аппарат, на экране которого через 30-60 сек. выдается показатель МНО.
В кардиохирургической литературе сейчас с надеждой оценивают влияние новых методов контроля за терапией непрямыми антикоагулянтами на частоту возникновения нарушений мозгового кровообращения и длительность жизни пациентов с механическими протезами в целом.
Из выше изложенного можно заключить, что несмотря на все предпринимаемые меры, тромбообразование на механическом протезе остается высоко вероятным, а небезопасная сама по себе антикоагулянтная терапия обязательна для пациента с любым механическим протезом.
Теперь оценим российские условия жизни пациента с механическими протезами.
Отечественные однодисковые протезы достаточно надежны и показали низкую частоту поломок в организме человека в процессе длительного функционирования, чего нельзя сказать о двустворчатых отечественных моделях, с нарушением функции которых чисто технического свойства (выпадение или фрагментация створок) связана серия скандальных судебных процессов в середине 90-х годов. Подобные поломки клинически протекают крайне тяжело, и если пациент находится далеко от специализированного кардиохирургического центра, смертельный исход вероятен почти в 100% случаев. Справедливости ради, необходимо отметить, что все крупные мировые производители механических протезов не избежали случаев технических поломок своих моделей, хотя частота их возникновения была невысокой.
Что же касается проблем свертывания крови на протезе, все выше изложенные моменты можно полностью перенести на наши российские протезы, но с некоторыми национальными особенностями, которые изложены ниже.
Во – первых, в России существуют реальные трудности в точном определении протромбинового теста в том или ином варианте в связи с закупкой больницами самых разнообразных реагентов, зачастую весьма далеких от эталонов ВОЗ. Имеется порочная практика длительного хранения приготовленного реагента с целью экономии, в результате чего цифровое выражение протромбинового теста совершенно дезинформирует и больного, и лечащего врача. Определение же современной формы выражения протромбинового времени, т.е. МНО, выполняется еще в меньшем количестве лабораторий страны. В результате, получить достоверный анализ можно исключительно в больницах, где выполняются операции на сердце и верификации методики уделяется большое внимание. Из этого вытекает вторая особенность.
Во – вторых, если учесть, что таких больниц и центров в России лишь несколько десятков, то можно представить себе препятствия в получении анализа, которые носят территориальный характер.
В – третьих, в России непрямые антикоагулянты не производятся. Из недорогих препаратов имеется препарат фенилин производства Харьковского химфармзавода (ХФЗ) и Таллинского ХФЗ. Несмотря на одинаковую дозировку, производимое действие препаратов заметно отличается. Мало того, мы замечали отличие и между разными сериями препарата одного и того же завода. Все это опять же требует приближения пациента к лаборатории, могущей дать оценку эффекта от приема препарата. К счастью, сейчас в России имеется в продаже высоко стандартизированный непрямой антикоагулянт варфарин фирмы Никомед, а также ввозятся в Россию индивидуальные коагулометры фирмы Зульцер, но стоимость этих продуктов несравнима с выше упомянутыми препаратами, и они недоступны для большинства россиян.
В – четвертых, осведомленность провинциальных российских врачей о принципах проведения терапии непрямыми антикоагулянтами совершенно недостаточна. Наша практика дает обилие примеров полного непонимания врачом, как соотносятся результаты анализа и дозировка препарата, какую тактику избрать при выполнении хирургических процедур у больного с приемом непрямых антикоагулянтов и т.д. В результате, больной сам должен глубоко разбираться в этом предмете, т.е. работает принцип — «спасение утопающих – дело рук самих утопающих».
За годы увлечения механическими протезами, годы надежд и разочарований, кардиохирургия шла вперед, снижая и снижая смертность, связанную с операцией, в результате чего повторное вмешательство на сердце стало обыденностью, выполняемой с риском, не отличающимся от первичной операции.
В новых условиях необходима переоценка наших взглядов на протезирование клапанов, заключающаяся в том, что качество жизни больного с протезом должно быть для нас более значимым, чем страх перед второй операцией, что кажущаяся надежность и долговечность механического протеза оборачивается заменой одной болезни на другую, иногда более опасную, чем первая. Вот почему мы предлагаем пациентам вернуться к имплантации протезов из биологических тканей. Эти протезы не требуют терапии непрямыми антикоагулянтами, современные методики обработки биоткани позволяют обеспечить нормальную работу протеза до 10-12, а иногда и до 20 лет, биологическая деградация протеза происходит постепенно, без возникновения критических ситуаций, подобно природному человеческому клапану, пораженному патологическим процессом. Заглянем в инструкцию к биологическому протезу Sulzer Mitroflow Synergy в раздел «Показания»: «…клапан предложен для использования у тех пациентов, которым нежелательна долговременная антикоагулянтная терапия по разным причинам, как-то проживание в отдаленных областях, наличие болезней желудочно-кишечного тракта или других потенциальных источников кровоточивости, у которых ожидается хирургическая операция в других областях, у пожилых пациентов, и при прочих ситуациях, когда предвидятся трудности в проведении антикоагулянтной терапии по социальным или медицинским причинам». А есть ли вообще пациенты, которым показана имплантация механического протеза? Кто может знать, что ждет больного с механическим протезом в будущем, не возникнет ли у него язва желудка, не потребуется ли операция, не захочет ли молодая женщина родить ребенка? Жизнь с механическим протезом полна опасностей и ограничений.
Вот почему мы имеем в нашем арсенале и предлагаем больным большой набор заменителей клапанов, созданных из биотканей. Среди них ксеноартериальные (рис.3) и ксеноперикардиальные (рис.4) протезы бразильской фирмы BRAILE, биологические протезы фирмы Зульцер (рис.5-1), (рис.5-2), отечественные биопротезы «КемКор» (г. Кемерово) (рис.6) и, наконец, донорские гомографты оригинального производства (рис.7).
| Рис. 3 Биологический ксеноаортальный протез BRAILE (Бразилия) | Рис.4 Биологический ксеноперикардиальный протез BRAILE (Бразилия) | Рис. 5-1 Биологический ксеноперикардиальный протез Mitraflow Synergy (США) |
| Рис. 5-2 Биологический ксеноаортальный протез «LABCOR» (США) | Рис.6. Отечественный биологический ксеноаортальный протез «КемКор» | Рис.7 Гомоаортальный трансплантат (гомографт,аллографт) |
2.Этапы операции
На первом этапе
больного подключают к кардиомониторам, обрабатывается грудная клетка, подводятся дыхательные трубки от аппарата искусственного дыхания, который подключается только после того, как начнет действовать наркоз (т.е. единственным дискомфортом для больного может стать некоторое першение и саднение в горле после операции).
Анестезиолог вводит пациента в состояние общего наркоза. С этого момента оперируемый не ощущает ничего.
Через пищевод в область сердца помещается ультразвуковое устройство, транслирующее изображение сердца на монитор в течение всей операции.
Второй этап
– это открытие грудной клетки. После разметки кардиохирург делает разрез на груди от вершины грудной клетки до пупка. При малоинвазивном методе длина разреза меньше на две трети.
Целью третьего этапа
является подключение к аппарату, обеспечивающему искусственное кровообращение. Во время операции обогащение крови кислородом происходит вне лёгких, затем она возвращается в аорту и движется по большому кругу кровообращения.
На этом этапе хирург останавливает сердце, промывает его и помещает в специальный раствор, поддерживающий его жизнеспособность вне кровообращения.
Четвёртый и пятый этапы
– это собственно замена клапана. Аорта разрезается, удаляется больной клапан. Если поражена и часть аорты, она тоже удаляется и ставится трансплантат. Отверстие клапана замеряется для подбора нового клапана нужного размера. Новый клапан пришивается, затем необходимо проконтролировать отсутствие истечений через него.
Шестой этап
– это отключение от аппарата искусственного кровообращения. Зашивается аорта, из полости сердца удаляется попавший в него воздух. Сердце начитает биться под током собственной крови. Если наблюдается неровный ритм, применяется электрошок, который восстанавливает ровный пульс.
Седьмой этап
– закрытие грудной клетки. Кости и ткани сшиваются, грудина закрывается швом, которые остаётся видимым на всю жизнь.
Вся операция обычно длится от 2 до 5 часов.
Немаловажным для исхода лечения является восьмой этап.
Начинается он в палате интенсивной терапии. Выписка из стационара происходит на 5-9 день после операции. Послеоперационная реабилитация продолжается амбулаторно.
Посетите нашу страницу Кардиология
Последствия и реабилитация в послеоперационный период
После операции пациент находится в отделении реанимации. Врачи наблюдают за состоянием больного, так как возможны негативные последствия и ему нужна будет реабилитация. В первые сутки могут быть такие осложнения, как внутреннее кровотечение, тромбоэмболия, нарушение сердечного ритма, инфекционный эндокардит, инфаркт (менее чем в 5 % случаев). Через двое суток пациенту разрешают вставать и ходить. В это время он может жаловаться на боли в грудной клетке и повышенную усталость. Выписывают пациента домой в сроки от 4 до 10 дней, где он находится под наблюдением врача.
Послеоперационный период длится 3 недели, в течение которого возможны временные нарушения сна, зрения, аппетита, отеки ног. Через месяц пациент проходит полное обследование. Кардиолог рассчитывает адекватную физическую нагрузку, диету, назначает поддерживающее лечение. Важно выполнять лечебную физкультуру для укрепления сердечной мышцы.
Причины пороков клапанов сердца
Пороки клапанов сердца у взрослых — это заболевания, в основе которых лежат нарушения клапанного аппарата (створок клапанов, фиброзного кольца, хорд, папиллярных мышц), врожденные или развившиеся в результате заболеваний и травм, нарушающие правильный кровоток через клапаны и приводящие к серьезным осложнениям, таким как тяжелая сердечная недостаточность, синкопальные состояния, аритмии, внезапная сердечная смерть и т.д.
Стеноз – это сужение отверстия клапана по различным причинам, вследствие чего сердцу приходится работать избыточно, преодолевая данное препятствие.
Недостаточность клапана – нарушение работы створок клапана, приводящее к их неполному смыканию и возвращению крови обратно в камеру сердца, что приводит к работе сердца с избыточным объемом крови.