Описание
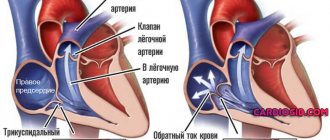
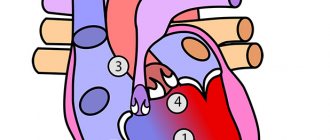
Главная задача трехстворчатого клапана (ТК) состоит в обеспечении односторонней циркуляции крови в правых отделах сердца. Открываясь при сжатии предсердий, он пропускает кровь в правый желудочек. Закрываясь, клапан не дает затечь крови в предсердие при сокращении желудочков.
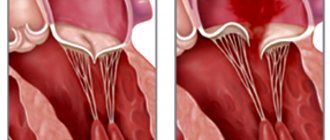
Что происходит при недостаточности ТК? Створки клапана полноценно не смыкаются, пропуская кровь в обратном направлении. Это называется регургитацией, из-за которой полость правого предсердия переполняется кровью и расширяется. Вследствие этого из ПП в правый желудочек (ПЖ) поступает больше крови, чем в норме, что также приводит к расширению последнего. Чтобы протолкнуть чрезмерное количество крови, желудочку приходится работать «нон-стоп», из-за чего развивается его гипертрофия (утолщение мышечного слоя). Положение дел со временем ухудшается: ПЖ больше не может работать в нужном темпе и полностью теряет силу.
Возникает состояние, которое называется правожелудочковой сердечной недостаточностью. Кровь начинает застаиваться везде, где может, особенно в нижних конечностях, почках, селезенке, печени.
Недостаточность трикуспидального клапана составляет примерно 15—30 % случаев всех пороков сердца. Также хочу отметить, что изолированный вариант недостаточности ТК — это скорее исключение, чем правило. Он встречается очень редко и чаще всего идет рука об руку с митральными пороками сердца.
В незначительной степени трикуспидальная регургитация может наблюдаться и у здоровых людей.
В запущенных формах исходом могут стать инвалидность и следующие осложнения:
- мерцательная аритмия;
- тромбоз и эмболия легочной артерии;
- кардиогенный цирроз печени вследствие длительного венозного застоя крови.
Пороки клапанов сердца и их лечение
Терапия клапанов сердца включает несколько методов: 1) медикаментозное лечение; 2) операция по реконструкции клапана; 3) операция по замене клапана; и 4) замена клапана чрескатетерным способом. Хотя лекарственная терапия не может устранить дисфункцию клапана, во многих случаях она может облегчить симптомы. Если появляется необходимость в реконструкции или протезировании клапана, ваш кардиолог, хирург или специалист по интервенционной кардиологии расскажет Вам о возможных методах лечения. Выбор между протезированием или реконструкцией зависит от ряда факторов, включая какой именно клапан поражен, тяжесть заболевания, наличие стеноза или регургитации.
Ваша бригада кардиологов
Если Вам предстоит операция по реконструкции или протезированию клапана сердца, за Вами будет наблюдать группа медицинских специалистов, которые стремятся обеспечить вашу безопасность и комфорт до, во время и после операции. Далее представлена информация, описывающая различных медицинских работников, с которыми Вы можете встретиться в ходе лечения.
Врач общей медицинской практики (терапевт) Возможно, первым обнаружит симптомы порока клапана сердца или заболевания, которые могут вызвать порок или нарушение работы клапана. Терапевт может назначить специальные исследования для подтверждения диагноза или направить Вас к соответствующему специалисту.
Кардиолог — врач, специализирующийся на заболеваниях сердца. Кардиолог не выполняет операций на сердце, но обычно проводит диагностические исследования, чтобы определить причину проблем с сердцем и назначить курс лечения для устранения нарушений работы сердца. Кардиолог может назначить прием лекарств и/или направить Вас к сердечно-сосудистому хирургу.
Сердечно-сосудистый хирург — врач, специализирующийся на операциях на сердце, в том числе по реконструкции или протезированию пораженных клапанов сердца. Хирург — основой специалист в процессе принятия решения о сроках и наилучшей стратегии, включая методику операции и выбор медицинского изделия для Вашего случая поражения клапана.
Специалист по интервенционной кардиологии (интервенционный кардиолог) — врач, прошедший дополнительную специализированную подготовку для проведения катетерных процедур по лечению заболеваний сердца. Интервенционный кардиолог сотрудничает с хирургом, чтобы сделать правильный выбор в вопросе необходимости проведения замены аортального клапана транскатетерным методом.
Анестезиолог — врач, обученный проводить седацию или давать общий наркоз (сон) при проведении хирургического вмешательства.
Врачи и медицинские сестры отделения интенсивной терапии — в отделении интенсивной терапии пациент находится под пристальным наблюдением и содержится после большинства видов хирургического вмешательства. Совместно с вашим хирургом и/или кардиологом врачи отделения интенсивной терапии и медсестры заботятся о Вас в этот период.
Подходы к хирургическому лечению пороков клапанов сердца
Большинство операций на сердце выполняется через разрез по всей длине грудной клетки, или грудины. Такой разрез называют срединной стернотомией. Как правило, процесс заживления проходит довольно хорошо, требуется около 6 недель для полного восстановления кости.
У некоторых пациентов операция на клапане сердца может быть выполнена с использованием небольших, то есть минимально инвазивных разрезов. Разрезы меньшего размера дают пациентам рад преимуществ. Предоперационные исследования, включая коронарографию, эхокардиографию и, во многих случаях, КТ грудной клетки (компьютерная аксиальная томография), помогают определить, каким пациентам может быть показана минимально инвазивная операция. Хирургические подходы, при которых выполняют небольшие разрезы, также подразумевают использование аппарата искусственного кровообращения, как и операции с проведением стернотомии.
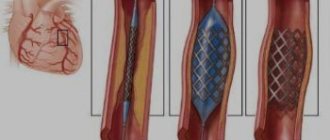
Транскатетерное протезирование аортального клапана (англ. TAVR): менее инвазивная альтернатива операции на открытом сердце
Если пациенту был диагностирован стеноз аорты тяжелой степени, но операция на открытом сердце сопряжена с умеренным или высоким риском, доступен другой вариант: транскатетерная протезирование аортального клапана (англ. TAVR). Данную процедуру также называют транскатетерной имплантацией аортального клапана (англ. TAVI). Это минимально-инвазивная операция, которая не требует вмешательства на открытом сердце.
| Процедура транскатетерного протезирования аортального клапана позволяет установить новый клапан в Ваш пораженный аортальный клапан. Новый клапан отодвигает створки Вашего пораженного клапана в сторону. Каркас имплантируется в створки Вашего пораженного клапана, чтобы обеспечить правильное расположение. |
Такая минимально-инвазивная процедура отличается от операции на открытом сердце. В ходе транскатетерного протезирования аортального клапана вместо рассечения грудной клетки и полного удаления пораженного клапана замену клапана проводят с помощью катетера.
Транскатетерное протезирование аортального клапана может быть выполнено несколькими способами, однако наиболее часто используют трансфеморальный (через разрез на бедре). Только бригада кардиологов может определить наилучший способ, принимая во внимание состояния здоровья человека и другие факторы.
Операция по протезированию клапана
Если сердечно-сосудистый хирург примет решение заменить сердечный клапан пациента, первым шагом является удаление пораженного клапана (удаление клапана и отложений кальция), а вторым — имплантация протеза клапана сердца на его место. Протезы клапанов, используемые для замены пораженных естественных клапанов, изготавливают из различных материалов и различных размеров.
Существуют две обширные категории протезов клапанов сердца, которые используются для замены пораженных клапанов:
- Биологические протезы, изготавливаемые в основном из тканей животных, а именно бычьего (коровьего) перикарда (прочной сумки, окружающей сердце), клапана аорты свиньи или же клапанов человека, взятых у посмертного донора.
- Механические клапаны изготовлены из синтетического материала, преимущественно углерода.
Биопротезы клапанов
Существует большое разнообразие биопротезов клапанов:
- Гетеротрансплантат (или ксенотрансплантат) — ткань клапана или перикарда животного происхождения, пригодная для использования в медицине (например, крупного рогатого скота (коров) или свиней).
- Гомотрансплантат (или аллотрансплантат) — человеческие клапаны, полученные от посмертного донора.
- Аутотрансплантат/собственная ткань — здоровый клапан, который был перемещен из одного места в организме человека в другое для замены пожаренного клапана (касается только клапана легочной артерии, который используют для замены клапана аорты).
Ксенотрансплантат — это биологический клапан, изготовленный из ткани животного происхождения. Так, створки клапана из перикарда обычно изготавливают из бычьего (коровьего) перикарда (сумки, окружающей сердце) и пришивают к гибкому или полужесткому каркасу. Кроме того, биологические протезы клапанов изготавливают из свиных клапанов. Клапан изготавливают из аортального клапана свиньи и обычно пришивают к гибкому или полужесткому каркасу и получают «каркасный» клапан. В ином случае, естественный корень аорты свиньи остается неизмененным и выступает в роли каркаса в «бескаркасном» клапане. Каждый клапан окружен тканевым кольцом (манжетой) для пришивания. Швы накладываются через манжету, чтобы прикрепить клапан к сердцу.
| Биологические протезы клапанов |
Механические клапаны
Створки механических клапанов изготовлены из специального типа углерода. Такие клапаны обычно имеют две створки. Створки открываются и закрываются в ходе сердечного цикла, обеспечивая движение крови в одном направлении.
Критерии и выбор сердечных клапанов
Выбор между механическим и биологическим протезом клапана зависит от индивидуальной оценки преимуществ и рисков каждого клапана, а также образа жизни, возраста и состояния здоровья каждого пациента.
Биопротезы не требуют длительного применения препаратов, подавляющих естественную способность крови к свертыванию (антикоагулянтов). Это важно для тех, кто не может принимать антикоагулянты из-за ранее перенесенных крупных кровотечений (например, желудочно-кишечной или мочеполовой системы) или повышенного риска травматических повреждений и кровотечений, связанных с активным времяпрепровождением, спортом или преклонным возрастом. Биопротезы обычно служат не менее 10 лет, а в некоторых случаях — более 30 лет. Если пациенту в возрасте до 60 лет имплантируют биопротез клапана, существует высокая вероятность того, что в какой-то момент возникнет повторная необходимость протезирования клапана, в то время как большинству пациентов в возрасте 70 лет и старше этого не требуется.
Механические клапаны мало подвержены износу. Однако, они требуют ежедневного приема антикоагулянтов, что может потребовать изменений в питании или образе жизни.
Зачастую решение о выборе биологического или механического протеза клапана связано с возрастом пациента, причем пожилым пациентам преимущественно устанавливают биопротезы. Однако нет единого мнения относительно точного возраста, в котором биопротез может быть предпочтительнее механического клапана.
Операции по реконструкции клапанов
Если это представляется возможным, предпочтительнее реконструировать клапан пациента, а не заменять его протезом. Обычно в ходе операции по реконструкции клапана хирург корректирует ткань или основные структуры митрального или трикуспидального клапанов.
Почти все операции по реконструкции клапанов включают в себя установку кольца или полукольца для аннулопластики. Это покрытое тканью изделие, которое имплантируется по окружности, или отверстию, митрального или трикуспидального клапана. Оно обеспечивает поддержку собственному клапану пациента и позволяет плотнее закрыть его створки, потенциально уменьшая протечки через клапан. Существует множество различных изделий для аннулопластики. Хирург выберет то, которое лучше всего подойдет для клапана Вашего сердца.
| Кольца для аннулопластики |
В дополнение к аннулопластике, реконструкция митрального клапана часто требует коррекции проблем со створками или хордами, которые прикрепляют створки клапана к сердцу. Если протечки обусловлены пролапсом митрального клапана, фиксация створок и хорд (и имплантация кольца или полукольца для аннулопластики) восстанавливает нормальную работу клапана.
Уход за пациентом после операции на клапане сердца
В норме период восстановления после стандартной операции на клапане сердца занимает от четырех до восьми недель. Восстановление может протекать быстрее, если был выполнен малый разрез, например, при минимально-инвазивных и транскатетерных операциях. За это время пациенты постепенно набираются сил и возобновляют нормальную повседневную деятельность. Регулярное обследование у кардиолога имеет большое значение. Обращайтесь к своему лечащему врачу по телефону или лично, если у Вас возникают вопросы или опасения по поводу здоровья, особенно при возникновении каких-либо необычных симптомов или изменении общего состояния здоровья.
Питание и физические упражнения
Два дополнительных важных аспекта восстановления и хорошего самочувствия в целом — это здоровое питание и регулярное выполнение физических упражнений. Если Ваш врач рекомендовал специальную диету, важно обязательно соблюдать ее. Здоровое питание является неотъемлемой частью здоровой жизни. В ходе восстановительного периода употребление богатых питательными веществами блюд обеспечит ваше тело энергией и может помочь ускорить процесс выздоровления.
Для улучшения общего состояния сердечнососудистой системы рекомендуется сочетать сбалансированную диету с рекомендациями врача по физической нагрузке и контролю веса. Регулярное выполнение программы физических упражнений является важной частью поддержания здорового образа жизни. Под руководством Вашего врача Вы должны постепенно наращивать физическую нагрузку и уровень активности. Прежде чем приступить к новому виду спортивной деятельности, проконсультируйтесь с врачом.
Антикоагулянты — важно следовать указаниям Вашего врача по приему лекарств, особенно если был назначен антикоагулянт. Антикоагулянты, или противосвертывающие препараты, подавляют естественную способность крови к свертыванию. Если Вам показан прием антикоагулянтов, Вам потребуется периодически выполнять анализ крови, чтобы оценить способность крови к свертыванию. Результат такого исследования поможет Вашему врачу определить необходимую дозировку антикоагулянта. Установление правильной дозировки препарата может занять некоторое время, но последовательность и сотрудничество с Вашим врачом имеют большое значение. Иногда возможно проводить исследование самостоятельно в домашних условиях, спросите об этом у врача. Проконсультируйтесь с Вашим врачом о взаимодействии с другими препаратами, которые Вы принимаете, и об ограничениях, касающихся диеты, которые действуют при приеме антикоагулянтов. Узнайте обо всех признаках, которые могут указывать на то, что Ваша дозировка слишком высока.
Прочая медицинская информация — Перед выполнением любых стоматологических процедур, включая профгигиену, проведением эндоскопии или операции, сообщайте врачу об установленном протезе сердечного клапана. Пациенты с протезом клапана более восприимчивы к инфекциям, которые могут в будущем привести к поражениям сердца. Поэтому, возможно, до и после некоторых медицинских процедур Вам потребуется принимать антибиотики, чтобы снизить риск заражения.
Кроме того, отправляясь в поездку более чем на несколько дней, старайтесь поддерживать диету и уровень физических упражнений как можно ближе к своей норме. Обязательно обсудите все препараты, которые Вы принимаете (в том числе безрецептурные), с Вашим врачом и не меняйте дозировку без особого на это указания.
Возможные причины появления
Существует много причин развития трикуспидальной недостаточности. К наиболее частым из них относят:
- Ревматизм — аутоиммунное воспаление, часто охватывающее клапаны. Может возникнуть через 1—2 недели после ангины (тонзиллита), вызываемой особым бета-гемолитическим стрептококком. Это наиболее частая причина не только недостаточности ТК, но и многих других приобретенных пороков сердца у детей.
- Инфекционный эндокардит — острая патология внутренней оболочки сердца, которую иногда называют «болезнью инъекционных наркоманов» из-за высокого риска инфицирования во время нечистоплотной инъекции. Но он также может развиться из-за плохой антисептической обработки кожи при непрофессиональной процедуре.
- Пороки митрального клапана (МК) — недостаточность МК или стеноз митрального отверстия часто возникают как следствие патологии трехстворчатого клапана.
- Заболевания дыхательной системы — хроническая обструктивная болезнь легких, бронхиальная астма.
- Врожденные сердечные дефекты — аномалия Эбштейна.
- Кардиологические болезни — кардиомиопатии, миокардиосклероз.
- Повышение давления в легочной артерии.
Более редкие причины недостаточности ТК:
- Использование лекарственных препаратов — некоторые медикаменты могут оказывать разрушающее действие на створки, например средство от мигрени «Метисергид» или таблетки для похудения «Фенфлурамин».
- Воздействие ионизирующего излучения — лучевая терапия для лечения злокачественных опухолей.
- Наследственные болезни, проявляющиеся дефектом соединительной ткани, — синдром Элерса-Данло, синдром Марфана, недифференцированные дисплазии.
- Карциноидные опухоли. При нейроэндокринных новообразованиях, расположенных в органах желудочно-кишечного тракта, по неизвестным причинам часто поражается трикуспидальный клапан.
- Ревматические болезни — ревматоидный артрит, системная красная волчанка, системная склеродермия, дерматомиозит.
- Болезнь Уиппла — очень редкая хроническая кишечная инфекция, которая может осложниться эндокардитом.
Трикуспидальный клапан (ТК) и его патология по сравнению с аортальным и митральным клапаном (МК) не получают должного внимания кардиологов и кардиохирургов. В результате имеется недостаток исследований и научных публикаций в этом направлении, в том числе в нашей стране. Точное понимание механизмов развития функциональной недостаточности ТК, определение тактики лечения при коррекции порока остаются до конца не решенной проблемой в клапанной хирургии сердца.
Под функциональной недостаточностью ТК, как правило, принято понимать недостаточность без структурных изменений элементов клапана на фоне дилатации и дисфункции правого желудочка (ПЖ), дисфункции левого желудочка (ЛЖ), легочной гипертензии, которые возникают при патологии МК, реже аортального клапана.
По данным разных авторов [10, 22, 37], функциональная недостаточность ТК встречается у 8—35% оперированных по поводу порока МК или аортального клапана.
Как известно, трикуспидальная регургитация (ТР) служит независимым прогностическим фактором прогрессирования хронической сердечной недостаточности и смерти после адекватной коррекции пороков МК и/или аортального клапана [11, 21, 25]. Так, по данным J. Nath и соавт. [47], годичная выживаемость для пациентов со II и III степенью регургитации составила 78,9 и 63,9% соответственно, независимо от функции ЛЖ, степени легочной гипертензии и возраста. При этом, по данным A. Calafiore и соавт. [16, 18], 5-летняя выживаемость пациентов со II и III степенью ТР после изолированной коррекции митрального порока составила 46%.
Этиологическим фактором в возникновении функциональной трикуспидальной недостаточности (ТН) являются патологические процессы, вызывающие пороки левых отделов сердца или легочную гипертензию [10, 41, 51, 53, 55]. Чаще всего это ревматическая болезнь сердца, ишемическая митральная недостаточность, миксоматозная дегенерация, дегенеративное (атеросклероз) поражение клапанов, инфекционный эндокардит левых отделов сердца, дилатационная кардиомиопатия, тромбоэмболия легочной артерии. В то же время в ряде исследований [59] достоверной связи между выраженностью порока МК и тяжестью ТН не находят.
Основным фактором развития регургитации большинство авторов [9, 27, 51, 55] считают дилатацию фиброзного кольца. По мнению G. Dreyfus и соавт. [25], дилатация фиброзного кольца — более объективный показатель тяжести ТН, чем степень ТР. С этим нельзя не согласиться, так как известно, что степень ТР, определяемая при эхокардиографии, может меняться в зависимости от пред-, посленагрузки и сократимости ПЖ. Считается, что при дилатированном кольце выраженная ТР с течением времени в большинстве случаев так или иначе проявится. С.Г. Суханов и соавт. [5] проследили результаты сочетанных операций — аннулопластики МК и реваскуляризации миокарда. Прогностическими факторами возникновения функциональной ТН после этих операций они считают дилатацию фиброзного кольца и фракцию выброса ЛЖ. Л.А. Бокерия и соавт. [1], кроме того, отмечают корреляцию между диаметром фиброзного кольца и степенью ТР.
Кроме, собственно, расширения фиброзного кольца, имеются данные об изменении и пространственной трехмерной конфигурации кольца в сторону его «уплощения» [8]. T. Ton-Nu и соавт. [60] исследовали трехмерную конфигурацию ТК у лиц без ТР и имеющих регургитацию на клапане. В группе без регургитации кольцо клапана имеет отчетливо более высокое положение переднезадних сегментов (относительно медиолатеральных) и эллипсовидную форму. При развитии функциональной ТН кольцо клапана «уплощается» и принимает более округлую форму. Сходные данные приводит S. Fukuda и соавт. [29] на меньшем числе наблюдений.
В качестве других факторов, вызывающих регургитацию, называют дилатацию ПЖ и следующее за ней смещение папиллярных мышц, что приводит к увеличению аннулоапикального расстояния, избыточному натяжению хорд и нарушению коаптации створок. Это состояние в англоязычной литературе обозначается термином «tethering», или «tenting» [9, 55]. Кроме того, по некоторым данным дилатация ПЖ увеличивает число ассоциированных с клапанными пороками осложнений [44].
M. Antunes и соавт. [10] в качестве одного из механизмов развития и усугубления дисфункции ПЖ, а следовательно и ТР, описали «рестрикционно-дилатационный синдром». Этот механизм представляет собой «порочный круг», когда дисфункция ЛЖ через повышение давления и/или объема в малом круге кровообращения приводит к дисфункции ПЖ. Это в свою очередь усугубляет дисфункцию ЛЖ посредством межжелудочкового взаимодействия через межжелудочковую перегородку.
Еще одним немаловажным элементом в развитии ТН является легочная гипертензия. M. De Bonis и соавт. [23] выявили зависимость между систолическим давлением в легочной артерии и степенью дисфункции ЛЖ. Аналогичные данные приводят S. Fukuda и соавт. [28]. В другом исследовании R. Ghanta и соавт. [33] обнаружили, что больные, у которых давление в легочной артерии после пластики ТК составляет 52 мм рт.ст. и выше, более подвержены рецидиву ТР. J. Nath и соавт. [47] отметили, что давление в легочной артерии более 40 мм рт.ст. утяжеляет ТР и повышает смертность.
По данным G. Lin и соавт. [39], одной из причин развития ТН может быть имплантация эндокардиальных электродов для кардиостимуляторов и кардиовертер-дефибрилляторов.
Таким образом, понимание механизмов развития ТН помогает в определении основных направлений при хирургической коррекции порока.
Длительное время под влиянием публикации N. Bra- unwald и соавт. [15] считалось, что коррекция ТР после успешной коррекции порока левых отделов сердца не требуется и что ТР регрессирует самостоятельно. О. Yilmaz и соавт. [62] в своем ретроспективном исследовании показали, что даже ТР III степени и выше регрессировала в течение 3 лет наблюдения после изолированной пластики МК. На этом основании они считают, что бессимптомная ТР не требует обязательной коррекции.
Однако есть сообщения, противоречащие этому убеждению. По данным A. Calafiore и соавт. [16, 18], 5-летняя выживаемость пациентов со II и III степенью ТР после изолированной коррекции митрального порока составила 45—46%, а с I степенью или без регургитации — 74,5—88,2%. Показано также, что, несмотря на уменьшение степени регургитации в раннем послеоперационном периоде у пациентов с некорригированной ТН, в отдаленном периоде она прогрессирует. H. Song и соавт. [57] отследили течение некорригированной ТН I и II степени у 638 пациентов, оперированных по поводу пороков левых отделов сердца. У 7,7% пациентов впоследствии развилась ТР III или IV степени. K. Matsuyama и соавт. [41] проанализировали отдаленные результаты коррекции пороков левых отделов без вмешательств на ТК с регургитацией в пределах II степени. У 16% пациентов в сроки наблюдения до 8 лет произошло прогрессирование ТН до III степени и выше. Дооперационная регургитация II степени, фибрилляция предсердий и атриомегалия левого предсердия более 60 мм были идентифицированы как факторы, ухудшающие течения ТР в отдаленном периоде.
A. Matsunaga и соавт. [40] представили результаты лечения 124 больных с ишемической митральной недостаточностью. При этом у 30% пациентов имелась выраженная ТР и только 43% из них выполнена аннулопластика. К окончанию наблюдения у 49% пациентов имелась регургитация не ниже III степени, у 74% пациентов без регургитации до операции в срок более 3 лет отмечалось появление регургитации на ТК. У пациентов с ТР как до операции, так и после нее, выявлен высокий индекс диаметра кольца/площадь поверхности тела.
При определении показаний к коррекции функциональной ТН существуют разные мнения. У большинства хирургов не вызывает сомнений необходимость коррекции выраженной регургитации III и IV степени [11, 17, 23, 49]. Однако вопрос о коррекции регургитации I и II степени остается нерешенным. G. Dreyfus и соавт. [25] пациентам с диаметром фиброзного кольца клапана менее 7 см, измеренного между переднесептальной и переднезадней комиссурами, выполняли коррекцию только митрального порока, а имевшим диаметр 7 см и более — коррекцию митрального порока и аннулопластику ТК. Степень регургитации до операции в обеих группах в среднем была менее I. В отдаленном периоде отмечено усугубление ТР более чем на две степени у 48% пациентов, которым не выполняли аннулопластику, и только у 2% получивших аннулопластику. В итоге они сделали вывод, что ориентация на диаметр трикуспидального кольца при определении показаний к коррекции ТН дает лучший результат.
N. Van de Veire и соавт. [61] пришли к заключению, что выполнение аннулопластики пациентам с дилатацией фиброзного кольца более 40 мм, по данным эхокардиографии, без значимой регургитации предотвращает дальнейшее прогрессирование ТН и способствует обратному ремоделированию ПЖ. У пациентов с ТР I, II степени и дилатацией фиброзного кольца, которым аннулопластика не выполнялась, констатировано прогрессирование ТН и дилатация ПЖ. Другие авторы [56] также предлагают выполнять аннулопластику ТК пациентам с умеренной степенью регургитации, если имеется дилатация фиброзного кольца более 40 мм или легочная гипертензия. V. Chan и соавт. [21] указывают, что ТР III и IV степени ассоциируется с повышенной смертностью в послеоперационном периоде. Выполнение аннулопластики ТК препятствует прогрессированию недостаточности и улучшает функциональный класс сердечной недостаточности пациентов, но не влияет на среднеотдаленную выживаемость. Наличие у пациентов с ТР III степени и выше в сочетании с дилатацией фиброзного кольца более 30 мм являются факторами, определяющими дальнейшее прогрессирование ТН. В.А. Иванов [3] показанием к коррекции функциональной недостаточности ТК также считает регургитацию II степени и выше и дилатацию фиброзного кольца более 40 мм (по данным чреспищеводной эхокардиографии).
Имеется определенная разница в руководствах по выполнению коррекции пороков ТК, предложенных Американской коллегией кардиологов/Американской ассоциацией сердца (ACC/AHA) и Европейским кардиологическим обществом (ESC).
Показания к коррекции трикуспидального порока, утвержденные ACC/AHA, включают следующие:
— пластика ТК показана при выраженной ТР пациентам с пороком МК, требующим операции (уровень доказательности В);
— протезирование или пластика ТК целесообразна у пациентов с первичной тяжелой симптомной ТР (уровень доказательности С);
— протезирование ТК целесообразно при выраженной ТР и измененных створках в случаях неэффективности пластики (уровень доказательности С);
— аннулопластика ТК возможна у пациентов с ТР менее IV степени во время операции на МК, если имеется легочная гипертензия или дилатация фиброзного кольца клапана (уровень доказательности С);
— пластика или протезирование ТК не показана пациентам с бессимптомной изолированной ТР и систолическим давлением в легочной артерии менее 60 мм рт.ст. (уровень доказательности С);
— протезирование или пластика ТК не показана пациентам с первичной ТР менее III степени (уровень доказательности С).
Согласно руководству по коррекции трикуспидальных пороков, принятым ESC, вмешательство на ТК показано в следующих случаях:
— пациентам с выраженной ТР во время коррекции пороков левых отделов сердца;
— пациентам с выраженной первичной ТР с клиническими проявлениями, не поддающейся медикаментозной терапии даже в отсутствие дисфункции желудочков;
— пациентам с выраженным трикуспидальным стенозом (с ТР или без нее), не поддающимся медикаментозной терапии;
— пациентам с выраженным трикуспидальным стенозом (с ТР или без нее), подвергающимся вмешательствам на левых отделах сердца;
— пациентам с умеренной органической ТР во время коррекции пороков левых отделов сердца;
— пациентам с вторичной умеренной ТР и дилатацией кольца более 40 мм во время коррекции пороков левых отделов сердца;
— пациентам с выраженной симптомной ТР с корригированными пороками левых отделов, в отсутствие дисфункции миокарда, клапанов, дисфункции ПЖ и легочной гипертензии;
— пациентам с выраженной изолированной малосимптомной ТР при прогрессирующей дилатации ПЖ и нарастании его дисфункции [43].
Наиболее распространенными методами хирургической коррекции функциональной ТН являются аннулопластика опорным кольцом, предложенная A. Carpentier в 1971 г., и шовная аннулопластика, предложенная N.G. De Vega в 1973 г., и их модификации [6, 19, 24].
И.И. Скопин и соавт. [4] выявили 3 типа строения ТК и выдвинули положение, что выбор типа аннулопластики должен производиться с учетом анатомического строения ТК.
По некоторым данным [14, 48, 49, 59], аннулопластика опорным кольцом обеспечивает более стойкий эффект в отдаленном периоде и более высокую выживаемость.
В частности, по данным P. McCarthy и соавт.[42], через 1 мес после аннулопластики по De Vega пациенты с регургитацией III и IV степени составили 13,6%, а через 8 лет — 33%. После пластики опорным кольцом этот показатели составили 15,2 и 17% соответственно. Несмотря на низкую частоту повторных операций (3% за 8 лет наблюдения), авторы отмечают высокую послеоперационную летальность после повторных вмешательств. Летальность составила 8%, а 5- и 8-летняя выживаемость — 65 и 50% соответственно. F. Filsoufi и соавт. [27] сообщали о хороших ближайших результатах после применения опорных колец трехмерной конфигурации и не наблюдали значимого увеличения степени регургитации.
G. Gatti и соавт. [31, 32] представили результаты использования эластичной полосы из политетрафторэтилена для аннулопластики. Летальность составила 5,7%, 4-летняя актуарная выживаемость — 91,7%. В среднеотдаленном периоде у 89,8% пациентов имелись ТР менее II степени и удовлетворительный функциональный статус. A. Calafiore и соавт. [17] предложили метод аннулопластики стандартной 50-миллиметровой полосой без учета площади поверхности тела и сообщили об удовлетворительных ближайших результатах. После такой пластики диаметр трикуспидального отверстия приближался к измерителю N25.
J. Bernal и соавт. [11] при коррекции функциональной ТН применяли шовную аннулопластику по De Vega и ее модификации. Летальность составила 8,1%, выживаемость в срок 6,8 года — 23,3%. Актуарная 12-летняя выживаемость составила 50,5%. Отмечена положительная динамика эхокардиографических показателей в виде уменьшения размеров ПЖ, уменьшения давления в легочной артерии. В период наблюдения ТР отсутствовала или была I степени у 50,6% пациентов, II степени — у 44,8%. Степень резидуальной ТР не влияла на смертность и частоту повторных операций на клапане в отдаленном периоде. Дооперационная тяжелая ТР была ассоциирована с большей частотой повторных операций. Повторная операция потребовалась 3,1% пациентам с функциональной ТН. Смертность после повторных операций составила 18,5%. A. Calafiore и соавт. [18] при выполнении аннулопластики по De Vega сообщали о 5-летней выживаемости 74,5% и прогрессировании ТР до III, IV степени у 5% пациентов; при этом летальность составила 5,5%. С.С. Добротин и соавт. [2] также отмечают удовлетворительные среднеотдаленные результаты после аннулопластики по De Vega. A. Sarraj и соавт. [54] сделали сообщение об использовании ими регулируемой сегментарной аннулопластики ТК, очень похожей на технику, предложенную Н.М. Амосовым в 1972 г., с удовлетворительными среднеотдаленными результатами.
R. Ghanta и соавт. [33] не выявили статистически значимых различий по среднеотдаленным результатам между шовной бикуспидализацией и кольцевой аннулопластикой; обе методики, по мнению авторов, дают хороший, стойкий эффект.
O. Alfieri и соавт. [7] в 2002 г. представили использованную ими для коррекции посттравматической ТР «технику клевера». В последующем E. Castedo и соавт. [20] описали подобную технику у пациентов с рецидивом ТН, назвав ее техника край в край. Y. Lai и соавт. [38] применяли данную технику как дополнительную процедуру в случаях неадекватной коррекции недостаточности кольцевой аннулопластикой и пластикой по Key и получили удовлетворительные результаты. M. De Bonis и соавт. [23] также представили результаты применения «техники клевера». Они использовали ее в дополнение к аннулопластике при пролабировании створок и при их натяжении, в 97% случаев — вследствие смещения папиллярных мышц, в 3% — изолированно. В среднеотдаленном периоде у 87,7% пациентов регургитация отсутствовала или соответствовала I степени, проявлений стеноза ТК не было.
G. Dreyfus и соавт. [26] для адекватной коррекции выраженной ТР у пациентов с нарушением коаптации вследствие смещения папиллярных мышц предложили выполнять увеличение передней створки заплатой из аутоперикарда с последующей имплантацией опорного кольца. Данное вмешательство выполнялось пациентам с глубиной коаптации более 8 мм. В сроки наблюдения от 6 до 20 мес резидуальная регургитация была не более I степени. F. Roshanali и соавт. [52] сравнили группы пациентов с тяжелой ТР, которым выполнялась аннулопластика и аннулопластика в сочетании с увеличением створки заплатой из аутоперикарда, если глубина коаптации была больше 8 мм или площадь глубины коаптации более 16 мм2. Через год резидуальная регургитация в группах, которым выполнена аннулопластика по De Vega и кольцевая аннулопластика, составила 28 и 14% соответственно, а в группах с пластикой по De Vega в сочетании с увеличением створки и кольцевой аннулопластики и увеличением створки — 10 и 8% соответственно.
U. Kappert и соавт. [35] предложили иной подход для коррекции ТН вследствие выраженной дилатации ПЖ — резекцию свободной стенки ПЖ в сочетании с кольцевой аннулопластикой. Через год наблюдения ТР не определялась.
R. Moraca и соавт. [46] при анализе результатов протезирования и пластики ТК не выявили различий в послеоперационном и отдаленном периодах. В заключение авторы указывают, что у пациентов, имеющих риск рецидива ТР, более предпочтительно протезирование клапана как более надежного и радикального вмешательства по редукции недостаточности. C. Park и соавт. [50] приводят схожие данные; они отметили лишь тенденцию к лучшей отдаленной выживаемости пациентов с пластикой клапана. Более того, не было летальных исходов у больных, которым выполнялось протезирование ТК в дополнение к коррекции порока левых отделов сердца. Авторы также считают, что в случаях с выраженной ТР и дисфункцией ПЖ следует отдавать предпочтение протезированию клапана. Другие авторы [13] определяют протезирование ТК как прогностический фактор повышенной летальности.
Несмотря на многочисленные сообщения о хороших результатах коррекции функциональной ТН, в ряде случаев наблюдается рецидив или прогрессирование ТР.
P. McCarthy и соавт. [42] в качестве независимых прогностических факторов, обусловливающих прогрессирование ТН, определили высокую дооперационную степень ТР, дисфункцию ЛЖ, наличие эндокардиального электрода, фибрилляцию предсердий и виды аннулопластик, отличные от кольцевой. M. De Bonis и соавт. [23] представили данные по коррекции ТР у пациентов с дилатационной кардиомиопатией и митральной недостаточностью. Через 1,8 года наблюдения у 12% пациентов имелась регургитация III или IV степени, у 18% пациентов с дооперационной регургитацией II степени и ниже в последующем произошло ее прогрессирование на две степени и выше. В качестве прогностических факторов прогрессирования ТР до III, IV степени рассматриваются выраженная регургитация на момент выписки и дооперационная дисфункция ПЖ. G. Gatti и соавт. [32] сообщают, что у пациентов с дооперационной регургитацией более II степени, фракцией укорочения ПЖ менее 35% и постоянным водителем ритма имелась тенденция к рецидиву ТР. R. Ghanta и соавт. [33] обнаружили, что такие факторы, как давление в легочной артерии после пластики ТК 52 мм рт.ст. и выше, а также высокая дооперационная степень регургитации, определяют склонность к рецидиву ТР.
В проспективном исследовании Y. Kim и соавт. [36] как независимый прогностический фактор неблагоприятного течения ТН после коррекции порока расценена дисфункция ПЖ. Чувствительным показателем дисфункции ПЖ представлена конечная систолическая площадь ПЖ; так, при площади менее 20 см2 отмечена более низкая частота развития сердечно-сосудистых осложнений в среднеотдаленном периоде. Сходные данные представили C. Park и соавт. [50].
S. Fukuda и соавт. [28] определили дооперационные глубину коаптации («tethering height») более 0,51 см и площадь «натяжения» («tethering area») более 0,8 см2, раннюю послеоперационную фракцию выброса ЛЖ менее 36,6% в качестве эхокардиографических прогностических факторов рецидива или персистенции ТР через год и более после операции. Также они обнаружили корреляцию между давлением в ПЖ и степенью ТР, и взаимосвязь между давлением в ПЖ и фракцией выброса ЛЖ в сроки наблюдения более года. Схожие данные авторы получили и для раннего послеоперационного периода [30].
S. Min и соавт. [45] в своей работе в качестве дооперационных эхокардиографических прогностических факторов резидуальной ТН выявили объем «натяжения» («tethering volume») более 1,68 мл и переднезадний размер кольца более 36 мм, а в качестве послеоперационных факторов — давление в легочной артерии.
H. Je и соавт. [34] показали, что возраст, ревматическая этиология митрального порока и невыполненная процедура Maze являются прогностическими факторами прогрессирования ТР II степени. Аналогичные данные представили H. Song и соавт. [57]. J. Stulak и соавт. [58] также сравнили группы пациентов с успешной процедурой Maze и коррекцией митрального порока с группой, в которой ритм не восстановился. Авторы сделали вывод, что успешная процедура Maze препятствует прогрессированию ТН. У пациентов с синусовым ритмом после операции степень ТН уменьшилась в 42% случаев, прогрессировала в 9%, а у пациентов с фибрилляцией предсердий — в 36 и 45% соответственно.
C. Yoon и соавт. [63] выявили, что уровень B-натрийуретического пептида более 200 пг/мл является неблагоприятным прогностическим фактором у больных с выраженной ТН.
По разным данным, летальность после коррекции ТН в сочетании с коррекцией пороков левых отделов сердца колеблется от 0 до 18%, но большинство авторов приводят цифры 4,4—8,1%. По данным J. Bernal и соавт. [12], летальность при повторных операциях после выполненной ранее пластики ТК составила 33,8%, частота осложнений развития 64,9%. Актуарная выживаемость через 10 лет после повторных операций составила 40%, а через 26 лет — 11,8%. В других работах авторы [11, 42] приводят летальность после повторных операций на уровне 18,5—37%.
Таким образом, функциональная ТН — достаточно серьезная проблема, которая сопутствует порокам левых отделов сердца и утяжеляет их течение. Выраженная ТР должна корригироваться без сомнения. Однако частые неудовлетворительные отдаленные результаты некорригированной регургитации I и II степени, возможно, обусловливают необходимость более активной хирургической тактики. Нуждаются в рассмотрении и другие параметры в качестве дополнительных или равнозначных степени регургитации при определении показаний к коррекции порока. До сих пор нет полной ясности, какая из методик аннулопластики является операцией выбора, хотя есть тенденция в сторону кольцевых методов аннулопластики. Остается также проблемой прогрессирование ТР после коррекции у пациентов с дилатированным ПЖ, которые нуждаются, видимо, в применении других хирургических пособий, нежели изолированная аннулопластика.
Виды патологии
Существует два вида недостаточности ТК:
- Органическая, которая возникает вследствие морфологических изменений створок клапана (сморщивания, фиброзирования, дегенерации) при ревматизме, эндокардите, заболеваниях соединительной ткани и т. д.
- Функциональная форма встречается в три раза чаще органической. В ее случае строение клапана не нарушено. Недостаточность возникает из-за повышенного давления в правом желудочке, что вызывает расширение клапанного фиброзного каркаса и створки не могут полностью сомкнуться. Данная разновидность порока трикуспидального клапана наблюдается в комплексе с митральными пороками сердца и другими патологиями: при легочной гипертензии, тяжелой бронхиальной астме (т. е. при состояниях, приводящих к перегрузке и повышению давления в ПЖ).
Симптомы трикуспидальной недостаточности
Основную клиническую картину рисуют признаки хронической сердечной недостаточности (ХСН):
- затруднение дыхания (одышка), усиливающееся при физической нагрузке;
- быстрое наступление усталости;
- сонливость;
- ноющие боли в груди;
- тахикардия;
- отеки на ногах, особенно по вечерам;
- тяжесть или ноющие боли в правом боку под ребром из-за увеличения печени;
- синюшная окраска губ и кончика носа;
- пульсация расширенных шейных вен.
На поздних стадиях часто возникают нарушения ритма сердца, например фибрилляция предсердий. Пациенты начинают испытывать неприятные ощущения в груди, высокую частоту и неритмичность пульса, головокружения, чувство дурноты, тошноту. Из-за резкого снижения артериального давления они могут даже упасть в обморок.
Фибрилляция предсердий — одно из самых неблагоприятных и опасных осложнений недостаточности ТК, так как оно довольно часто становится причиной ишемических инсультов.
Чем отличается сердечная недостаточность при пороке от состояния другого происхождения? Даже при крайне выраженных явлениях застоя крови во внутренних органах люди могут чувствовать себя вполне здоровыми, не испытывать никаких неприятных ощущений и, более того, прекрасно переносить физические нагрузки.
Степени недостаточности трикуспидального клапана
Для объективной оценки прогресса порока учитывается объем регургитации (обратного заброса крови) согласно данным в таблице ниже.
| Степень регургитации | Эхо-КГ признак | Симптомы |
| Трикуспидальная недостаточность 1-й степени | Минимальный и едва заметный ток крови без каких-либо нарушений гемодинамики | Может наблюдаться у здоровых людей. Нет абсолютно никаких симптомов |
| Трикуспидальная недостаточность 2-й степени | Регургитация на 2 см от ТК | Ввиду компенсации гемодинамических расстройств может сопровождаться небольшой одышкой при интенсивной физической работе |
| Недостаточность трикуспидального клапана 3-й степени | Регургитация на расстоянии более 2 см от ТК | Появляется одышка при привычной нагрузке, учащение сердцебиения, незначительная тяжесть в ногах и их отечность по вечерам |
| Недостаточность ТК 4-й степени | Регургитация, занимающая практически всю полость ПП | Развернутая картина ХСН: затруднение дыхания, боли в сердце, отеки, тяжесть в правом боку и т. д. |
Публикации в СМИ
Трикуспидальная недостаточность — неспособность правого предсердно-желудочкового клапана эффективно препятствовать обратному движению крови из правого желудочка в правое предсердие во время систолы желудочков сердца.
Частота • По данным аутопсий пороки трёхстворчатого клапана обнаруживают у 15–30% больных c ревматическими пороками сердца • Трикуспидальная недостаточность составляет 85% пороков трёхстворчатого клапана • По данным ЭхоКГ трикуспидальную недостаточность I степени можно выявить практически у всех здоровых людей.
Этиология • Первичная трикуспидальная недостаточность при врождённых аномалиях (аномалии Эбштайна, аномалиях количества створок, в сочетании с дефектом межпредсердной перегородки или при корригированной транспозиции магистральных) — 50%, травме сердца, карциноидном синдроме (вследствие образования деформирующих фиброзных бляшек в створках клапана), миксоматозной дегенерации или ревматическом поражении клапана, эндокардите наркоманов (изолированное поражение трикуспидального клапана — 40% случаев), синдромах дисплазии соединительной ткани (обычно пролапс трикуспидального клапана при синдроме Марфана или Элерса–Данло) • Вторичная трикуспидальная недостаточность вследствие дилатации фиброзного кольца при высокой лёгочной гипертензии осложняет 90% всех пороков митрального клапана (из них 95% стенозов митрального клапана) и 90% случаев дилатационной кардиомиопатии • Вторичная трикуспидальная недостаточность вследствие ишемической дисфункции или разрыва папиллярных мышц при инфаркте правого желудочка.
Патофизиология • При первичной недостаточности возрастает нагрузка объёмом правых отделов сердца, увеличиваются размеры их полостей, происходит застой крови в большом круге кровообращения • В ряде случаев при дилатации правого предсердия возникают его тромбозы, а также суправентрикулярные нарушения ритма сердца (аномалия Эбштайна часто сочетается с синдромом Вольффа–Паркинсона–Уайта) • Присоединение вторичной недостаточности при митральных пороках, осложнённых высокой лёгочной гипертензией, обычно сопровождается разгрузкой малого круга кровообращения и некоторым улучшением гемодинамики без существенного застоя в большом круге кровообращения и снижения ударного объёма • По мере прогрессирования порока сердечный выброс уменьшается более значительно • При повышении давления в правом предсердии более 10 мм рт.ст. развивается застой в большом круге кровообращения • Выделяют четыре степени порока: I — едва определимая обратная струя крови, II — обратный ток определяется на расстоянии 2 см от клапана, III — струя регургитации определяется на расстоянии более 2 см от клапана, IV — регургитация определяется на большом протяжении полости правого предсердия.
Клиническая картина и диагностика • Жалобы •• У грудных детей обычно выявляют тяжёлую сердечную недостаточность и цианоз, в более старшем возрасте — одышку, повышенную утомляемость, цианоз и симптомы правожелудочковой недостаточности • В 25% случаев начальное проявление — наджелудочковая тахикардия как проявление синдрома Вольффа–Паркинсона–Уайта или фибрилляции предсердий при их дилатации • Жалобы, обусловленные сопутствующими состояниями при вторичной недостаточности (болевой синдром при инфаркте правого желудочка, симптомы пороков митрального клапана и др.).
• Периферические симптомы •• Пульсация яремных вен •• Пульсация по левому краю грудины, увеличивающаяся на вдохе •• Пальпируемая пульсация правого предсердия и лёгочной артерии в систолу желудочков •• Пульсация печени.
• Клапанные симптомы •• Систолическое дрожание •• Ослабление I тона •• Усиление лёгочного компонента II тона •• III тон •• Звуки хлопающего паруса при пролапсе клапана •• Пансистолический шум (особенно при повышенной постнагрузке правого желудочка) над мечевидным отростком грудины, часто музыкальный или напоминающий звук клаксона, интенсивность которого усиливается на вдохе (симптом Риверо-Корвальо) или при надавливании на печень •• При тяжёлой трикуспидальной недостаточности иногда выслушивают низкочастотный протодиастолический или мезодиастолический шум.
• Симптомы недостаточности в большом круге кровообращения •• Расширение размеров сердца вправо •• Набухание шейных вен •• Увеличение печени •• Симптом Плеша — набухание шейных вен при лёгкой компрессии печени во время её пальпации •• Отёки •• Асцит.
• Симптомы основного заболевания (синдрома Марфана, инфекционного эндокардита, ИМ, ТЭЛА).
Специальные исследования • ЭКГ •• Признаки гипертрофии и перегрузки правых отделов сердца •• -Волна и пароксизмы тахикардии из АВ-узла при синдроме Вольффа–Паркинсона–Уайта •• Фибрилляция и трепетание предсердий •• АВ-блокада при аномалии Эбштайна или расщеплении септальной створки клапана. • Яремная флебограмма: выраженные волны V, высота которых коррелирует со степенью тяжести трикуспидальной регургитации. • Рентгенография органов грудной клетки •• Выбухание дуг правого желудочка и правого предсердия •• Расширение теней полых вен •• При вторичной недостаточности — усиление лёгочного рисунка, расширение и неструктурность корней лёгких, линии Керли В, выбухание дуг левых отделов сердца и лёгочной артерии.
• ЭхоКГ •• Увеличение размеров полостей и гипертрофия стенок правых отделов сердца •• Расширение верхней полой вены •• Расширение диаметра фиброзного кольца клапана при вторичном пороке •• Деформация клапанного аппарата при ревматизме •• Признаки других клапанных или врождённых аномалий •• Смещение фиброзного кольца клапана и «атриализация» правого желудочка, а также увеличение амплитуды движения створок при аномалии Эбштайна •• Утолщение и деформация створок при карциноидном синдроме •• Наличие вегетаций или дефектов створок при инфекционном эндокардите •• Регистрация потока регургитации в допплеровском режиме и определение тяжести регургитации по отношению площади струи к площади правого предсердия (I степень — соотношение не превышает 1:3, II степень — 2:3, III степень — превышает 2:3) •• По максимальной скорости регургитирующей струи (v) рассчитывают систолическое давление в лёгочной артерии (СДЛА): СДЛА = СДПЖ (в отсутствие стеноза лёгочной артерии); СДПЖ = 4v2 + ЦВД, где СДПЖ — систолическое давление в правом желудочке •• Чреспищеводную ЭхоКГ проводят всем пациентам для исключения тромбоза правого предсердия и вегетаций, даже при нормальном сердечном ритме.
• Катетеризация правых отделов сердца •• На кривой давления в правом предсердии — выраженная волна V и крутой Y-спад •• При тяжёлой недостаточности — волна A и X-спад сглажены, поэтому кривая давления в правом предсердии сходна с таковой в правом желудочке •• При изолированной недостаточности — ускорение АВ-кровотока в период раннего диастолического наполнения •• Наличие высокого конечного диастолического АВ-градиента давления свидетельствует о сопутствующем стенозе трёхстворчатого клапана •• Проводят измерение давления в правом желудочке, правом предсердии и лёгочной артерии в покое и на фоне проб с кислородом и аминофиллином для определения обратимости лёгочной артериальной гипертензии и прогноза хирургического лечения •• При повышении систолического давления в правом желудочке более 60 мм рт.ст. практически всегда причиной трикуспидальной недостаточности бывают митральные пороки.
• Правая вентрикулография •• Регистрация потока регургитации •• Оценка топографии правых отделов сердца при аномалии Эбштайна и исключение сопутствующих аномалий (транспозиция магистральных сосудов, ДМПП и др.).
• Коронарная ангиография •• Выполняют при наличии эпизодов стенокардии и положительных результатах нагрузочного тестирования, а также всем женщинам старше 45 лет, мужчинам старше 40 лет и всем кандидатам на реконструкцию нескольких клапанов •• У 14% пациентов с пороками трёхстворчатого клапана выявляют ИБС.
ЛЕЧЕНИЕ • Консервативное лечение •• В отсутствие лёгочной гипертензии даже тяжёлая недостаточность обычно поддаётся терапии диуретиками и венозными вазодилататорами (нитраты внутрь и в виде пластырей, при тяжёлой рефрактерной трикуспидальной недостаточности — ингибиторы АПФ) •• Дозу подбирают в зависимости от ЦВД, диуреза и выраженности отёков •• Эффективность сердечных гликозидов при синусовом ритме невелика •• При рефрактерной трикуспидальной недостаточности и тяжёлой дисфункции правого желудочка показаны инотропные средства в/в (предпочтительно добутамин) •• При лёгочной гипертензии наиболее благоприятный эффект оказывает снижение давления в лёгочной артерии: в ряде случаев эффективны диуретики и вазодилататоры, но их следует применять с осторожностью, поскольку диапазон приемлемых значений наполнения сердца сужен, а способность увеличивать сердечный выброс в ответ на снижение ОПСС ограничена •• Профилактику инфекционного эндокардита рекомендуют во всех случаях первичной трикуспидальной недостаточности, а при вторичной трикуспидальной недостаточности необходимости в профилактике, по-видимому, нет •• При инфекционном эндокардите гемодинамические осложнения и эмболии переносятся лучше, чем при эндокардите левых отделов сердца, поэтому антибиотикотерапию перед операцией можно проводить дольше (в ряде случаев вообще удаётся обойтись без хирургического вмешательства).
• Хирургическое лечение •• Показания ••• III–IV степень трикуспидальной недостаточности с выраженными клиническими проявлениями ••• Гемодинамически значимые пороки в сочетании со II и большей степенью относительной трикуспидальной недостаточности ••• III–IV степень бессимптомного порока при грубой деформации створок или клапанного аппарата •• Противопоказания ••• Тяжёлая сопутствующая патология, угрожающая жизни больного ••• Терминальная стадия недостаточности кровообращения ••• Отрицательный результат проб с аминофиллином и кислородом ••• Активность ревматического процесса не считают противопоказанием к оперативному лечению •• Методы хирургического лечения ••• Шовные методы Кея–Бойда и ДеВега или опорно-кольцевой метод Карпантье аннулопластики используют при первичном пороке и сохранном клапанном аппарате ••• При грубых морфологических изменениях клапана, инфекционном эндокардите, аномалии Эбштайна и неэффективности предшествующей аннулопластики проводят протезирование клапана биологическими искусственными клапанами (30% операций на трёхстворчатом клапане) ••• Неоднозначное отношение к механическим клапанам в трикуспидальной позиции вызвано повышенным тромбообразованием в правых отделах сердца, обусловленным, по-видимому, низкой концентрацией ПгI2, обладающего антитромботическим эффектом (этот Пг синтезируется в лёгких и поступает с током крови только в левые отделы сердца).
Специфические осложнения • ТЭЛА • Вторичный инфекционный эндокардит • Тромбоз протеза • Дегенеративные изменения биологического протеза и необходимость в репротезировании • АВ-блокада.
Прогноз • При естественном течении порока прогноз практически всецело определяется сопутствующими состояниями, например тяжестью поражения митрального и аортального клапанов •• Присоединение вторичного трикуспидального порока ухудшает прогноз •• При травматической недостаточности пациенты, выжившие в остром периоде, обычно относительно легко переносят порок в течение 5–10 лет, после чего наступает быстрое прогрессирование симптомов •• Среди пациентов с умеренной трикуспидальной недостаточностью после оперативной коррекции сопутствующего тяжёлого митрального порока 66% пациентов в дальнейшем нуждаются в коррекции прогрессирующей трикуспидальной недостаточности • Прогноз при оперативном лечении •• Госпитальная летальность — 14,1%.
Синонимы • Недостаточность правого предсердно-желудочкового клапана • Недостаточность трикуспидального клапана. Сокращения • СДЛА — систолическое давление в лёгочной артерии • СДПЖ — систолическое давление в правом желудочке.
МКБ-10 • I07.1 Трикуспидальная недостаточность
Диагностика: УЗИ-критерии и другие методы
Осматривая человека с трикуспидальной недостаточностью, я должен обратить внимание на наличие следующих признаков:
- усиленная и разлитая пульсация в подложечной области, которая возникает из-за выраженного утолщения и расширения правого желудочка;
- увеличенная и пульсирующая печень;
- очень характерный симптом правожелудочковой ХСН — гепатоюгулярный рефлюкс (когда я надавливаю на печень, шейные вены начинают сильно набухать);
- при прослушивании сердца можно столкнуться с продолжительным систолическим шумом на мечевидном отростке у нижнего края грудины (этот хрящ находится в подложечной области).
Мой главный инструментальный способ диагностики трикуспидальной недостаточности — это эхокардиография (Эхо-КГ, УЗИ сердца). Ее основные критерии окончательного вердикта:
- регургитация крови в правое предсердие;
- ширина регургитирующей струи более 7 мм;
- площадь отверстия регургитации более 40 мм2;
- расширение полостей и утолщение мышечного слоя ПЖ и ПП;
- усиленная пульсация расширенной нижней полой вены.
Также одним из критериев наличия болезни является реверсивный ток крови в печеночных венах. На пленке ЭКГ я довольно часто обнаруживаю признаки перегрузки правых отделов сердца, а именно:
- гипертрофия ПП и ПЖ: высокий остроконечный зубец P в отведениях II, III, aVF (так называемый «P-пульмонале»), высокие зубцы R в I, II отведении, глубокие зубцы S в отведениях V5, V6;
- неполная блокада правой ножки пучка Гиса;
- мерцательная аритмия (фибрилляция предсердий).
Чтобы лучше отследить нарушения ритма, я провожу холтеровское (суточное) мониторирование ЭКГ, так как многие аритмии бывают приступообразными (пароксизмальными) и могут не обнаружиться на обычной кардиограмме.
Недостаточность трехстворчатого клапана
ОПРЕДЕЛЕНИЕ, ЭТИОЛОГИЯ И ПАТОГЕНЕЗнаверх
Патологический заброс крови из правого желудочка в правое предсердие вследствие нарушения смыкания трехстворчатого клапана. Причины: органические — ревматическая болезнь, инфекционный эндокардит, карциноидный синдром, синдром Марфана, болезнь Фабри, болезнь Уиппла, пролапс трехстворчатого клапана, ревматоидный артрит, СКВ, врожденные пороки (синдром Эбштейна и др.), дисфункция папиллярных мышц, ЛС (метисергид, фенфлурамин); функциональные (чаще всего при приобретенном пороке) — расширение кольца при анатомически нормальном клапане, изменение геометрии правого желудочка вызванное чаще всего пороком митрального клапана, а также легочной гипертензией, инфарктом правого желудочка, врожденным пороком сердца (например, стенозом легочной артерии).
КЛИНИЧЕСКАЯ КАРТИНА наверх
Обычно преобладают симптомы порока митрального клапана, которому сопутствует порок трехстворчатого клапана.
1. Субъективные симптомы: снижение переносимости физической нагрузки, слабость, тяжесть и распирание в правом подреберье.
2. Объективные признаки: пульсация значительно расширенных яремных вен, симптом Плеша; у пациентов с выраженной недостаточностью появляется пульсация сосудов головы и шеи, реже, пульсация глазных яблок, правого желудочка, печени; на поздних стадиях порока — генерализованый отек подкожной клетчатки, асцит и желтовато-цианотичная окраска покровов; пансистолический шум, усиливающийся при глубоком вдохе, а также диастолический шум (при выраженной недостаточности).
ДИАГНОСТИКАнаверх
Дополнительные методы исследования
1. ЭКГ: P pulmonale, признаки гипертрофии правого желудочка и часто неполная блокада правой ножки пучка Гиса; обычно фибрилляция предсердий.
2. Рентгенография органов грудной полости: при функциональной недостаточности — кардиомегалия с расширением тени правого предсердия, может появиться выпот в плевральной полости и расширение непарной вены; при выраженной недостаточности — увеличение правого желудочка.
3. Эхокардиография: оценка структуры, степени недостаточности клапана и систолического давления в правом желудочке (давление >55 мм рт. ст. предполагает вторичную причину порока); выраженная недостаточность трехстворчатого клапана при нормальной структуре клапана может появиться при систолическом давлении в легочной артерии ≥55 мм рт. ст.; недостаточность при систолическом давлении в легочной артерии <40 мм рт. ст. скорее указывает на патологию в структуре клапана; у многих здоровых лиц имеет место клинически незначимая недостаточность.
ЛЕЧЕНИЕ наверх
1. Недостаточность трехстворчатого клапана в сочетании с митральным пороком:
1) изолированная коррекция стеноза митрального клапана может существенно уменьшить степень функциональной недостаточности трехстворчатого клапана;
2) операция пластики трехстворчатого клапана → при значительной недостаточности или расширении кольца (≥40 мм или >21 мм/м2) и необходимости операции на митральном клапане;
3) у пациентов с тяжелой трикуспидальной недостаточностью после вмешательства на клапане левого сердца при наличии у них жалоб или прогрессирующей дилатации правого желудочка или снижении его функции, без снижения функции клапанов левого сердца, тяжелого нарушения функции правого или левого желудочка и без тяжелого сосудистого поражения легких → подумайте о возможности хирургического лечения.
2. Выраженная первичная изолированная трикуспидальная недостаточность с субъективными симптомами и без тяжелой правожелудочковой недостаточности: пластика клапана, при невозможности → замена клапана.
3. Выраженная изолированная трикуспидальная недостаточность бессимптомная или с маловыраженными симптомами, но с прогрессирующим расширением правого желудочка или ухудшением его функции: рассмотреть возможность оперативного лечения.
4. В сочетании с нарушениями проводимости: установка электрода для эпикардиальной стимуляции во время операции замены клапана.
ПРОГНОЗ наверх
Пациенты с выраженной трикуспидальной недостаточностью, независимо от ее причины, имеют плохой отдаленный прогноз из-за нарастающей правожелудочковой дисфункции и застоя крови в венах большого круга кровообращения.
Лечение: методы и показания
Первостепенная задача медиков — устранение причины несостоятельности клапана.
Медикаментозная терапия имеет несколько направлений:
- борьба с ХСН и максимально возможное замедление ее прогресса;
- профилактика и лечение нарушений ритма сердца;
- предотвращение тромбозов.
В лечении сердечной недостаточности я применяю следующие лекарственные препараты:
- бета-адреноблокаторы — «Бисопролол», «Метопролол»;
- ингибиторы АПФ — «Периндоприл», «Лизиноприл»;
- антагонисты альдостерона, или калийсберегающие диуретики — «Спиронолактон».
При отеках я использую более мощные мочегонные средства — «Торасемид», «Индапамид». Если в полостях (грудной, брюшной) или перикардиальной сумке скапливается слишком много жидкости, я советуюсь с хирургами насчет ее откачивания. В зависимости от полости, с которой убирают лишнее, выделяют следующие процедуры: плевральная пункция, лапароцентез, пункция перикарда.
Для лечения аритмий назначаются антиаритмические препараты — «Амиодарон», «Пропафенон». Чтобы предотвратить тромбообразование и избежать возникновения эмболии легочной артерии или инсульта у больных с фибрилляцией предсердий, я применяю антикоагулянты — «Варфарин», «Дабигатран», «Ривароксабан».