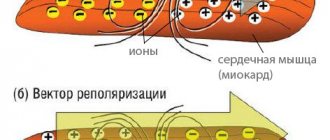
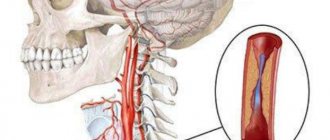
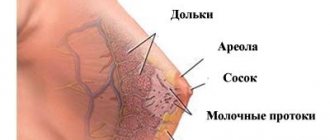
Аорта – самый крупный непарный артериальный сосуд большого круга кровообращения, идущий от сердца и питающий все внутренние органы и системы, кроме легких. На всем своем протяжении аорта имеет равномерную толщину и одинаковое строение. Под влиянием неблагоприятных экзогенных и эндогенных факторов нарушается ее строение: на стенках появляются атеросклеротические бляшки или фиброзные наросты, нарушающие нормальный кровоток.
Обнаружить уплотнение аорты можно с помощью различных диагностических методов: рентгенографического, флюорографического или ультразвукового исследования. Специалисты, обнаружив подобный дефект, должны найти основные причины патологии и назначить правильное лечение. В противном случае болезнь может привести к тяжелым последствиям: расслоению стенок аорты и разрыву кровеносного сосуда. Эти осложнения сопровождается большой кровопотерей и часто заканчиваются смертью больного.
В зависимости от расположения очага поражения выделяют следующие формы патологии:
- Уплотнение корня аорты,
- Уплотнение дуги аорты,
- Уплотнение восходящей аорты,
- Уплотнение нисходящей части аорты.
Причины патологий аорты
Аортальная патология возникает под воздействием трех групп факторов:
- Устранимых. К ним относят малоподвижный образ жизни, злоупотребление алкоголем, курение и употребление большого количества жирной пищи.
- Частично устранимых. К таким факторам относят сахарный диабет, ожирение, хроническую интоксикацию организма, инфекционные болезни и артериальную гипертензию.
- Неустранимых. К таким факторам аортальной патологии относят генетическую предрасположенность и возраст.
В чем опасность этой патологии?
Опасность уплотнения аорты зависит от степени изменения ее стенок. Когда она незначительна, вреда организму не будет.
Если же изменение толщины стенок сопровождается кальцинозом, фиброзом, то есть, нарушением структуры — это означает что возможно возникновение серьезных заболеваний сосудов.
Ими могут быть:
- Тромбоз. При нем происходит закупоривание аорты с нарушением кровотока.
- Аортальная аневризма. При ней выпячиваются стенки сосуда вследствие его истончения или растяжения.
- Расслоение аорты. Кровь затекает между слоями стенок, усугубляя их деформацию, что приводит к ее разрыву.
- Аортальный стеноз. Сужение стенок сосуда, которое заканчивается непроходимостью.
Закупоривание аорты вызывает сердечные патологии, которые с трудом поддаются лечению. В тяжелых случаях развивается тромбоз головного мозга. Это происходит из-за непроходимости сосудов, питающих его.
Результатом разрыва аорты становится большая потеря крови, которая заканчивается смертью при неоказании медицинской помощи.
Классификация заболевания
Специалисты выделяют 3 стадии заболевания:
- Начальную. На этой стадии в аорте появляется жировое пятно, происходит разрыхление сосудистой стенки, она отекает. Специальные ферментальные вещества способны обеспечивать защиту сосудов и растворять липиды, но их ресурсы со временем истощаются. Патология в стадии липидного пятна может быть обнаружена при диагностике даже у младенцев.
- Среднюю. На этой стадии липидные отложения разрастаются, формируется бляшка, состоящая из жиров и волокон соединительной ткани. На данном этапе бляшки еще являются жидкими. Их можно растворить. Основную опасность представляет рыхлость бляшек. Отложения могут разорваться и блокировать артерию.
- Тяжелую. На этой стадии бляшка уплотняется благодаря солям кальция, может расти и сужать просвет артерии. Это приводит к закупориванию сосуда. Нельзя исключить развитие некроза тканей, гангрены органа или конечности.
Что это такое?
Понять, что такое фиброз створок митрального клапана, можно, взглянув на особенности его строения и функционирования. Суть работы клапанного аппарата заключается в пропускании крови (в одну сторону) при сокращении определенного отдела. Основную роль выполняют створки, которые представлены рыхлой соединительной тканью. Их питание осуществляется за счет мельчайших сосудов. У аортального клапана три створки (правая, левая, задняя), а у митрального их две (задняя, передняя).
Под влиянием раздражающих факторов соединительная ткань становится более грубой, из-за чего перестает полноценно выполнять свои функции (сохранять гибкость створок). Со временем значительно сокращается число кровеносных сосудов, питающих клапан. Клетки, из которых он состоит, начинают умирать, замещаясь на фиброзную ткань. Она представляет собой одну из разновидностей соединительных тканей, которой характерна высокая прочность.
Симптомы атеросклероза
Симптомы патологии зависят от локализации процесса и стадии.
К основным признакам закупоривания сосудов относят:
- периодическое усиление сердцебиения;
- шум в ушах;
- пульсацию в области шеи, в голове;
- слабость;
- одышку;
- быструю утомляемость;
- головокружения.
Для патологии коронарных артерий характерны:
- давящие и жгучие боли в груди;
- тошнота и рвота;
- потеря сознания;
- головокружения;
- одышка (особенно в положении лежа);
- скачки артериального давления.
Для дуговой патологии характерны сильные боли. Обычно они отдают в лопатку, левую руку и плечо. Боли усиливаются при физических нагрузках и стрессовых ситуациях. Боль нельзя снять нитроглицерином.
Основной симптом при поражениях грудного отдела – боль за грудиной. Также пациенты страдают от одышки, ускоренного сердцебиения, боли в голове, головокружений, ухудшения внимания и памяти, затрудненного глотания. При закупоривании аортального клапана больной испытывает выраженный дискомфорт в грудине. Также может возникнуть боль, одышка, головокружение.
Патологии сосудов брюшного отдела приводят к болям в животе. Дискомфорт не имеет четкой локализации. Обычно он появляется после приема пищи. Также больные жалуются на запоры и диарею, вздутие живота, снижения аппетита.
При атеросклерозе подвздошных артерий ухудшается кровоснабжение ног. Конечности немеют и отекают, сокращается тонус мышц. В некоторых случаях заболевание приводит к появлению язв на стопах.
Особенно опасными являются многочисленные осложнения патологии.
К ним относят:
- выпячивание стенки артерии;
- стенокардию;
- коллапс аорты;
- ишемию тканей и органов;
- сердечную недостаточность;
- инсульт;
- тромбоз висцеральных артерий.
При любых осложнениях атеросклероза пациент ощущает резкое ухудшение состояния. Боль невозможно снять даже сильными обезболивающими. В этом случае следует немедленно вызвать скорую!
Лечение уплотнения стенок аорты народными средствами
Если стенки аорты уплотнены, лечение этой проблемы можно проводить и народными средствами. Самым распространенным из них является использование чесночного масла.
Для этого головку чеснока нужно очистить, размять и залить стаканом подсолнечного масла. В течение суток этот настой нужно периодически перемешивать, после чего, добавив сок одного лимона и еще раз перемешав, оставить на неделю отстаиваться в прохладном месте.
Описанное средство принимают по чайной ложечке трижды в день за 30 минут до приема пищи. Один курс такого лечения длится три месяца, после чего на месяц нужно прерваться, а затем снова повторить лечение.
Диагностика патологии
Диагностика патологии включает:
- Осмотр пациента.
- Сбор анамнеза.
- Инструментальные и лабораторные исследования.
На приеме врач выслушает все жалобы, оценит вес пациента, измерит артериальное давление, определит все факторы риска, выявит признаки патологии.
Лабораторные исследования обязательно включают анализ крови с оценкой таких показателей, как концентрация липопротеидов, холестерина и триглицеридов.
Инструментальные исследования включают:
- ЭКГ.
- Аортографию и ангиографию. При таком обследовании специалисты исследуют состояние сосудов, выявляют аневризмы и иные поражения.
- Коронаграфию. Такое обследование позволяет оценить состояние коронарных артерий.
- УЗИ. В рамках обследования выявляются ухудшение кровотока, снижение просвета сосудов, наличие тромбов и бляшек на стенках, появление аневризм.
- Реовазографию. Данное обследование позволяет оценить скорость кровотока.
- КТ и МРТ. Эти методики позволяют быстро обнаружить выпячивания артерий, локализацию и протяженность повреждений.
Диагностические процедуры
Диагностика описываемой патологии включает в себя несколько этапов:
- Для начала пациент сдает нужные анализы, проходит обследование на наличие инфекций.
- Во время аускультативного обследования врач может услышать изменения в тонах аорты, отметить появление характерного шума.
- Информативным является рентгенографическое исследование, флюорография. Аорта уплотнена (что это значит и почему развивается, вы уже знаете), ее тень на снимке удлинена, возможно появление патологического разворота или нехарактерного изгиба по ходу сосуда.
- Золотым стандартом на сегодняшний день является контрастная ангиография. Во время этой процедуры врач может изучить особенности кровотока, увидеть те или иные отклонения.
- Также проводится ультразвуковое исследование, допплерография.
- Если врачу нужны дополнительные сведения, то пациента отправляют на магнитно-резонансную томографию. На трехмерных снимках врач может тщательно осмотреть и изучить структуру аорты, близлежащих органов.
Лечение
Своевременное лечение создает возможности для улучшения качества жизни и предотвращения осложнений. Обычно в первую очередь врач рекомендует скорректировать образ жизни пациента.
Для терапии патологии очень важно:
- Придерживаться правильного питания. Пациенту следует отказаться с соленой, острой и жареной пищи. Важно снизить количество животных жиров. Рацион следует выстраивать на основе овощей и фруктов, бобовых, нежирных молочных продуктов, цельного зерна.
- Посвящать время физическим нагрузкам. Они должны быть регулярными. Физические нагрузки не просто полезны для организма, но и позволяют привести в норму вес.
- Полноценно отдыхать и насыщать организм питательными веществами. Следует спать не менее 7-8 часов, проводить время на природе, принимать комплексы витаминов и минералов.
Непосредственно терапия патологии проводится медикаментозно.
Обычно пациентам назначаются:
- Статины. Данные вещества способствуют снижению концентрации холестерина в крови. Статины уменьшают синтез агрессивных веществ.
- Никотиновая кислота и производные. Данные вещества повышают содержание липопротеидов высокой плотности, сокращают уровень холестерина и триглицедиров.
- Секвестранты желчных кислот. Эти вещества выводят холестерин.
- Фибраты. Данные вещества подавляют синтез триглицеридов в печени и способствуют их быстрому удалению.
- Бета-блокаторы. Эти вещества способствуют устранению дискомфорта и боли в груди, а также снижению давления.
При неэффективности медикаментозного лечения патологии проводятся операции.
Сегодня специалистами осуществляются следующие вмешательства:
- Шунтирование. Операция заключается в наложении шунта, приводящего в норму нарушенный кровоток.
- Ангиопластика. Эта операция заключается в реконструкции сосуда. В результате вмешательства восстанавливается его просвет.
При обнаружении аневризмы она иссекается. Удаленный участок заменяется протезом. Если происходит расширение кольца аортального клапана, он иссекается и заменяется искусственным.
Важно! Разрыв аневризмы лечится только хирургическим путем. Операция проводится экстренно.
В нашей клинике выполняется комплексная терапия патологий. Специалисты не только устраняют проявления болезни, но и ее причины. Благодаря этому увеличивается уровень жизни пациента.
Цены терапии зависят от многочисленных факторов.
В их числе:
- сложность терапии;
- выбранная методика;
- состояние пациента;
- наличие сопутствующих болезней и др.
Цена на комплексную терапию может быть озвучена заранее. Это позволит вам спланировать расходы на услуги нашей клиники.
Важно! Врачи подходят к терапии индивидуально. Они обязательно учитывают все факторы, которые могут повлиять на ее успешность.
Почему может развиться уплотнение?
Уплотнение аорты может сформироваться на любом ее участке. Самым сложным отделом считается дуга, так как в месте изгиба сосуда изменяется скорость течения крови и ее динамика.
Основные причины развития:
- Атеросклероз: при нарушении липидного обмена в крови на стенках сосудов образуются атеросклеротические бляшки. Из-за этого просвет аорты сужается, замедляется кровоток. В результате происходит разрастание фиброзной (рубцовой) ткани, уплотнение стенок.
- Гипертоническая болезнь: при постоянно повышенном аортальном давлении эластичность сосудов нарушается, в них образуются фиброзные соединения. Стенки становятся жесткими и толстыми.
- Инфекционные заболевания (туберкулез, сифилис, сепсис и другие).
- Болезни аутоиммунного характера (склеродермия, аортит).
- Интоксикация в результате длительного лечения антибиотиками приводит к расширению и склерозированию сосудов.
Помимо этого, изменение толщины стенок аорты может происходить в результате неправильного образа жизни и в качестве следствия старения организма.
Факторы риска, повышающие шанс развития этой патологии у взрослых людей:
- пожилой возраст (более 50 лет);
- вредные привычки — табакокурение, алкоголизм;
- злоупотребление жирной пищей, фаст-фудом.
У детей утолщение створок клапана и самой аорты наблюдается в случае плохой наследственности. В детском возрасте патология находится в неактивной фазе, а в дальнейшем может активироваться.
Согласно статистике, самыми частыми причинами развития уплотнения являются — атеросклероз и пожилой возраст (более 80% диагностируемых случаев).
Профилактика атеросклероза аорты
Профилактика атеросклероза аорты позволяет предупредить развитие болезни. Это проще, чем долгое время лечить патологию.
Для устранения обратимых факторов риска достаточно:
- отказаться от курения и употребления спиртного;
- избегать переедания и стрессовых ситуаций;
- избавиться от лишнего веса.
При наследственной предрасположенности к атеросклерозу аорты следует регулярно сдавать кровь для оценки содержания холестерина. Это позволит быстро выявить любые нарушения метаболизма липидов и скорректировать его.
Особенно важно заниматься профилактикой патологии людям с:
- ожирением;
- гипертонией;
- диабетом;
- стенокардией.
Регулярно посещать кардиолога следует всем людям в возрасте от 40 лет. Пристальное внимание здоровью важно уделять тем, кто испытывает приступы стенокардии или перенес инсульт.
Фиброзные кольца клапанов сердца при недифференцированной дисплазии соединительной ткани
Библиографическое описание:
Кузнецова, В. В. Фиброзные кольца клапанов сердца при недифференцированной дисплазии соединительной ткани / В. В. Кузнецова. — Текст : непосредственный // Медицина и здравоохранение : материалы I Междунар. науч. конф. (г. Чита, ноябрь 2012 г.). — Чита : Издательство Молодой ученый, 2012. — С. 26-36. — URL: https://moluch.ru/conf/med/archive/62/2893/ (дата обращения: 18.10.2021).
В литературных источниках имеются сообщения о диаметре митрального и аортального фиброзных колец при дисплазии соединительной ткани. По данным исследования Яковлева В.М. и соавт. [5], увеличение диаметра митрального фиброзного кольца в обе фазы сердечного цикла может служить критерием соединительнотканной дисплазии митрального клапана с нарушением его функции. В этой работе было выявлено статистически достоверное увеличение диаметра митрального фиброзного кольца в обе фазы сердечного цикла в группе пациентов с пролапсом митрального клапана с наличием митральной регургитации в сравнении с контрольной группой (пациенты без дисплазии соединительной ткани) и внутри опытной группы (пациенты с пролапсом митрального клапана без митральной регургитации). В работе Малеева Э.Г и соавт. [1] пациенты с пролапсом митрального клапана также имели больший диаметр митрального фиброзного кольца по сравнению с контрольной группой.
В работе J.R. Matos-Souza et al. [6] было обследовано 627 человек с изолированным пролапсом митрального клапана и сопоставимых с ними по возрасту, полу и индексу массы тела 627 человек без пролапса митрального клапана; всего 454 мужчины и 800 женщин в возрасте 37,9 ± 0,3 с индексом массы тела 23,7 ± 0,1 кг/м2. Лица с пролапсом митрального клапана имели достоверно больший диаметр аортального фиброзного кольца по сравнению с контролем (30,4 ± 0,1 против 29,5 ± 0,1 мм). Кроме этого, многофакторный анализ продемонстрировал независимую ассоциацию между пролапсом митрального клапана и размером аортального кольца на модели, включающей вмешивающиеся переменные – возраст, пол, индекс массы тела, площадь поверхности тела, уровень кровяного давления и индекс массы миокарда левого желудочка [6].
Относительно диаметра двух других фиброзных колец сердца при дисплазии соединительной ткани в доступной литературе данных не обнаружено.
Цель исследования:
изучение диаметра фиброзных колец клапанов сердца при дисплазии соединительной ткани и их взаимосвязи с антропометрическими показателями и морфо-функциональными показателями сердца.
Материал и методы.
В основу исследования положены данные, полученные при обследовании 60 пациентов с ДСТ в возрасте от 18 до 44 лет (средний возраст — 25,9±6,8 года) и 27 пациентов без признаков ДСТ. Объективное исследование проводилось по общепринятой методике. Во время физикального исследования проводились следующие измерения: рост, вес, окружность грудной клетки (ОГК), окружность талии (ОТ), размах рук, рост сидя, длина кисти, длина стопы. На основании полученных данных рассчитывались ИМТ, площадь поверхности тела (ППТ), индексы пропорциональности (ИП между ОГК и ростом стоя, ИП между длиной ног и длиной туловища, индекс Пинье). У пациентов определялись САД, ДАД и ЧСС.
Наличие дисплазии соединительной ткани у пациентов устанавливалось по совокупности признаков [3]. Эходопплеркардиография проводилась на ультразвуковом сканере экспертного класса с цветным допплеровским картированием VIVID-3 фирмы General Electric (США). Ультразвуковое исследование сердца выполнено в соответствии с рекомендациями Европейской и Американской ассоциаций эхокардиографии для проведения измерений, расчетов и оценки камер сердца и магистральных сосудов (2006 г.). Локация проводилась в парастернальной позиции (III-IV межреберье по левому краю грудины) в горизонтальном положении больного с приподнятым головным концом путем изменения угла наклона датчика для последовательного изображения различных отделов сердца. Для получения структурной характеристики сердца оценивали конечные диастолический и систолический диаметры (КДР ЛЖ, КСР ЛЖ, см), объемы (КДО, КСО, мл) ЛЖ, толщину задней стенки ЛЖ (ТЗСЛЖ, см) в систолу и в диастолу, толщину межжелудочковой перегородки (ТМЖП, см) в систолу и в диастолу, индексированные показатели объемов ЛЖ (ИКСО, ИКДО, мл/м2), массу миокарда ЛЖ (ММЛЖ, г). Структурно-геометрические изменения определяли по индексу ММЛЖ (ИММЛЖ, г/м2), относительной толщине стенок левого желудочка и миокардиальному стрессу. Объемные показатели левого желудочка и фракцию выброса левого желудочка рассчитывали по формулам Teichholz [4]. Показатели систолической функции левого желудочка включали: фракцию выброса (ФВ, %), фракцию укорочения передне-заднего диаметра ЛЖ в систолу (ФУ, %), скорость циркулярного укорочения волокон миокарда (Vcf, c-1). При оценке состояния центральной и периферической гемодинамики учитывали значения ударного (УО, мл) и минутного (МО, л/мин) объемов, ударный (мл/м2) и сердечный (л/мин/м2) индексы, общее периферическое сосудистое сопротивление (ОПСС, дин*с*см-5). Диастолическую функцию левого желудочка изучали по временным и скоростным параметрам трансмитрального диастолического потока: время изоволюметрического расслабления (ВИР, с), время ускорения раннего трансмитрального диастолического потока(АТ, с), замедления раннего трансмитрального диастолического потока (ДТ, с), период изгнания (ЕТ, с), пиковые скорости быстрого (Е, м/с) и медленного (А, м/с) диастолического наполнения, их соотношение (Е/А) [4].
Статистическая обработка данных проводилась с помощью пакета прикладных программ Statistica 6.0 фирмы StatSoft и MIX для Windows, а также возможностей Microsoft Excel. Анализ данных на нормальность распределения проводился с помощью теста Колмогорова-Смирнова. В качестве нулевой гипотезы принималась гипотеза о нормальном распределении количественного признака. Так как распределение всех признаков было отлично от нормального распределения, то признаки описаны медианой и интерквартильным размахом (25 и 75 процентили). Сравнение двух независимых групп выполнялось с помощью U-теста Манна-Уитни. Оценка зависимости между двумя переменными проводилась с применением коэффициента корреляции Спирмена. Уровень принятия или отклонения нулевой гипотезы составлял ниже 0,05.
Результаты и обсуждение.
Общая характеристика сравниваемых групп. Пациенты с ДСТ (табл.1) имели достоверно большую длину тела по сравнению с группой контроля (p=0,0001) и достоверно меньшую массу тела (p=0,0004), что является отражением общих свойств популяции пациентов с дисплазией соединительной ткани. При этом ИМТ и ППТ у пациентов с ДСТ были статистически значимо ниже, чем у пациентов группы контроля (p<0,0001 и p=0,02). ОТ и ОГК у пациентов с ДСТ были статистически значимо меньше, чем у пациентов группы контроля (p=0,00001 и p=0,0005). Рост сидя, длина кисти, стопы и размах рук статистически значимо не различались между группами. САД, ДАД и ЧСС у пациентов с ДСТ оказались статистически значимо снижены по сравнению с группой контроля (p=0,007, p=0,03 и p=0,02 соответственно).
Таблица 1
Общая характеристика пациентов в исследуемых группах, Ме (Р25-Р75)
| Показатель | Пациенты с ДСТ (n=149) | Контрольная группа (n=55) | p |
| Рост, см | 176 (170-183) | 170 (161-177) | 0,0001 |
| Рост сидя, см | 92 (90-96) | 93 (90,5-96,5) | 0,5 |
| ОГК, см | 79 (73-86) | 86 (80-94) | 0,0005 |
| ОТ, см | 70 (67-76) | 79 (75,5-88) | 0,00001 |
| Размах рук, см | 179 (173-186) | 181 (171-186,5) | 0,8 |
| Кисть, см | 20 (19-21) | 20 (19-21) | 0,77 |
| Стопа, см | 27(26-29) | 28 (25,5-29) | 0,79 |
| Вес, кг | 60 (53-68) | 66 (57-76) | 0,0004 |
| ИМТ, кг/м2 | 19,3 (17,7-21,2) | 22,8 (21,2-25,6) | <0,00001 |
| ППТ, м2 | 1,76 (1,62-1,89) | 1,81 (1,72-1,94) | 0,02 |
| САД, мм рт ст | 100 (90-110) | 110 (100-120) | 0,007 |
| ДАД, мм рт ст | 60 (55-70) | 65 (60-80) | 0,03 |
| ЧСС, уд/мин | 70 (64-75) | 77 (69-84) | 0,02 |
Таким образом, пациенты с ДСТ антропометрически достоверно отличались от группы контроля. Пациенты с ДСТ характеризовались достоверно большим ростом, меньшими массой тела, ИМТ, площадью поверхности тела, ОГК, ОТ, что свойственно популяции данных пациентов в целом.
При сопоставлении структурно-геометрических параметров сердца у пациентов с ДСТ и лиц контрольной группы выявлен ряд отличий (табл.2).
Размеры всех полостей сердца, измеренные в диастолу, у пациентов с ДСТ оказались достоверно меньше, чем у пациентов группы контроля (p<0,05), что объясняется меньшими размерами тела у пациентов с ДСТ. КДО ЛЖ и индексированный показатель КДО ЛЖ у пациентов с ДСТ были также достоверно занижены по сравнению с контрольными показателями (p=0,008 и p=0,03). Таким образом, при одной и той же площади поверхности тела пациенты с ДСТ характеризовались меньшим КДО ЛЖ. При этом отсутствовало достоверное уменьшение КСР ЛЖ (p=0,44), КСО (p=0,32) и ИКСО ЛЖ (p=0,89). По толщине МЖП и ЗСЛЖ в диастолу группы достоверно не различались между собой (p= 0,32 и p=0,19), в систолу толщина МЖП и ЗСЛЖ была достоверно меньше у пациентов с ДСТ (p=0,02 и p=0,002). Относительная толщина стенки левого желудочка не различалась между группами (p=0,37). ММЛЖ и ИММЛЖ были достоверно меньше в группе с ДСТ (p=0,03 и p=0,045). Диаметр нижней полой вены в группе с ДСТ был занижен по сравнению с показателем группы контроля (p=0,04). По величине КСМС существенных различий в сравниваемых группах не обнаружено (p=0,21).
Таблица 2
Структурно-геометрическая характеристика сердца пациентов с ДСТ и группы контроля, Ме (Р25-Р75)
| Показатель | Пациенты с ДСТ (n=60) | Контрольная группа (n=27) | p |
| КДР ЛЖ, см | 4,5(4,23-4,82) | 4,8(4,5-5,0) | 0,009 |
| КСР ЛЖ, см | 3,0(2,7-3,19) | 3,1(2,8-3,2) | 0,44 |
| МЖП с, см | 1,17(1,01-1,27) | 1,25(1,15-1,35) | 0,02 |
| МЖП д, см | 0,82(0,7-0,92) | 0,85(0,8-0,91) | 0,32 |
| ЗСЛЖ с, см | 1,29(1,2-1,4) | 1,4(1,3-1,5) | 0,002 |
| ЗСЛЖ д, см | 0,82(0,75-0,93) | 0,86(0,8-0,96) | 0,19 |
| Отн. толщина стенки ЛЖ | 0,35 (0,32 -0,39) | 0,34 (0,33-0,38) | 0,37 |
| ЛП, см | 2,9(2,6-3,18) | 3,3(3,0-3,5) | 0,0004 |
| ПП, см | 3,18(2,9-3,46) | 3,4(3,27-3,6) | 0,003 |
| НПВ, см | 1,06(0,81-1,85) | 1,8(1,43-2,0) | 0,04 |
| ПЖ,см | 2,1(1,9-2,38) | 2,4(2,0-2,63) | 0,02 |
| ММЛЖ, г | 119,7(95,29-146) | 135,5(117,1-151) | 0,03 |
| КДО ЛЖ, мл | 92,75 (79-108,5) | 108 (92,84-118) | 0,008 |
| КСО ЛЖ, мл | 35 (27,27-39,66) | 38 (30-41) | 0,32 |
| ИКДО ЛЖ, мл/м2 | 53,65(48,88-61,9) | 58,06(52,45-67,05) | 0,03 |
| ИКСО ЛЖ, мл/м2 | 20,31(16,08-22,54) | 20,03(17,2-22,68) | 0,89 |
| ИММЛЖ, г/м2 | 72,29(59,67-82,38) | 74,86(69,9-87,68) | 0,045 |
| КСМС ЛЖ, дин*см2 | 109,56(95,13-123,99) | 112,92(106,02-122,38) | 0,21 |
По данным литературы, различные показатели состояния трансаортального и транспульмонального кровотока дают представление о систолической функции левого и правого желудочков[2]. В то же время показатели трансмитрального и транстрикуспидального диастолического кровотока отражают диастолическую функцию левого и правого желудочков (табл.3).
Пиковая трансаортальная скорость и пиковый трансаортальный градиент давления в группе пациентов с ДСТ были статистически значимо меньше, чем в группе контроля (p=0,005 и p=0,004). Пиковая трансмитральная скорость и пиковый трансмитральный градиент давления не различались между группами (p=0,51 и p=0,39). Также не было выявлено статистически значимых различий по показателям пиковой транстрикуспидальной скорости и пикового транстрикуспидального градиента давления (p= 0,97 и p=0,97). Пиковая транспульмональная скорость и пиковый транспульмональный градиент давления в группе с ДСТ был достоверно занижен по сравнению с контрольными показателями (p=0,006 и p=0,007).
Таблица 3
Трансклапанные пиковые градиенты скорости и давления пациентов с ДСТ и группы контроля, Ме (Р25-Р75)
| Показатели | Пациенты с ДСТ(n=60) | Контрольная группа (n=27) | p |
| Пиковая трансаортальная скорость, м/с | 1,07(0,95-1,18) | 1,17(1,03-1,3) | 0,005 |
| Пиковый трансаортальный градиент давления, мм рт. ст. | 4,5(3,63-5,6) | 5,48(4,24-6,76) | 0,004 |
| Пиковая трансмитральная скорость, м/с | 0,79(0,72-0,9) | 0,8(0,76-0,9) | 0,51 |
| Пиковый трансмитральный градиент давления, мм рт. ст. | 2,51(2,05-3,24) | 2,56(2,31-3,24) | 0,39 |
| Пиковая транспульмональная скорость, м/с | 0,89(0,77-0,99) | 0,95(0,9-1,16) | 0,006 |
| Пиковый транспульмональный градиент давления, мм рт. ст. | 3,14(2,39-3,92) | 3,61(3,21-5,38) | 0,007 |
| Пиковая транстрикуспидальная скорость, м/с | 0,71(0,62-0,78) | 0,7(0,63-0,77) | 0,97 |
| Пиковый транстрикуспидальный градиент давления, мм рт. ст. | 1,96(1,55-2,45) | 1,96(1,59-2,37) | 0,97 |
При изучении сократительной функции левого желудочка у пациентов с ДСТ и контрольной группы также были выявлены закономерные различия (табл. 4).
ФВ и ФУ ЛЖ были снижены у пациентов с ДСТ по сравнению с контрольной группой, однако различия не были статистически значимы (p=0,18 и p=0,09 соответственно). Тем не менее можно отметить тенденцию к снижению фракции укорочения левого желудочка у пациентов с ДСТ. Скорость циркулярного укорочения волокон миокарда у пациентов с ДСТ была достоверно ниже, чем у лиц группы контроля (p=0,0007). Процент систолического укорочения МЖП и ЗСЛЖ статистически значимо не различался между группами (p=0,30 и p=0,7).
Таблица 4
Показатели систолической функции ЛЖ у пациентов с ДСТ и группы контроля, Ме (Р25-Р75)
| Показатели | Пациенты с ДСТ (n=60) | Контрольная группа (n=27) | p |
| ФВ, % | 64,18 (60,28-68,01) | 65,4 (62-72) | 0,18 |
| ФУ, % | 34,82 (31,74-37,78) | 36,36(33,33-41,67) | 0,09 |
| Скорость циркулярного укорочения волокон миокарда, с-1 | 0,11 (0,10-0,13) | 0,13 (0,12 -0,15 ) | 0,0007 |
| % систолического укорочения МЖП | 41,33 (29,47-55,56) | 46,34 (30,53-60) | 0,39 |
| % систолического укорочения МЖП | 56,17 (40,91-73,33) | 60 (50,52-66,67) | 0,7 |
Основными интегративными показателями, характеризующими работу сердца, являются УО и МО желудочков. У лиц с ДСТ важнейшие параметры насосной функции миокарда были занижены по сравнению с контрольными показателями (табл.5).
Таблица 5
Состояние центральной и периферической гемодинамики у пациентов с ДСТ и группы контроля, Ме (Р25-Р75)
| Показатели | Пациенты с ДСТ (n=60) | Контрольная группа (n=27) | p |
| УО, мл | 57,2 (52-69,34) | 70 (61-81) | 0,003 |
| МОК, л/мин | 4,08 (3,4-4,82) | 5,46 (4,31-6,24) | 0,0001 |
| УИ, мл/м2 | 34,62 (30,87-39,27) | 38,1 (34,78-45,25) | 0,01 |
| СИ, л/м2*мин | 2,38 (2,03-2,9) | 3,03 (2,55-3,33) | 0,0006 |
| ОПСС, дин*с*см-5 | 1483,15(1275,5-1789,42) | 1224,39(1103,17-1534,85) | 0,01 |
У лиц с ДСТ оказались достоверно уменьшены все показатели, характеризующие работу левого желудочка: УО (p=0,003), МОК (p=0,0001), УИ (p=0,01), СИ (p=0,0006). ОПСС в группе с ДСТ достоверно превышало контрольные значения (p=0,01), что можно объяснить компенсаторной реакцией на снижение сердечного выброса.
Таким образом, сократительный процесс левого желудочка у пациентов в нашей выборке по сравнению с контрольной группой характеризовался снижением скорости циркулярного сокращения волокон миокарда, пиковой трансаортальной скорости и определяющего ее градиента давления, УО, МОК, УИ, СИ. Компенсаторные реакции со стороны периферической гемодинамики характеризовались повышением ОПСС.
В последние годы внимание многих исследователей сердечной гемодинамики приковано к диастолической функции, изменения которой являются наиболее ранними в патофизиологии нарушений сердечной гемодинамики (табл.6).
У пациентов с ДСТ ВИР ЛЖ (IVRT) оказалось достоверно уменьшенным по сравнению с группой контроля (p=0,01). Время ускорения раннего трансмитрального диастолического потока AT у пациентов с ДСТ было статистически значимо меньше чем в группе контроля (p=0,001). Время замедления раннего трансмитрального диастолического потока DT, реагирующее на изменение жесткости миокарда, не различалось в группах, хотя и имелась тенденция к его увеличению в группе пациентов с ДСТ (p=0,07). Общее время раннего и позднего диастолического потока оказалось статистически значимо больше в группе пациентов с ДСТ (p=0,002) за счет удлинения времени позднего диастолического потока. Время раннего диастолического потока статистически значимо не различалось между группами (p=0,38). Таким образом, у пациентов с ДСТ увеличение продолжительности диастолы происходило за счет фазы систолы предсердия, то есть диастола была более энергоемкой. Отличия по скоростным показателям диастолической функции ЛЖ у лиц с ДСТ были представлены снижением предсердного компонента трансмитрального диастолического потока(p=0,01), что повлекло увеличение соотношения скоростных потоков (p=0,075). Таким образом, пациенты в нашей выборке характеризовались нарушением диастолического наполнения левого желудочка, которое было обусловлено ускорением релаксации, увеличением периода позднего диастолического наполнения и относительным укорочением периода раннего диастолического наполнения.
Таблица 6
Диастолическая функция левого желудочка у пациентов с ДСТ и группы контроля, Ме (Р25-Р75)
| Показатели | Пациенты с ДСТ (n=60) | Контрольная группа (n=27) | p |
| IVRT, мс | 72 (64-80) | 80 (73-88) | 0,01 |
| AT, мс | 72 (60-87) | 88 (80-104) | 0,001 |
| DT, мс | 150(57-192) | 111(44-136) | 0,07 |
| Время раннего и позднего диастолического наполнения, мс | 501 (444-589) | 430 (358-494) | 0,002 |
| Время раннего трансмитрального диастолического потока, мс | 225,5(132-284) | 199 (159-236) | 0,38 |
| Скорость раннего диастолического наполнения, м/с | 0,79(0,72-0,90) | 0,8 (0,76-0,9) | 0,51 |
| Скорость позднего диастолического наполнения, м/с | 0,48(0,43-0,58) | 0,6(0,47-0,63) | 0,01 |
| E/A | 1,56(1,38-1,89) | 1,4(1,23-1,73) | 0,08 |
Фиброзный скелет сердца образован четырьмя кольцами, соединенными между собой соединительной тканью. Предсердия, желудочки, клапаны, легочный артериальный ствол и аорта плотно прикрепляются к этому соединительно-тканному каркасу. У пациентов с ДСТ АФК было достоверно меньше, чем у пациентов группы контроля (p=0,002), что можно объяснить меньшими размерами тела и, соответственно, сердца пациентов с ДСТ (табл.7). В то же время у пациентов с ДСТ наблюдалось патологическое расширение МФК, превышающее контрольные показатели (p=0,007). По данным, приведенным в работе [6], этот показатель может служить критерием соединительнотканной дисплазии митрального клапана с нарушением его функции. Трикуспидальное и пульмональное фиброзные кольца не различались между группами (p=0,46 и p=0,8).
Таблица 7
Диаметр фиброзных колец клапанов пациентов с ДСТ и группы контроля, Ме (Р25-Р75)
| Показатели | Пациенты с ДСТ (n=60) | Контрольная группа (n=27) | p |
| АФК, см | 1,86 (1,73-2,05) | 2,01(1,9-2,3) | 0,002 |
| МФК, см | 3,57 (3,27-3,81) | 3,2(3,0-3,45) | 0,007 |
| ТФК, см | 2,7 (2,5-3,2) | 2,9(2,8-3,0) | 0,46 |
| ПФК, см | 2,1 (1,9-2,25) | 2,05(1,9-2,25) | 0,8 |
Для АФК получены положительные корреляционные связи средней силы с размерами тела (весом (r=0,41, p=0,001), ИМТ (r=0,38, p=0,003), площадью поверхности тела (r=0,36, p=0,005), ОГК (r=0,34, p=0,009), ОТ (r=0,4, p=0,002), индексом пропорциональности ОГК/рост (r=0,3, p=0,02)), показателями преднагрузки (КДО ЛЖ (r=0,46, p=0,0003), ИКДО ЛЖ (r=0,41, p=0,001)), показателями центральной гемодинамики (УО ЛЖ (r=0,51, p=0,00005), МОК (r=0,50, p=0,00007)), ММЛЖ (r=0,43, p=0,0008), показателями систолической функции ЛЖ (толщиной МЖП в систолу (r=0,43, p=0,0008), толщиной ЗСЛЖ в систолу (r=0,42, p=0,001). Отрицательные корреляционные связи умеренной силы получены для АФК и ОПСС (r=-0,41, p=0,002), индекса Пинье (r=-0,38, p=0,005 ).
Были выявлены положительные корреляционные связи средней силы между диаметром МФК и размерами тела (ростом (r=0,31, p=0,02), весом (r=0,33, p=0,02), площадью поверхности тела (r=0,37, p=0,007)), временем изгнания из левого желудочка (r=0,48, p=0,0004), общим временем раннего и позднего трансмитрального диастолического потока (r=0,34, p=0,01), отрицательные корреляционные связи средней силы между диаметром МФК и показателями систолической (ФВ ЛЖ (r=-0,42, p=0,002), скоростью систолического укорочения волокон миокарда (r=-0,54, p=0,00005), % систолического укорочения МЖП (r=-0,29, p=0,04), % систолического укорочения волокон ЗСЛЖ (r=-0,37, p=0,007)) и диастолической функции ЛЖ (временем ускорения раннего трансмитрального диастолического потока (r=-0,52, p=0,0001), пиковой скоростью трансмитрального диастолического потока (r=-0,49, p=0,0003) и ее градиентом (r=-0,48, p=0,0004)).
Наши сведения о патологическом расширении МФК при ДСТ согласуются с данными других авторов [1; 5]. В то же время в литературных источниках мы не встретили сведений о сужении АФК при ДСТ. Уменьшение АФК у наших пациентов можно объяснить уменьшением объема ЛЖ в диастолу (r=0,46, p=0,0003), уменьшением УО ЛЖ (r=0,51, p=0,00005). В работе [6] лица с ПМК имели достоверно больший диаметр аортального фиброзного кольца по сравнению с контролем (30,4 ± 0,1 против 29,5 ± 0,1 мм). Это может быть связано с тем, что в этом исследовании пациенты были старше (средний возраст 37,9 ± 0,3 лет) и не отличались от группы контроля по ИМТ (23,7 ± 0,1 кг/м2). В нашей выборке средний возраст пациентов с ДСТ составил 25,9±6,8 года, средний возраст контрольной группы 25,2± 5,4 года; пациенты достоверно отличались по ИМТ. В группе с ДСТ медиана ИМТ 19,3 кг/м2 (квартили 17,7-21,2), в контрольной группе соответственно 22,8 (21,2-25,6) кг/м2 (p<0,00001).
В нашей выборке получены достоверные корреляции диаметра АФК с ИМТ (r=0,38, p=0,003), а также с индексом Пинье (r=-0,38, p=0,005). Таким образом, более вероятно, что меньший диаметр АФК связан с меньшими размерами тела пациентов с ДСТ и меньшими размерами камер сердца. Однако при меньших размерах камер сердца у пациентов с ДСТ диаметры ТФК и ПФК не отличались между группами.
Литература:
- Анализ деформации миокарда левого желудочка при пролапсе митрального клапана / Э.Г. Малеев [и др.] // Вестн. Санкт-Петерб. мед. акад. последиплом. образования. – 2011. – № 2. – С. 134-142.
- Достижения и перспективы исследования фазовой структуры сердечного цикла с помощью допплерэхокардиографии. Возможности применения в педиатрии [Электронный ресурс]. – Режим доступа: https://crawfordcountyredcross.org/kardiologiya/dostizgeniya_i_ perspektivy. html. – [Дата обращения: 21.02.12].
- Нечаева Г.И. Дисплазия соединительной ткани: терминология, диагностика, тактика ведения пациентов / Г.И. Нечаева, И.А. Викторова. – Омск : ООО Типография БЛАНКОМ, 2007. – 188 с.
- Рыбакова М.К. Практическое руководство по ультразвуковой диагностике. Эхокардиография / М.К. Рыбакова, М.Н. Алехин, В.В. Митьков. – М. : Видар-М, 2008. – 512 с.
- Яковлев В.М. Соединительнотканная дисплазия митрального клапана / В.М. Яковлев, Р.С. Карпов, Е.В. Швецова. – Томск : Сиб. Издат. Дом, 2004. – 144 с.
- Isolated mitral valve prolapse is an independent predictor of aortic root size in a general population / J.R. Matos-Souza // Eur. J. Echocardiogr. – 2010. – Vol. 11, № 3. – P. 302-305.